La cromatografía de gases-espectrometría de masas (GC-MS) combina las características de la cromatografía de gases-líquidos (GC) y la espectrometría de masas (MS). Esto permite identificar diferentes sustancias dentro de una muestra de ensayo. La GC-MS tiene muchos usos, como la detección de drogas, la investigación de incendios, el análisis medioambiental y la investigación de explosivos. También puede utilizarse para identificar muestras desconocidas. La GC-MS también puede utilizarse en la seguridad de los aeropuertos para detectar sustancias en el equipaje o en los seres humanos. Además, la GC-MS puede identificar trazas de elementos en materiales deteriorados, incluso después de que la muestra se haya deshecho tanto que otras pruebas no puedan funcionar.
La GC-MS es la mejor manera de que los expertos forenses identifiquen las sustancias porque es una prueba específica. Una prueba específica identifica positivamente la presencia real de una sustancia concreta en una muestra determinada. Una prueba no específica sólo dice que hay categorías de sustancias en la muestra. Aunque una prueba no específica podría sugerir estadísticamente la identidad de la sustancia, esto podría conducir a una identificación falsa positiva.
Principio de funcionamiento
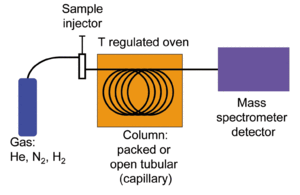
En la GC-MS primero la muestra se volatiliza y se separa en una columna de cromatografía de gases según las diferencias en volatilidad y en la interacción con la fase estacionaria. Cada compuesto sale de la columna en un tiempo característico (tiempo de retención) y entra al espectrómetro de masas, donde se ioniza y se fragmenta. El detector registra la relación masa/carga (m/z) de los iones y sus abundancias, produciendo un espectro de masas que actúa como una "huella" característica de cada compuesto.
Componentes principales
- Inyector: introduce la muestra (líquida o gaseosa) en el sistema; puede ser split/splitless según la concentración.
- Columna capilar: columna recubierta con fase estacionaria donde ocurre la separación por GC.
- Gas portador: helio, hidrógeno o nitrógeno que transporta los analitos por la columna.
- Interfaz: mantiene la transición entre la salida caliente de la GC y la entrada del MS.
- Sistema de ionización: electrón impact (EI) y químico (CI) son los más comunes en GC-MS.
- Analizador de masas: cuadrupolo, trampa iónica, tiempo de vuelo (TOF) u otros; determina la resolución y rango dinámico.
- Detector: registra los iones y genera el espectro de masas.
Modos de análisis e ionización
Los dos modos más habituales en GC-MS son:
- Full scan (barrido completo): se registra el espectro completo en un rango de m/z; útil para identificación cualitativa y búsqueda en bibliotecas.
- SIM (Selected Ion Monitoring): se monitorizan iones específicos; aumenta sensibilidad y selectividad para cuantificación.
En cuanto a ionización, EI (impacto electrónico) produce fragmentación reproducible y es ideal para comparación con bibliotecas. CI (ionización química) da menos fragmentación y mayor probabilidad de observar el ion molecular, útil para determinar la masa molecular.
Preparación de la muestra
La GC-MS requiere que los analitos sean volátiles y térmicamente estables. Para compuestos polares o no volátiles se emplea derivatización (por ejemplo silylación) para hacerlos más volátiles. Otras técnicas de preparación incluyen extracción líquido-líquido, extracción en fase sólida (SPE), microextracción en fase sólida (SPME) y purificación para reducir interferencias de la matriz.
Interpretación de resultados
La identificación fiable combina:
- Tiempo de retención (o índice de retención) — comparado con estándares.
- Espectro de masas — comparación con bibliotecas (por ejemplo NIST) o con espectros de referencia.
- Presencia del ion molecular y fragmentos característicos — ayuda a confirmar la estructura.
Se debe tener cuidado con la co-elución (dos compuestos que salen a la vez) y con efectos de matriz que pueden alterar señales. Para aumentar la confianza de identificación se recomienda confirmar con estándares y, cuando sea necesario, usar técnicas complementarias.
Aplicaciones típicas
- Forense: identificación de drogas, venenos, ignífugos y restos de explosivos.
- Medio ambiente: análisis de contaminantes orgánicos volátiles, pesticidas y hidrocarburos.
- Alimentos y bebidas: control de adulteraciones, residuos de pesticidas y análisis de aroma.
- Clínica y toxicológica: análisis de fármacos en sangre, orina y tejidos.
- Industria: control de calidad y análisis de productos químicos.
Ventajas y limitaciones
- Ventajas: alta sensibilidad y selectividad, capacidad para identificar compuestos desconocidos mediante bibliotecas, buena reproducibilidad y amplio uso forense y ambiental.
- Limitaciones: solo sirve para compuestos que pueden volatilizarse; compuestos térmicamente lábiles o muy polares requieren derivatización o técnicas alternativas (p. ej. LC-MS). Además, la interpretación requiere experiencia y controles de calidad.
Alternativas y complementariedad
La LC-MS (cromatografía líquida acoplada a espectrometría de masas) se utiliza cuando los analitos no son volátiles o son termo-lábiles. Muchas investigaciones modernas combinan ambas técnicas para cubrir una gama más amplia de compuestos.
Buenas prácticas y control de calidad
Para resultados fiables es importante:
- Usar estándares y curvas de calibración para cuantificación.
- Realizar controles en blanco y controles de matriz.
- Verificar el rendimiento del sistema (resolución, sensibilidad, línea base).
- Documentar procedimientos y criterios de identificación (tiempo de retención, coincidencia de espectros, umbrales de similitud).
En resumen, la GC-MS es una técnica poderosa y ampliamente utilizada para la identificación y cuantificación de compuestos orgánicos volátiles y semivolátiles. Su combinación de separación por cromatografía y análisis estructural por espectrometría de masas la hace especialmente valiosa en forense, medio ambiente, salud pública e industria.