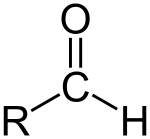
Un aldehído (/ˈældɪhaɪd/) es un compuesto orgánico que contiene un grupo formilo. Un grupo formilo es una parte de una molécula con la estructura R-CHO. Está formado por un carbono doblemente unido al oxígeno (grupo carbonilo, C=O). Ese mismo carbono está unido además a un átomo de hidrógeno y a un grupo R, donde R representa una cadena lateral (el resto de la molécula). El grupo sin la cadena lateral se llama grupo aldehído o grupo formilo. Los aldehídos son compuestos muy comunes en la química orgánica, y muchos de ellos son responsables de aromas y sabores característicos; por ejemplo, varios ingredientes de fragancias naturales y sintéticas son aldehídos.
Estructura y nomenclatura
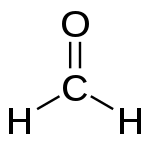
La fórmula general de un aldehído se escribe R-CHO. Si R = H, el aldehído más simple es el metanal (conocido tradicionalmente como formaldehído). Cuando R es un grupo alquilo o arilo aparecen otros aldehídos como el etanoal (acetaldehído) o el benzaldehído. En la nomenclatura IUPAC los aldehídos se nombran cambiando la terminación del alcano correspondiente por -al (por ejemplo, metano → metanal, etano → etanal).
Propiedades físicas
- Los aldehídos son generalmente polares por la presencia del grupo carbonilo, lo que les confiere cierta solubilidad en solventes polares y agua (los aldehídos de cadena corta son miscibles con agua).
- En pesos moleculares bajos suelen ser volátiles y de olor fuerte o penetrante; aldehídos aromáticos (como el benzaldehído o la vainillina) pueden tener olores agradables.
- Puntos de ebullición: más altos que los hidrocarburos de masa similar por dipolo, pero menores que los alcoholes porque no forman enlaces de hidrógeno tan eficientemente entre sí.
Reactividad y reacciones importantes
El carbono carbonílico de los aldehídos es electrofílico, por lo que experimentan con facilidad reacciones de adición nucleofílica. Entre las reacciones más relevantes se encuentran:
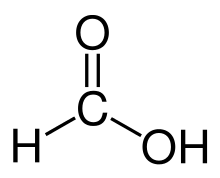
- Oxidación: los aldehídos se oxidan fácilmente a ácidos carboxílicos (R-CHO → R-COOH). Por eso reaccionan positivamente en pruebas químicas como la de Tollens (espejo de plata) o la de Fehling/Benedict (en aldehídos alifáticos que pueden oxidarse).
- Reducción: se reducen a alcoholes primarios (R-CHO → R-CH2OH) mediante hidruros (NaBH4, LiAlH4) o hidrogenación catalítica.
- Formación de hemiacetales y acetales: en presencia de alcoholes y ácido, los aldehídos forman hemiacetales y, con exceso de alcohol, acetales (protección funcional en síntesis orgánica).
- Formación de iminas (bases de Schiff): reacción con aminas primarias para dar R-CH=NR'.
- Adiciones nucleofílicas variadas: reacciones con cianuros (formación de cianohidrinas), con hidrazinas (formación de hidrazonas), con dinitrofenilhidrazina (DNPH) para derivatización y análisis.
Diferencias con las cetonas
La diferencia estructural más clara entre un aldehído y una cetona es la posición del grupo carbonilo:
- En los aldehídos el grupo formilo está en un extremo de la cadena: R-CHO. El carbono del carbonilo tiene un átomo de hidrógeno unido (—CHO).
- En las cetonas el grupo carbonilo está en el interior de la cadena y está unido a dos grupos orgánicos: R-CO-R'.
Estas diferencias producen consecuencias importantes:
- Mayor reactividad de los aldehídos frente a la oxidación: por tener un hidrógeno unido al carbono carbonílico, los aldehídos se oxidan con facilidad a ácidos carboxílicos; las cetonas resisten esa oxidación bajo condiciones suaves.
- Mayor electrofilicidad: como las cetonas tienen dos grupos que pueden donar electrones por efecto inductivo o por impedimento estérico, el carbono carbonílico de las cetonas suele ser menos electrofílico que el de los aldehídos, lo que hace a los aldehídos más susceptibles a reacciones de adición nucleofílica.
- Diferencias físicas: las cetonas generalmente presentan puntos de ebullición algo más altos que los aldehídos de masa molar similar cuando la interacción intermolecular favorece, aunque las tendencias pueden variar según la estructura.
Ejemplos comunes
- Metanal (formaldehído): H-CHO — ampliamente usado en resinas y como conservante; es tóxico y clasificado como carcinógeno en ciertos contextos.
- Etanal (acetaldehído): CH3-CHO — intermedio en varias síntesis y producto de la oxidación del etanol.
- Benzaldehído: C6H5-CHO — aldehído aromático responsable del olor a almendra amarga; usado en síntesis y en fragancias.
- Vanillina (aldehído aromático sustituido): compuesto responsable del aroma de la vainilla.
Aplicaciones y seguridad
- Aplicaciones: producción de polímeros y resinas (por ejemplo, formaldehído en resinas fenólicas), síntesis orgánica (intermedios), industrias de fragancias y sabores (benzaldehído, vanillina), conservantes y reactivos analíticos.
- Seguridad: muchos aldehídos son irritantes para ojos, piel y vías respiratorias; algunos (como el formaldehído) son tóxicos y están asociados con riesgos carcinogénicos. Se deben manejar con precaución, en campana extractora y con equipo de protección adecuado.
En resumen, los aldehídos son compuestos con el grupo formilo R-CHO, de gran importancia en química orgánica por su reactividad (oxidación, adición nucleofílica, formación de acetales e iminas) y por su presencia en muchos compuestos con olores y aplicaciones industriales. Su principal diferencia frente a las cetonas es la posición terminal del grupo carbonilo y la presencia del hidrógeno unido al carbono carbonílico, lo que condiciona su comportamiento químico.