Este artículo sólo trata de la química de los alcoholes.
El alcohol que se utiliza en las bebidas es el etanol; puede encontrar más información en la página de bebidas alcohólicas y alcoholismo.
En química, alcohol es un término general que se refiere a muchos compuestos orgánicos utilizados en la industria y la ciencia como reactivos, disolventes y combustibles. Los alcoholes son hidratos de carbono formados por un grupo alquilo con uno o más grupos hidroxilos (-OH) unidos a sus átomos de carbono. El alcohol es incoloro y también transparente.
Definición y fórmula general
Un alcohol es un compuesto orgánico que contiene uno o varios grupos hidroxilo (-OH) enlazados a átomos de carbono saturados. La fórmula general de un alcohol monohídrico acíclico simple es R–OH, donde R representa un grupo alquilo (por ejemplo, metilo CH3–, etilo C2H5–).
Estructura y enlaces
- El grupo hidroxilo está formado por un átomo de oxígeno unido a un hidrógeno. El enlace O–H es polar, porque el oxígeno es más electronegativo que el hidrógeno.
- La polaridad del grupo –OH permite la formación de puentes de hidrógeno entre moléculas, lo que afecta fuertemente las propiedades físicas (puntos de ebullición, solubilidad).
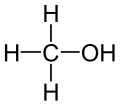
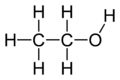
- Ejemplos: metanol (CH3OH), etanol (C2H5OH), propan-1-ol (C3H7OH).
Clasificación
- Según el número de grupos –OH: monohídricos (un –OH), dioles o glicoles (dos –OH), polialcoholes (varios –OH, por ejemplo, glicerol).
- Según el carbono portador del –OH:
- Primarios (1º): –CH2–OH (ej. etanol).
- Secundarios (2º): –CH(OH)– (ej. isopropanol).
- Ternarios (3º): –C(OH)– con tres sustituyentes carbonados (ej. tert-butanol).
- Alcoholes especiales: fenoles (–OH unido a un anillo aromático; propiedades distintas a los alcoholes alifáticos), alcoholes benílicos, vinylicos, allenílicos, etc.
Nomenclatura básica
Según la IUPAC, se nombra derivando el nombre del alcano correspondiente y sustituyendo la terminación –ano por –ol, indicando la posición del grupo –OH con un número (por ejemplo, propan-2-ol). Para alcoholes con varios grupos –OH se usan sufijos como –diol, –triol, etc. En nombres comunes también existen formas tradicionales (etanol, metanol, glicerol, etc.).
Propiedades físicas
- Muchos alcoholes de cadena corta son líquidos incoloros a temperatura ambiente; algunos polialcoholes son viscosos o sólidos.
- Gracias a los puentes de hidrógeno, los alcoholes presentan puntos de ebullición más altos que los alcanos de masa molar similar.
- Los alcoholes de bajo peso molecular (metanol, etanol, propanol) son miscibles con agua. A medida que crece la cadena carbonada, la solubilidad en agua disminuye.
- La densidad de la mayoría de los alcoholes comunes es menor que la del agua (por ejemplo, etanol ≈ 0,79 g·mL−1), aunque hay excepciones en compuestos muy polares y con estructuras compactas.
Propiedades químicas y reacciones principales
- Acidez: los alcoholes son ácidos débiles (pKa típicos alrededor de 16 para alcoholes alifáticos simples). Se pueden desprotonar con bases fuertes para formar alcóxidos (R–O−), que son nucleófilos potentes.
- Oxidación: los alcoholes primarios se oxidan a aldehídos y luego a ácidos carboxílicos; los secundarios a cetonas; los terciarios resisten la oxidación suave y suelen romperse con oxidantes fuertes.
- Deshidratación: bajo catálisis ácida, los alcoholes pueden perder agua para formar alquenos (eliminación E1/E2).
- Esterificación: reacción con ácidos carboxílicos (o sus derivados) para formar ésteres (Fischer esterificación) utilizada en síntesis y en la industria de aromas y polímeros.
- Sustitución nucleofílica: conversión a haluros de alquilo (R–X) mediante agentes como SOCl2, PBr3 o mediante protonación y sustitución en condiciones adecuadas.
- Reacciones con agentes deshidratantes o reactividad con haluros de ácidos, anhídridos y isocianatos para obtener éteres, ésteres y otros derivados.
Obtención y síntesis
- Hidratación de alquenos (adición de agua en presencia de ácido) produce alcoholes. Este es un método industrial muy usado (por ejemplo, producción de etanol a partir de etileno).
- Fermentación de azúcares por levaduras produce etanol (ruta biotecnológica importante para bebidas y biocombustibles).
- Reducción de aldehídos y cetonas con agentes reductores (NaBH4, LiAlH4) produce alcoholes primarios o secundarios.
- Reacción de Grignard con formaldehído, aldehídos o cetonas seguida de hidrólisis para formar alcoholes de distinto orden.
- Hidrólisis de haluros de alquilo o ésteres bajo condiciones apropiadas.
Usos y aplicaciones
- Solventes en síntesis orgánica, pinturas, tintas y lacas (por ejemplo, etanol, isopropanol).
- Combustibles y aditivos: etanol como biocombustible o aditivo (gasohol); metanol y butanol también se usan como combustibles o precursores.
- Materias primas industriales: producción de éteres, ésteres, anticongelantes (etilenglicol), polímeros y plastificantes.
- Productos farmacéuticos y cosméticos: muchos fármacos contienen grupos alcohol y se emplean alcoholes como disolventes y excipientes.
- Desinfectantes y antisépticos: etanol e isopropanol son ampliamente usados por su actividad germicida.
- Alimentos y bebidas: etanol es el alcohol presente en bebidas; otros alcoholes pueden añadirse como sabores o solventes para esencias.
Seguridad y toxicidad
- Muchos alcoholes son inflamables; su manipulación y almacenamiento requieren precauciones frente a fuentes de ignición.
- Metanol es altamente tóxico por ingestión o inhalación: puede causar ceguera irreversible y muerte por formación de formaldehído y ácido fórmico.
- El etanol es tóxico en dosis altas y su consumo continuado causa dependencia y efectos adversos sobre la salud; sin embargo, su toxicidad es menor que la del metanol.
- Algunos alcoholes y sus vapores pueden ser irritantes para la piel, ojos y vías respiratorias; se deben usar equipos de protección adecuados.
Identificación y análisis
- En espectroscopía infrarroja (IR) los alcoholes muestran una banda ancha característica de O–H entre ≈ 3200–3600 cm−1.
- En resonancia magnética nuclear (1H NMR) el protón hidroxilo aparece en una región variable (dependiente del disolvente y del intercambio), mientras que los protones vecinos al carbono portador del –OH aparecen en las regiones típicas de metilos, metilenos o metinos.
- Pruebas químicas clásicas: oxidación selectiva, reacciones con anhidridos o haluros acídicos para formar ésteres, o formación de alcóxidos con bases fuertes.
Notas finales
Los alcoholes constituyen una familia muy amplia y versátil de compuestos orgánicos, esenciales en síntesis química, procesos industriales y productos de uso cotidiano. Su comportamiento depende de la estructura (número y posición de los grupos –OH, tamaño de la cadena carbonada y presencia de otros grupos funcionales), por lo que su estudio combina aspectos físicos, químicos y de seguridad.