El carbono es un elemento químico muy importante, cuyo símbolo químico es C. Toda la vida conocida en la Tierra lo necesita. El carbono tiene masa atómica 12 y número atómico 6. Es un no metal, es decir, no es un metal.
Cuando el hierro se alea con el carbono, se forma el acero duro. El carbono en forma de carbón es un combustible importante.
Propiedades fundamentales
El carbono es un elemento tetravalente: puede formar hasta cuatro enlaces covalentes con otros átomos. Su configuración electrónica es 1s² 2s² 2p². El peso atómico medio de los átomos de carbono en la naturaleza es aproximadamente 12,011 u, debido a la mezcla de isótopos (principalmente 12C y 13C).
- Estado a temperatura ambiente: sólido.
- Enlace y química: forma enlaces simples, dobles y triples, y cadenas largas (catenación), lo que permite la enorme diversidad de moléculas orgánicas.
- Propiedades físicas: presenta puntos de fusión y ebullición muy altos; a presión atmosférica muchas formas de carbono subliman a temperaturas del orden de varios miles de °C.
- Electronegatividad: moderada (≈ 2,5 en la escala de Pauling), lo que favorece tanto enlaces covalentes puros como enlaces polarizados en moléculas orgánicas.
Alótropos (formas del carbono)
El carbono existe en distintas formas cristalinas y moleculares llamadas alótropos, con propiedades físicas muy distintas entre sí:
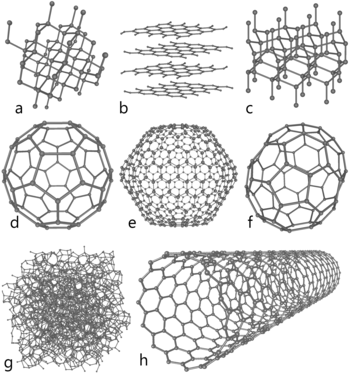
- Diamante: red tridimensional muy rígida; es el material natural más duro conocido y es un aislante eléctrico.
- Grafito: capas planas de átomos en anillos hexagonales que se deslizan entre sí; conductor eléctrico en el plano de las capas y buen lubricante sólido.
- Grafeno: una sola capa de grafito (monocapa de átomos en una red hexagonal); destaca por su resistencia mecánica, conductividad eléctrica y alta movilidad electrónica.
- Fullerenos y nanotubos: moléculas y estructuras tubulares basadas en anillos de carbono; tienen aplicaciones en materiales avanzados, electrónica y medicina experimental.
- Carbón amorfo y carbón activado: formas porosas usadas en filtración y adsorción.
Isótopos y abundancia
Los isótopos naturales más comunes son 12C (estable, mayoritario) y 13C (estable, ≈1,1 %). El 14C es radiactivo y se emplea en la datación por radiocarbono para restos orgánicos hasta decenas de miles de años.
Importancia biológica y en la Tierra
El carbono es la columna vertebral de las moléculas biológicas: forma la base de carbohidratos, lípidos, proteínas y ácidos nucleicos. El ciclo del carbono —intercambio entre atmósfera (CO2), biosfera, hidrosfera y geosfera— regula el clima y la disponibilidad de carbono para los ecosistemas.
Usos y aplicaciones
El carbono y sus compuestos tienen multitud de aplicaciones en ciencia, industria y vida cotidiana. Entre las más relevantes:
- Materiales: acero (aleaciones de hierro y carbono), fibras de carbono para estructuras ligeras y resistentes, grafito para electrodos y lubricantes.
- Energía: combustibles fósiles (carbón, petróleo, gas natural) contienen carbono; su combustión produce CO2 y energía.
- Filtración y purificación: carbón activado y adsorbentes basados en carbono para agua y aire.
- Electrónica y nanotecnología: grafeno, nanotubos y fullerenos en sensores, baterías, supercondensadores y dispositivos electrónicos.
- Medicina y química: compuestos orgánicos en fármacos, materiales biocompatibles y sistemas de liberación controlada.
Impacto ambiental
La combustión de materiales carbonosos libera dióxido de carbono (CO2), principal gas de efecto invernadero producido por actividades humanas, y contribuye al cambio climático. Además, la quema incompleta puede generar monóxido de carbono (CO), tóxico para la salud. Por ello existen esfuerzos para reducir emisiones, capturar carbono y promover fuentes de energía renovable.
Curiosidades
- El diamante y el grafito están hechos del mismo elemento, pero sus propiedades son muy distintas por la diferente estructura enlazada de los átomos.
- El carbono es capaz de formar millones de compuestos conocidos; la rama de la química que los estudia es la química orgánica.
En resumen, el carbono es un elemento versátil y esencial: esencial para la vida, base de innumerables materiales y compuestos industriales, y protagonista en desafíos globales como el cambio climático y el desarrollo de nuevas tecnologías.