Los átomos de un elemento químico pueden existir en variantes que tienen propiedades químicas muy similares pero masas diferentes. Estas variantes se llaman isótopos del elemento. Todos los átomos de un mismo elemento comparten el mismo número de protones (es decir, el mismo número atómico), pero los distintos isótopos difieren en el número de neutrones, y por tanto en su número de masa (protones + neutrones). La masa de un átomo está relacionada con la cantidad de sustancia o materia que contiene, y por eso isótopos distintos presentan masas y, en sentido práctico, pesos diferentes.
Notación y cálculo del número de neutrones
Un isótopo se suele identificar indicando el nombre del elemento y su número de masa, por ejemplo carbono-12 (escrito también 12C) o carbono-14 ( 14C ). Si Z es el número atómico (protones) y A el número de masa, entonces el número de neutrones es N = A − Z. Por ejemplo, el carbono tiene Z = 6; por eso 12C tiene 6 neutrones (12 − 6) y 14C tiene 8 neutrones (14 − 6).
Isótopos estables y radiactivos
Algunos isótopos son estables: no cambian espontáneamente a otro núcleo. Otros son inestables y se transforman con el tiempo mediante procesos de desintegración radiactiva; éstos son los isótopos radiactivos. La desintegración puede emitir partículas (alfa, beta) o radiación gamma y transforma el núcleo en otro isótopo o incluso en otro elemento.
Ejemplos comunes:
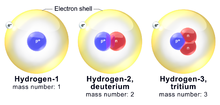
- Hidrógeno: protio (1H, estable), deuterio (2H, estable) y tritio (3H, radiactivo, vida media ≈ 12,3 años).
- Carbono: carbono-12 (estable) y carbono-14 (radiactivo, vida media ≈ 5 730 años; se usa en datación).
- Uranio: U-235 (radiactivo, fisible, vida media ≈ 7,04×10^8 años) y U-238 (radiactivo, vida media ≈ 4,468×10^9 años).
- Oxígeno: 16O, 17O y 18O (16O y 18O estables; las proporciones entre ellas se usan en paleoclimatología).
Diferencias importantes entre isótopos
- Propiedades químicas: generalmente muy similares porque dependen principalmente de los electrones y el número de protones (Z).
- Propiedades físicas: masas distintas llevan a ligeras diferencias en comportamientos físicos —por ejemplo, en la velocidad de difusión, puntos de ebullición y fraccionamiento isotópico en procesos naturales.
- Propiedades nucleares: la estabilidad, modos y tasas de desintegración radiactiva dependen de la combinación específica de protones y neutrones.
Aplicaciones y usos
Los isótopos tienen múltiples usos en ciencia, tecnología y medicina:
- Datación: el carbono-14 se usa para datar materiales orgánicos hasta decenas de miles de años.
- Medicina nuclear: isótopos como 99mTc (vida media ≈ 6 h), 18F (≈ 110 min, usado en PET), o 131I (≈ 8 días) se usan en diagnóstico y tratamiento.
- Energetía nuclear: isotopos fisibles como U-235 y Pu-239 son centrales en reactores y armas nucleares.
- Seguimiento y trazadores: isótopos (estables o radiactivos) permiten seguir reacciones químicas, rutas metabólicas y movimientos de sustancias en el medio ambiente.
- Estudios climáticos y ecológicos: análisis de proporciones de 18O/16O, 13C/12C, 15N/14N informan sobre temperaturas pasadas, dietas y ciclos biogeoquímicos.
Abundancia isotópica y masa atómica
Un elemento en la naturaleza suele ser una mezcla de isótopos en determinadas proporciones (abundancias isotópicas). La masa atómica que aparece en la tabla periódica es un promedio ponderado de las masas de sus isótopos según esas abundancias. Por ejemplo, el carbono tiene masa atómica ≈ 12,011 u porque la mayor parte es 12C, pero existe también una fracción pequeña de 13C y trazas de 14C.
Cómo se detectan y miden
Las técnicas más habituales para distinguir y cuantificar isótopos son la espectrometría de masas (incluyendo ICP-MS, IRMS) y detectores de radiación para isótopos radiactivos. Estas técnicas permiten determinar abundancias relativas, identificar trazas radiactivas y medir vidas medias.
Seguridad y consideraciones
Los isótopos radiactivos requieren manejo y almacenamiento seguros: su radiación puede dañar tejidos y materiales. Los riesgos dependen del tipo de radiación, la energía y la vida media. En aplicaciones médicas y nucleares se aplican normas estrictas para proteger a personas y al medio ambiente.
Resumen
Un isótopo es una variante de un elemento químico con igual número de protones pero distinto número de neutrones, lo que cambia su masa y su comportamiento nuclear. Pueden ser estables o radiactivos, y tienen aplicaciones clave en datación, medicina, energía, investigación ambiental y muchas otras áreas. La comprensión de los isótopos —su notación, abundancia y propiedades— es fundamental en química, física, geología, biología y tecnología.