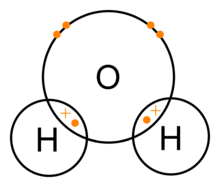
Los enlaces covalentes son enlaces químicos que se forman cuando dos átomos —generalmente no metálicos— comparten uno o más pares de electrones de valencia para alcanzar una configuración electrónica más estable. Un ejemplo muy conocido es el agua (H2O), en la que el hidrógeno (H) y el oxígeno (O) quedan unidos por enlaces covalentes.
Formación del enlace covalente
Los electrones que participan en los enlaces son los electrones de valencia, que ocupan la capa exterior del átomo. La distribución de estas capas viene determinada por la mecánica cuántica y, en muchos casos, los átomos tienden a completar una capa exterior con ocho electrones (regla del octeto) o con dos en el caso de los elementos más ligeros como el hidrógeno y el helio. Sin embargo, hay excepciones (por ejemplo, moléculas con número impar de electrones, elementos del tercer periodo o superiores que pueden expandir su octeto, etc.).
Cuando dos átomos se aproximan, los orbitales de sus electrones de valencia pueden solaparse. Ese solapamiento crea un nuevo orbital compartido con menor energía que los orbitales aislados, por lo que los electrones tienden a ocuparlo y se libera energía (calor o, en ciertos casos, radiación). El resultado es que la densidad electrónica aumenta en la región entre ambos núcleos y aparece una fuerza neta de atracción que mantiene unidos a los átomos: el enlace covalente.
En un átomo neutro el número de electrones suele coincidir con el número de protones. Los electrones orbitan alrededor del núcleo en orbitales (regiones probabilísticas) y la primera capa admite hasta dos electrones; las siguientes capas suelen admitir hasta ocho en muchos casos sencillos. Los enlaces covalentes se forman por el compartir de estos electrones exteriores entre átomos, no por la transferencia completa que caracteriza al enlace iónico.
Tipos de enlace covalente
- Enlace simple: comparte un par de electrones (por ejemplo H—H en H2).
- Enlace doble: comparte dos pares de electrones (por ejemplo O=O en O2).
- Enlace triple: comparte tres pares de electrones (por ejemplo N≡N en N2).
- Enlace coordenado o dativo: ambos electrones del par compartido proceden del mismo átomo (por ejemplo en algunos complejos y en NH4+).
- Distinción σ y π: los enlaces σ (sigma) resultan del solapamiento frontal de orbitales y suelen ser más fuertes; los π (pi) aparecen por solapamiento lateral y se dan en dobles y triples enlaces junto con el σ.
Polaridad y electronegatividad
Si los átomos que forman el enlace tienen la misma electronegatividad, el par de electrones se reparte simétricamente y el enlace es no polar (por ejemplo H—H, Cl—Cl). Si existe una diferencia de electronegatividad, la nube electrónica se desplaza hacia el átomo más electronegativo, generando cargas parciales (δ− en el átomo que atrae electrones y δ+ en el otro) y dando lugar a un enlace polar. La polaridad de las moléculas depende tanto de la polaridad de los enlaces como de la geometría molecular: una molécula con enlaces polares puede ser apolar si su geometría compensa los dipolos (por ejemplo CO2).
Propiedades físicas relacionadas
- Longitud y energía de enlace: a mayor orden de enlace (simple → doble → triple) suele disminuir la longitud de enlace y aumentar la energía de enlace (mayor fuerza).
- Estado y puntos de fusión/ebullición: las sustancias moleculares con enlaces covalentes débiles entre moléculas (fuerzas intermoleculares pequeñas) suelen tener puntos de fusión y ebullición bajos; en cambio, las redes covalentes (por ejemplo diamante, SiO2) son sólidos firmes con puntos de fusión muy altos porque la red tridimensional está formada por enlaces covalentes fuertes.
- Conductividad eléctrica: en general los compuestos covalentes no conducen la electricidad en estado sólido y líquido, salvo que existan electrones libres o especies iónicas; los conductores covalentes incluyen materiales con electrones deslocalizados (como el grafito).
- Solubilidad: la solubilidad depende de la polaridad; “lo semejante disuelve a lo semejante”: sustancias polares se disuelven en disolventes polares (agua), las no polares en disolventes no polares (hexano).
- Interacciones intermoleculares: la polaridad permite fuerzas como dipolo-dipolo, fuerzas de London (dispersión) y enlaces de hidrógeno (especialmente relevantes en el agua y en biopolímeros), que condicionan propiedades macroscópicas.
Representaciones y reglas
Para describir y predecir la estructura de moléculas covalentes se usan:
- Fórmulas de Lewis: muestran pares de electrones y enlaces entre átomos, útiles para la regla del octeto y para identificar pares solitarios.
- Modelos de enlace: el modelo de solapamiento de orbitales atómicos y la teoría de orbitales moleculares (OM) proporcionan una descripción cuántica más precisa: aparecen orbitales enlazantes y antienlazantes y conceptos como orden de enlace y delocalización electrónica.
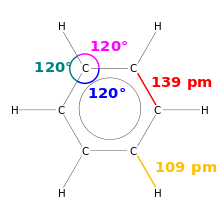
- Resonancia: en estructuras donde los electrones pueden localizarse en diferentes posiciones equivalentes, la molécula se describe como una mezcla (resonancia) que explica estabilidad y propiedades intermedias (por ejemplo, el ion nitrato NO3− o el benceno).
Ejemplos comunes
- Agua (H2O): formada por un átomo de oxígeno y dos átomos de hidrógeno. El oxígeno es más electronegativo, por lo que la densidad electrónica se desplaza hacia él y adquiere una ligera carga negativa (δ−), mientras que los hidrógenos quedan con carga parcial positiva (δ+). Por su geometría angular, la molécula es polar y puede formar enlaces de hidrógeno.
- Hidrógeno (H2): enlace covalente simple entre dos átomos idénticos, no polar.
- Oxígeno (O2): enlace doble entre dos átomos de oxígeno; es apolar.
- Nitrógeno (N2): enlace triple muy fuerte; gas diatómico con alta energía de enlace.
- Dióxido de carbono (CO2): molécula lineal con enlaces dobles C=O; a pesar de que los enlaces son polares, la geometría hace que la molécula global sea apolar.
- Metano (CH4): enlace covalente entre carbono e hidrógeno; geometría tetraédrica y molécula apolar en conjunto.
Distinción importante: moléculas covalentes vs sólidos covalentes
Hay que distinguir entre moléculas discretas unidas por enlaces covalentes (por ejemplo H2O, CO2) y sólidos en los que todos los átomos están conectados por enlaces covalentes formando una red extensa (redes covalentes). Las redes covalentes (diamante, carburo de silicio, cuarzo) presentan propiedades mecánicas y térmicas muy diferentes a las sustancias moleculares por la continuidad de los enlaces.
Resumen
El enlace covalente es un mecanismo fundamental mediante el cual los átomos comparten electrones para alcanzar una configuración electrónica más estable. Su naturaleza (simple, doble, triple, polar o no polar), su fuerza y su distribución electrónica determinan gran parte de las propiedades físicas y químicas de las sustancias. Modelos como las fórmulas de Lewis, el solapamiento de orbitales y la teoría de orbitales moleculares ayudan a describir y predecir su comportamiento.