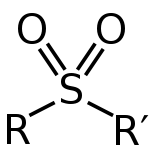
Una sulfona es una molécula que tiene un átomo de azufre con enlaces a dos átomos de oxígeno. El azufre tiene dos enlaces dobles con los dos oxígenos. Tiene un enlace simple con los otros dos grupos. Suelen fabricarse mediante la oxidación de los tioéteres.
Se utilizan en muchas reacciones químicas importantes. Por ejemplo, la olefinación Julia utiliza una sulfona para obtener un alqueno a partir de un aldehído. También se utilizan a veces como disolventes.
Estructura y propiedades generales
Las sulfona típicas tienen la fórmula general R–S(=O)2–R', donde R y R' pueden ser grupos alquilo, arilo u otros sustituyentes orgánicos. La geometría alrededor del átomo de azufre es aproximadamente tetraédrica; las descripciones de resonancia muestran contribuciones con enlaces S=O y también estructuras con carga parcial positiva en el azufre y negativa en los oxígenos (S(+)=O(−)). Esto explica la alta polaridad de la función sulfonilo y la fuerte capacidad de los oxígenos para aceptar enlaces de hidrógeno y coordinar metales.
Propiedades físicas: las sulfona suelen ser moléculas polares, con puntos de ebullición y de fusión elevados frente a compuestos no polares de masa similar. Ejemplos comunes: el dimetilsulfóxido oxidado (dimetilsulfona, MSM) es un material cristalino de punto de fusión relativamente alto; el sulfolano (una sulfona cíclica) es un disolvente polar de alto punto de ebullición muy usado industrialmente.
Obtención y métodos sintéticos
- Oxidación de tioéteres (tioéter → sulfoxido → sulfona): oxidantes habituales son el peróxido de hidrógeno, oxone, mCPBA (meta-cloroperbenzoico) y otros perácidos. La oxidación puede controlarse para obtener primero sulfoxidos y, con exceso de oxidante, sulfona.
- Reacciones con cloruros de sulfónico (sulfonilación): la unión de grupos sulfonilo a un sistema orgánico a través de reactivos como R–SO2Cl seguida de sustitución nucleofílica permite preparar sulfona sustituidas o sulfonatos que pueden convertirse en sulfona por posteriores transformaciones.
- Alquilación de sulfinatos: sales sulfinato (p. ej., R–SO2– Na+) pueden alkilarse con haluros de alquilo para formar sulfona.
- Rutas más especiales: acoplamientos con organometálicos sobre derivados sulfonilo o transformaciones específicas como la adición-eliminación en síntesis de sulfona funcionalizadas.
Reactividad y usos en síntesis orgánica
Las sulfona son grupos funcionales muy útiles en síntesis por varias razones:
- Acidez de los hidrógenos α: los hidrógenos situados en carbono adyacente al grupo –SO2– son notablemente acidificables. La desprotonación con bases fuertes genera carbaniones estabilizados por el efecto estabilizante del grupo sulfonilo; esos carbaniones se emplean en alkilaciones, condensaciones y en la construcción de cadenas carbonadas.
- Olefinación Julia (y variantes): la condensación de una anión sulfona con un aldehído o una cetona seguida de pasos de eliminación conduce a alquenos con buena control sobre la estereoquímica (Julia–Kocienski, Julia–Lythgoe, etc.).
- Ramberg–Bäcklund: las α-halo-sulfonas pueden sufrir eliminación intramolecular para dar alquenos mediante una secuencia de deshalogenación y pérdida de SO2.
- Grupo saliente y transformaciones de desulfuración: bajo condiciones reductoras (p. ej., Raney-Ni), el grupo –SO2– puede eliminarse para obtener hidrocarburos (usado como estrategia de protección/activación o para introducir equivalentes sintéticos temporales).
- Activación y dirección: por su carácter electronegativo, las sulfona modifican la reactividad de anillos aromáticos, estabilizan carbaniones intermedios y se emplean como grupos directores en síntesis selectiva.
Ejemplos y aplicaciones prácticas
- Dimetilsulfona (MSM): se usa como disolvente y aditivo en aplicaciones industriales y como suplemento dietético en algunos contextos.
- Sulfolano (tetrahidrotiopeno‑dióxido): disolvente polar, estable a temperaturas elevadas, usado en procesos de extracción y síntesis.
- Dapsone (diaminodifenilsulfona): ejemplo de sulfona con actividad farmacológica, utilizada como antibacteriano y antiinflamatorio en enfermedades como la lepra y dermatitis herpetiforme.
- Sulfona en química de polímeros: los enlaces sulfonilo (–SO2–) aparecen en polímeros de ingeniería conocidos como polisulfonas, apreciados por su estabilidad térmica y resistencia química.
Seguridad y medio ambiente
El perfil toxicológico varía según la sulfona concreta. Algunas son relativamente inocuas, mientras que otras (p. ej., fármacos como dapsona) requieren vigilancia por efectos adversos (hemolisis, metahemoglobinemia, reacciones cutáneas). Los disolventes sulfonados industriales deben manipularse con guantes y ventilación adecuada; en procesos industriales se controlan emisiones y efluentes para evitar contaminación.
Resumen
Las sulfona son compuestos versátiles y estables que combinan una fuerte polaridad con capacidad para estabilizar cargas y carbaniones. Se sintetizan con facilidad a partir de tioéteres y a través de otras rutas, y su reactividad las hace indispensables en métodos sintéticos como la olefinación Julia, la Ramberg–Bäcklund y en múltiples transformaciones de construcción de C–C. Además, aparecen en aplicaciones industriales (disolventes, polímeros) y farmacéuticas (p. ej., dapsone).