Una reacción química se produce cuando una o varias sustancias químicas se transforman en otra u otras. Ejemplos:
- el hierro y el oxígeno se combinan para formar el óxido
- el vinagre y el bicarbonato de sodio se combinan para formar acetato de sodio, dióxido de carbono y agua
- cosas que se queman o explotan
- muchas reacciones que ocurren dentro de los seres vivos
- reacciones electroquímicas al descargar o recargar las baterías
Algunas reacciones son rápidas y otras son lentas. Algunas ocurren a diferentes velocidades, dependiendo de la temperatura o de otras cosas. Por ejemplo, la madera no reacciona con el aire cuando está fría, pero si se calienta lo suficiente, empieza a arder. Algunas reacciones desprenden energía. Son reacciones exotérmicas. En otras reacciones se absorbe energía. Son reacciones endotérmicas.
Las reacciones nucleares no son reacciones químicas. En las reacciones químicas sólo intervienen los electrones de los átomos; en las reacciones nucleares intervienen los protones y los neutrones de los núcleos atómicos.
Tipos principales de reacciones químicas
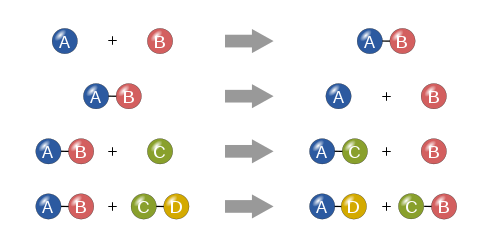
- Reacciones de síntesis (combinación): dos o más sustancias se unen para formar un único producto. Ejemplo común: formación de óxido a partir de hierro y oxígeno.
- Reacciones de descomposición: una sustancia se divide en dos o más productos más simples. Suele requerir energía (calor, luz o corriente eléctrica).
- Reacciones de desplazamiento simple: un elemento sustituye a otro en un compuesto.
- Reacciones de doble desplazamiento: dos compuestos intercambian iones entre sí, formando nuevos compuestos y, a veces, precipitados o gases.
- Combustión: reacción rápida entre una sustancia y un oxidante (a menudo el oxígeno) que libera energía (luz y calor). La madera que arde en presencia de aire es un ejemplo.
- Reacciones ácido–base (neutralización): ácido y base reaccionan para formar una sal y agua; el ejemplo clásico de vinagre con bicarbonato de sodio produce acetato de sodio, dióxido de carbono y agua.
- Reacciones redox (oxidación-reducción): implican transferencia de electrones entre especies; muchas reacciones de corrosión, combustión y la mayoría de las reacciones en baterías pertenecen a esta categoría. Las reacciones electroquímicas que ocurren al cargar y descargar las baterías son ejemplos aplicados.
Velocidad de reacción y factores que la afectan
La velocidad con la que ocurre una reacción química depende de varios factores:
- Concentración de los reactivos: mayor concentración suele aumentar la frecuencia de colisiones entre partículas y acelerar la reacción.
- Temperatura: un aumento de la temperatura incrementa la energía cinética de las partículas y suele acelerar las reacciones.
- Superficie de contacto: en sólidos, partículas más pequeñas o mayor superficie de contacto favorecen reacciones más rápidas.
- Presencia de catalizadores: los catalizadores aceleran las reacciones disminuyendo la energía de activación, sin consumirse en el proceso.
- Presión: para reacciones que involucran gases, aumentar la presión puede aumentar la velocidad al elevar la concentración efectiva.
Energía en las reacciones
Cada reacción tiene asociada una transferencia de energía. Las reacciones exotérmicas liberan energía al entorno (ej.: combustión), mientras que las reacciones endotérmicas absorben energía (ej.: la descomposición térmica de algunos compuestos). Además de la energía neta intercambiada, muchas reacciones requieren una energía de activación inicial para que las moléculas reaccionen; los catalizadores reducen esa barrera.
Reacciones reversibles y equilibrio químico
No todas las reacciones van hasta completarse en una sola dirección. Muchas son reversibles: los productos pueden reaccionar entre sí para regenerar los reactivos. Cuando las velocidades directa e inversa se igualan, el sistema alcanza un equilibrio químico. En el equilibrio no necesariamente hay cantidades iguales de reactivos y productos, sino que las concentraciones permanecen constantes en el tiempo.
Representación y balance de reacciones
Las reacciones se representan mediante ecuaciones químicas, donde se escriben los reactivos a la izquierda y los productos a la derecha, separados por una flecha. Según la ley de conservación de la masa, el número de átomos de cada elemento debe ser el mismo en ambos lados: por eso las ecuaciones se balancean ajustando coeficientes estequiométricos. El balance permite además calcular cantidades (masa, moles) necesarias o producidas en una reacción (estequiometría).
Importancia y aplicaciones
Las reacciones químicas son fundamentales en la vida diaria y la industria: desde la digestión y el metabolismo en los seres vivos, la producción de materiales (plásticos, medicamentos, fertilizantes), el funcionamiento de las baterías, hasta procesos ambientales como la formación de óxidos y la depuración de aguas.
Seguridad y consideraciones prácticas
Algunas reacciones son peligrosas: pueden liberar gases tóxicos, calor intenso, o ser explosivas. Es importante manejar reactivos con las precauciones adecuadas (protección personal, ventilación, control de fuentes de ignición) y conocer las propiedades de los productos y reactivos involucrados.
En resumen, una reacción química implica la reorganización de los electrones alrededor de los átomos para formar nuevas sustancias (a diferencia de las reacciones nucleares, que afectan al núcleo). Comprender los tipos, la energía, la velocidad y la representación de las reacciones permite predecir y controlar procesos químicos en la ciencia, la tecnología y la vida cotidiana.