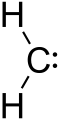Un carbeno es una molécula con un átomo de carbono que tiene dos enlaces y otros dos electrones que no hacen ningún enlace. Como el carbono sólo tiene 6 electrones a su alrededor, es bastante reactivo. La fórmula general puede escribirse como R-(C:)-R'.
Un carbeno puede ser un singlete o un triplete. En el primer tipo, los dos electrones que no forman enlaces son como un par solitario. Ambos permanecen en el mismo orbital. En cambio, en un carbeno triplete, los dos electrones permanecen en orbitales diferentes. En este caso, ambos tienen el mismo espín.
Los carbenos pueden realizar muchas reacciones. Pueden ser tanto electrófilos como nucleófilos. Les gusta hacer reacciones de adición sobre dobles enlaces. También se encuentran en reacciones quelotrópicas.
La mayoría de los carbenos son muy inestables. Sin embargo, algunos pueden existir durante mucho tiempo. Un ejemplo famoso es el catalizador de Grubbs, desarrollado por Robert Grubbs.
Estructura electrónica y geometría
Desde el punto de vista electrónico, un carbeno es un carbono divalente con cuatro electrones en los orbitales no enlazantes. En el singlete los dos electrones están apareados en un mismo orbital (habitualmente un orbital híbrido tipo sp2), y queda un orbital p vacío perpendicular al plano de los sustituyentes. Esta disposición suele dar una geometría doblemente doblada (bent), con ángulos alrededor de 100–120° en torno al carbono divalente. Por eso los carbenos singlete tienden a ser electròfilos (tienen un orbital vacío).
En el triplete, los dos electrones están no apareados en orbitales ortogonales (uno en un orbital híbrido y otro en un orbital p), por lo que el carbeno se comporta como un dirradical. Su geometría suele ser más cercana a lineal que la del singlete, y su química se aproxima a reacciones paso a paso de tipo radical.
Tipos y factores que determinan singlete vs triplete
El estado preferido (singlete o triplete) depende de varios factores:
- Sustituyentes electrónicos: Sustituyentes que donan electrones por efecto inductivo o por resonancia (ej. grupos arilo con capacidad donadora, sustituyentes heteroatómicos como N) estabilizan el singlete al estabilizar el par solitario y el orbital vacío.
- Sustituyentes que estabilizan radicales: Grupos que estabilizan radicales (por ejemplo sustituyentes alquilo que estabilizan por hiperconjugación) tienden a favorecer el estado triplete.
- Efectos estéricos: Pueden influir en la geometría y así en la energía relativa de los estados.
Formación y ejemplos comunes
Los carbenos pueden generarse por varios métodos experimentales:
- Descomposición térmica o fotoinducida de compuestos diazo (expulsión de N2) — uno de los métodos más utilizados para obtener carbenos libres o carbenos transferibles mediante catalizadores metálicos.
- Eliminación α de haluros (por ejemplo, tratamiento de haloformos con bases fuertes) para formar carbenos halogenados como el dicloro-carbino (:CCl2).
- Reacciones catalizadas por metales (Rh, Cu, Ru) en las que se forma primero un carbeno metálico que puede transferir el fragmento carbénico a un sustrato.
- Métodos especializados como la reacción de Simmons–Smith (formación de un “carbenoide” de metileno que ciclopropaniza alquenos) o fotólisis de cetenas.
Ejemplos sencillos: :CH2 (metileno), :CCl2 (dicloro-carbino), y carbenos estabilizados como los N-heterocyclic carbenes (NHC), por ejemplo el carbeno de Arduengo, que son singletes persistentes y ampliamente usados como ligandos y catalizadores.
Reactividad característica
Los carbenos participan en numerosas transformaciones importantes en síntesis orgánica:
- Ciclopropanación: Adición a dobles enlaces para formar ciclopropanos (reacción concertada para singletes; paso radicalario para tripletes).
- Inserción en enlaces X–H: Inserción en enlaces C–H, O–H o N–H, útil para funcionalizar moléculas.
- Formación de ylidos: Reacción con compuestos como fosfinas para dar ylidos, que pueden ser intermediarios en otras transformaciones.
- Reacciones radicalarias: Los carbenos triplete suelen reaccionar por rutas paso a paso similares a los radicales.
- Transferencia desde carbenos metálicos: Muchos procesos catalíticos usan carbenos unidos a metales (p. ej. carbeno de Rh, Cu) para lograr inserciones o ciclopropanaciones con alta selectividad.
Carbenos libres vs carbenos metálicos
Es importante distinguir entre carbenos libres (especies de carbono divalente en solución sin enlace fuerte a un metal) y carbenos unidos a metales. Los últimos (metal-carbenos) son intermediarios clave en reacciones como la metátesis de olefinas y las inserciones metal-catalizadas. Dentro de los metal-carbenos, se clasifica a veces entre:
- Carbenos tipo Fischer: metales en estados bajos de oxidación con sustituyentes aceptores; tienden a ser electrofílicos.
- Carbenos tipo Schrock: metales en estados altos de oxidación, más nucleofílicos y con carácter aniónico.
El catalizador de Grubbs contiene un grupo alkilideno (carbeno ligado a Ru) esencial para la metátesis de olefinas; no se trata de un carbeno libre, sino de un complejo metal-carbeno estable y catalíticamente activo.
Estabilización y carbenos persistentes
Aunque la mayoría de los carbenos libres son muy reactivos y de vida corta, existen carbenos persistentes estabilizados por efectos electrónicos y estéricos. Entre los más conocidos están los N-heterocyclic carbenes (NHCs), que deben su estabilidad a la donación electrónica de los átomos de nitrógeno y a la protección estérica de los sustituyentes. Estos carbenos persistentes se utilizan como ligandos en catálisis homogénea y como bases/donadores de electrones en síntesis.
Detección y estudio
Los carbenos transientes se detectan y caracterizan mediante técnicas como espectroscopía de EPR (específicamente útil para carbenos triplete), espectroscopía ultrarrápida (flash photolysis), estudios espectroscópicos ópticos y mediante reacciones de captura con donantes o alquenos que “atrapan” el carbene formando productos característicos.
Resumen práctico
- Un carbeno es un carbono divalente con un par de electrones no enlazantes; puede existir como singlete (par apareado) o triplete (dos electrones no apareados).
- Su reactividad incluye ciclopropanación, inserciones y formación de ylidos; el comportamiento depende del estado electrónico (singlete → más concertado/electrofílico; triplete → radicalario).
- Se generan por descomposición de diazo, eliminación α, fotólisis o mediante carbenos metálicos; la estabilización puede lograrse con heteroátomos o sustituyentes voluminosos (NHCs, carbenos arílicos, silyl-carbenos).
- Los carbenos ligados a metales (ej. en el catalizador de Grubbs) son fundamentales en catálisis moderna, especialmente en metátesis de olefinas.
Si desea, puedo añadir esquemas electrónicos sencillos (representaciones orbitales) o incluir ejemplos experimentales típicos (procedimientos para generar dicloro-carbino o para usar diazo-compuestos con catalizadores de Rh) en lenguaje accesible.