Los orbitales atómicos son los lugares que rodean el núcleo de un átomo donde es más probable que estén los electrones en un momento dado. Es una función matemática que describe el comportamiento ondulatorio de un electrón o de un par de electrones en un átomo.
La palabra "orbital" se utiliza porque se pensaba que los electrones se comportaban de forma similar al sistema solar, donde el núcleo es como el sol y los electrones orbitan como los planetas.
El número de orbitales atómicos de un elemento está definido por el período en el que se encuentra el elemento. Los electrones se mueven entre los orbitales dependiendo de la velocidad a la que se mueven y de cuántos otros electrones hay.
En la teoría atómica y la mecánica cuántica, un orbital atómico es un número cuántico. Cada orbital puede estar ocupado por uno o dos electrones. La disposición de los orbitales está relacionada con las configuraciones electrónicas de los átomos. Se derivaron de las descripciones proporcionadas por los primeros espectroscopistas de ciertas líneas espectroscópicas de los metales alcalinos como agudas, principales, difusas y fundamentales.
Definición y concepto físico
Un orbital atómico es, en términos prácticos, una región del espacio donde la probabilidad de encontrar un electrón es alta. Matemáticamente se representa por una función de onda (ψ) que surge de resolver la ecuación de Schrödinger para el átomo. El cuadrado de la función de onda (|ψ|²) da la densidad de probabilidad electrónica.
Números cuánticos
Los orbitales se caracterizan por cuatro números cuánticos:
- n (número cuántico principal): indica el tamaño y la energía aproximada del orbital (n = 1, 2, 3…).
- l (número cuántico azimutal o del momento angular): define la forma del orbital y toma valores 0 ≤ l ≤ n−1. Cada valor de l corresponde a una letra: l = 0 (s), 1 (p), 2 (d), 3 (f).
- m_l (número cuántico magnético): indica la orientación espacial del orbital; toma 2l+1 valores enteros entre −l y +l.
- m_s (número cuántico de espín): describe el espín del electrón; puede ser +1/2 o −1/2.
Tipos de orbitales y formas
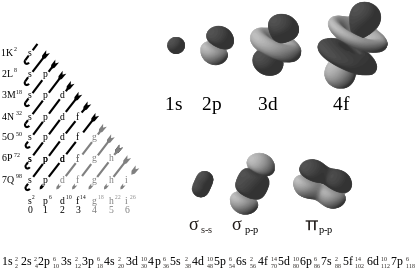
- Orbitales s (l = 0): simétricos y esféricos. Cada nivel n tiene un orbital s.
- Orbitales p (l = 1): forma de mancuerna (dos lóbulos) con tres orientaciones (p_x, p_y, p_z).
- Orbitales d (l = 2): formas más complejas (cuatro lóbulos tipo trébol y un caso con un toro alrededor), con cinco orientaciones.
- Orbitales f (l = 3): aún más complejos; siete orientaciones, relevantes en lantánidos y actínidos.
Cada subshell tiene un número fijo de orbitales: s = 1 orbital, p = 3, d = 5, f = 7. El número total de orbitales en la capa n es n², y la capacidad máxima de electrones por capa es 2n².
Configuración electrónica y reglas de llenado
La distribución de electrones entre orbitales determina la configuración electrónica de un átomo y explica sus propiedades químicas. Las reglas principales para rellenar orbitales son:
- Principio de Aufbau: los electrones ocupan primero los orbitales de menor energía (orden aproximado: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s...).)
- Principio de exclusión de Pauli: cada orbital puede contener como máximo dos electrones con espines opuestos.
- Regla de Hund: al llenar una subshell degenerada, se colocan primero electrones con espines paralelos en orbitales vacíos antes de aparearlos.
Ejemplo práctico: el oxígeno (Z = 8) tiene configuración 1s2 2s2 2p4. En la subshell 2p habrá dos orbitales con un electrón y uno con dos, según la regla de Hund.
Excepciones conocidas: algunos elementos (p. ej. Cr y Cu) muestran configuraciones atípicas como resultado de la estabilidad relativa de configuraciones d medio llenas o completamente llenas (por ejemplo, Cr: [Ar] 4s1 3d5; Cu: [Ar] 4s1 3d10).
Nodos y características de las funciones de onda
Los orbitales presentan nodos, regiones donde la probabilidad de encontrar el electrón es cero. Hay dos tipos:
- Nodos radiales: su número es n − l − 1.
- Nodos angulares: su número es igual a l; determinan la forma angular del orbital.
Energia, degeneración y efectos de muchos electrones
En el átomo de hidrógeno los orbitales con igual n tienen la misma energía (degeneración). En átomos multielectrónicos, la interacción electrón-electrón provoca desdoblamiento energético: la energía depende tanto de n como de l. Conceptos como penetración y apantallamiento explican por qué, por ejemplo, 4s suele estar por debajo energéticamente que 3d en el llenado inicial, aunque en estados ionizados las energías relativas cambien.
Relación con la tabla periódica y la espectroscopía
La estructura de la tabla periódica refleja el llenado de orbitales: los bloques s, p, d y f corresponden a los tipos de orbitales que están siendo ocupados. La observación experimental de los espectros atómicos (líneas de emisión y absorción) proporcionó las primeras evidencias de niveles discretos de energía y motivó la clasificación histórica de líneas como agudas, principales, difusas y fundamentales, de las que derivaron las letras s, p, d y f.
Visualización y aplicaciones
Hoy se visualizan orbitales mediante cálculos y representaciones de densidad electrónica (superficies de contorno donde |ψ|² es constante). Comprender orbitales y configuraciones es fundamental en química para:
- Predecir enlaces y geometrías moleculares.
- Entender reactividad y propiedades magnéticas.
- Interpretar espectros de absorción/emisión y propiedades electrónicas de materiales.
En resumen, los orbitales atómicos son herramientas conceptuales y matemáticas clave que permiten describir y predecir la distribución electrónica y el comportamiento químico de los átomos. Su estudio conecta la teoría cuántica con observaciones experimentales como la espectroscopía y la estructura periódica.