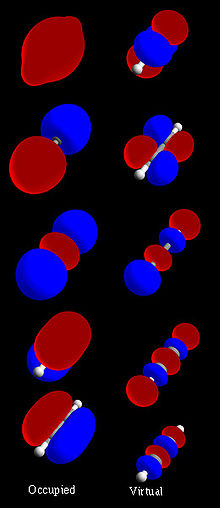
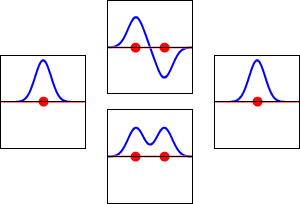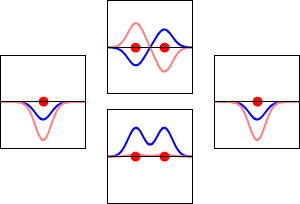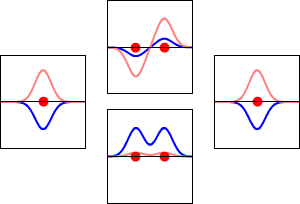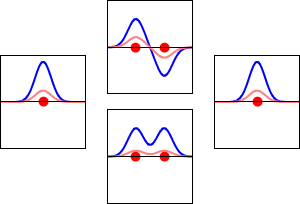
En química, un orbital molecular (o MO) explica lo que ocurre con los electrones cuando los átomos se unen en una molécula. Un MO es una función matemática que describe el comportamiento ondulatorio de un electrón en una molécula. Las funciones pueden indicar la probabilidad de encontrar un electrón en una región específica. Los químicos utilizan estas funciones para predecir o explicar las propiedades químicas y físicas.
Los químicos suelen construir modelos matemáticos de orbitales moleculares combinando orbitales atómicos. También se pueden utilizar orbitales híbridos de cada átomo de la molécula u otros orbitales moleculares de grupos de átomos. Los ordenadores pueden trabajar con estas funciones. Los orbitales moleculares permiten a los químicos aplicar la mecánica cuántica al estudio de las moléculas. Los orbitales moleculares responden a preguntas sobre cómo se unen los átomos en las moléculas. Las distintas formas redondeadas de un diagrama de orbitales indican dónde es más probable que se encuentren los electrones en un átomo.
¿Qué es un orbital molecular en términos sencillos?
Un orbital molecular es una región del espacio en una molécula donde la probabilidad de encontrar un electrón es alta. Matemáticamente se representa por una función de onda. Estas funciones pueden tener distintas formas y signos (fases) y se obtienen combinando orbitales atómicos mediante métodos como la aproximación de la combinación lineal de orbitales atómicos (LCAO). La forma y la energía de un MO determinan cómo participan los electrones en el enlace, en la reactividad y en las propiedades ópticas y magnéticas de la molécula.
Tipos principales de orbitales moleculares
- Orbitales enlazantes (bonding): resultan de la suma constructiva de orbitales atómicos; aumentan la densidad electrónica entre núcleos y estabilizan la molécula.
- Orbitales antienlazantes (antibonding): aparecen por suma destructiva; tienen nodos entre núcleos y desestabilizan si se ocupan con electrones (se representan con un asterisco, p. ej. σ* o π*).
- Orbitales no enlazantes (nonbonding): corresponden a electrones que no contribuyen apreciablemente al enlace (p. ej. pares solitarios).
- Sigma (σ) y pi (π): clasificación según la simetría alrededor del eje internuclear; σ se comparte a lo largo del eje, π tiene densidad por encima y por debajo del eje.
- Orbitales degenerados y delocalizados: en sistemas conjugados o aromáticos (como el benceno) los MOs pueden extenderse sobre varios átomos, dando lugar a propiedades particulares como la aromaticidad.
- HOMO y LUMO: el orbital ocupacional de mayor energía (HOMO) y el orbital virtual de menor energía (LUMO) son claves para entender reactividad y transiciones electrónicas.
Cómo se construyen: LCAO, solapamiento y simetría
La construcción básica de MOs considera combinaciones lineales de orbitales atómicos. Dos factores importantes son:
- Solapamiento: cuanto mayor sea el solapamiento entre orbitales atómicos, mayor será la estabilización del MO enlazante.
- Simetría: solo orbitales atómicos con la misma simetría pueden combinarse eficazmente.
Las combinaciones constructivas producen orbitales enlazantes sin nodos entre núcleos; las destructivas originan orbitales antienlazantes con nodos. Además, la energía relativa de los orbitales atómicos (por ejemplo 2s vs 2p) influye en la energía de los MOs resultantes.
Reglas de llenado y diagramas de orbitales
- Los MOs se llenan con electrones siguiendo el principio de Aufbau (de menor a mayor energía), el principio de exclusión de Pauli (máximo dos electrones por orbital con espines opuestos) y la regla de Hund (ocupación máxima de orbitales degenerados con espines paralelos antes de aparearlos).
- Los diagramas de orbitales moleculares muestran las energías relativas de MOs enlazantes, no enlazantes y antienlazantes. Son herramientas útiles para predecir propiedades como la longitud de enlace, la energía de enlace y el magnetismo (p. ej. la paramagnetismo del O2 se explica por electrones en orbitales π*).
Papel en la química cuántica y aplicaciones prácticas
Los orbitales moleculares son la forma práctica de aplicar la mecánica cuántica a la química. Permiten:
- Explicar la estabilidad y la longitud de enlace en moléculas.
- Predecir la reactividad mediante análisis de HOMO/LUMO (quién dona y quién acepta electrones).
- Interpretar espectros electrónicos y de absorción (transiciones entre MOs) y espectros de fotoelectrones.
- Comprender propiedades magnéticas (diamagnetismo vs paramagnetismo) y conductividad en materiales.
- Analizar fenómenos de delocalización y aromaticidad en sistemas conjugados.
Métodos computacionales y visualización
La obtención práctica de MOs se hace con programas de química computacional que resuelven la ecuación de Schrödinger aproximada. Entre los métodos más comunes están Hartree–Fock (HF), la teoría del funcional de la densidad (DFT) y técnicas post-HF (CI, MP2, CC). Estos programas generan las funciones de onda y permiten visualizar las densidades electrónicas y fases de los MOs (mediante isosurfaces), facilitando la interpretación.
Ejemplos breves
- H2: la combinación de dos orbitales 1s produce un orbital σ (enlazante) y un σ* (antienlazante); H2 es estable porque los dos electrones ocupan el σ enlazante.
- O2: su diagrama MO muestra dos electrones no apareados en orbitales π*, lo que explica su carácter paramagnético.
- Benceno: los 6 electrones π se delocalizan en MOs extendidos sobre el anillo, dando lugar a la estabilidad aromática.
Conceptos prácticos a recordar
- Los MOs describen probabilidades, no trayectorias de electrones.
- La ocupación de orbitales antienlazantes reduce la estabilidad; la ocupación de enlazantes la aumenta.
- HOMO y LUMO son útiles para prever reactividad y color (transiciones electrónicas).
En resumen, los orbitales moleculares son herramientas fundamentales que conectan la teoría cuántica con observables químicos y físicos. Gracias a ellos, la química cuantitativa puede explicar y predecir enlaces, reactividad, propiedades ópticas y magnéticas, y el comportamiento de sistemas desde moléculas sencillas hasta materiales complejos.