En química y física, la teoría atómica explica cómo ha cambiado nuestra comprensión del átomo a lo largo del tiempo. Antes se pensaba que los átomos eran las piezas más pequeñas de la materia. Sin embargo, ahora se sabe que los átomos están formados por protones, neutrones y electrones. Estas partículas subatómicas están formadas por quarks. La primera idea del átomo procede del filósofo griego Demócrito. Muchas de las ideas de la teoría moderna proceden de John Dalton, químico y físico británico.
La teoría se aplica a los sólidos, líquidos y gases, pero no se aplica de forma análoga a los plasmas o a las estrellas de neutrones.
Qué es el átomo hoy
Un átomo es la unidad básica de un elemento químico y está formado por un núcleo compacto (conteniendo protones y neutrones) rodeado por una nube de electrones. El número de protones (número atómico, Z) define el elemento, mientras que la suma de protones y neutrones (número de masa, A) determina la mayor parte de su masa. Los electrones ocupan niveles de energía y regiones de probabilidad (orbitales) descritos por la mecánica cuántica, no por órbitas circulares clásicas.
Historia breve y modelos atómicos
- Antigüedad: Filósofos como Demócrito propusieron la idea de partículas indivisibles ("átomos").
- Dalton (principios del s. XIX): Propuso que los elementos están formados por átomos indivisibles con masas características, explicando las proporciones en las reacciones químicas.
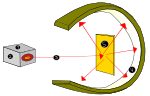
- Thomson (1897): Descubrió el electrón mediante experimentos con rayos catódicos y propuso el modelo del "pudín" con cargas positivas y electrones incrustados.
- Rutherford (1911): Experimentos de dispersión con lámina de oro mostraron que la carga positiva y casi toda la masa están concentradas en un núcleo pequeño y denso.
- Bohr (1913): Introdujo niveles discretos de energía para los electrones y explicó parte del espectro atómico del hidrógeno.
- Mecánica cuántica (años 1920): Contribuciones de Schrödinger, Heisenberg y otros reemplazaron órbitas por funciones de onda y principios de incertidumbre, dando el modelo atómico moderno.
- Descubrimiento del neutrón (Chadwick, 1932): Explicó la existencia de isótopos y completó la comprensión del núcleo.
- Teoría de quarks y cromodinámica cuántica (s. XX): Mostró que protones y neutrones están compuestos por quarks unidos por gluones.
Partículas subatómicas y estructura más profunda
Las principales partículas en un átomo son:
- Protones: Partículas con carga positiva (≈ +1 e) situadas en el núcleo. Están formados por quarks (dos quarks "up" y un quark "down").
- Neutrones: Partículas sin carga eléctrica neta en el núcleo. Están formados por un quark "up" y dos quarks "down".
- Electrones: Partículas con carga negativa (≈ −1 e) que pertenecen a la familia de los leptones; no están formadas por quarks según el conocimiento actual.
Los quarks tienen cargas fraccionarias (+2/3 o −1/3) y se mantienen unidos por los gluones mediante la fuerza fuerte, descrita por la cromodinámica cuántica (QCD). Además existen otras partículas relevantes en física de altas energías (mesones, bariones, etc.) que aparecen en choques y decaimientos, y que ayudan a estudiar la estructura interna de la materia.
Fenómenos derivados: isótopos, iones y enlaces
Los átomos de un mismo elemento pueden tener distinto número de neutrones: son isótopos. Algunos isótopos son estables y otros radiactivos. Cuando un átomo gana o pierde electrones se convierte en ion (carga neta distinta de cero). Las interacciones entre electrones y núcleos explican la formación de enlaces químicos (iónicos, covalentes, metálicos) y las propiedades macroscópicas de materiales y sustancias.
Métodos experimentales que sustentan la teoría
- Espectroscopía: las líneas espectrales muestran niveles de energía discretos.
- Experimentos de dispersión y aceleradores de partículas: permiten "ver" la estructura interna del núcleo y descubrir partículas elementales.
- Producción y detección de partículas en cámaras de niebla y detectores modernos: confirman la existencia de electrones, protones, neutrones, quarks y otras partículas.
Aplicaciones y límites de la teoría atómica
La teoría atómica es la base de la química, la física de materiales, la electrónica, la energía nuclear, la medicina nuclear y muchas tecnologías modernas. Sin embargo, sus aplicaciones tienen límites prácticos y conceptuales:
- Plasmas: En un plasma la mayor parte de los átomos está ionizada; las interacciones colectivas electromagnéticas dominan el comportamiento y se requiere la física del plasma para describirlo. Aunque la idea de átomos sigue siendo útil a nivel de partículas individuales, la descripción macroscópica es distinta.
- Estrellas de neutrones: En condiciones extremas de densidad y presión, la materia deja de estar organizada en átomos; los electrones y protones pueden combinarse en neutrones y formarse materia degenerada o incluso fases exóticas (materia de quarks). Por eso la teoría atómica tal como se usa en química no es adecuada para describir esos objetos.
Resumen
La teoría atómica ha evolucionado desde la noción filosófica de átomos indivisibles hasta un modelo complejo basado en mecánica cuántica y cromodinámica cuántica. Explica la estructura y comportamiento de la materia en condiciones ordinarias y, con extensiones (física nuclear, física de partículas, física del plasma), también sirve para entender fenómenos más extremos, aunque con limitaciones cuando las condiciones superan las de los átomos aislados.