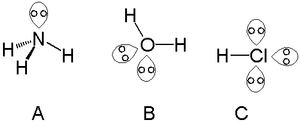
Un par solitario es un grupo de dos electrones que no se utilizan en ningún enlace entre átomos. Siempre se encuentran en la última capa del átomo, la capa de valencia. Junto con los electrones utilizados en los enlaces, constituyen el número total de electrones de valencia. Suelen tener una energía elevada.
Un par solitario puede utilizarse para formar nuevos enlaces entre moléculas. Los nucleófilos siempre tienen un par solitario que se utiliza para atacar a un electrófilo. Los pares solitarios también son importantes para la forma de una molécula. Ocupan más espacio alrededor de un átomo que un electrón enlazante. Los pares solitarios de un mismo átomo quieren estar lo más lejos posible unos de otros.
Representación y carga formal
En estructuras de Lewis los pares solitarios se representan normalmente como dos puntos “:” junto al símbolo del átomo o con líneas en modelos más detallados. Su presencia influye en la carga formal de un átomo: al contar electrones no compartidos se determina si un átomo tiene carga parcial o completa. Los pares solitarios también pueden participar en la formación de enlaces coordinados (enlace dativo), donde ambos electrones del enlace proceden del mismo átomo.
Influencia en la geometría molecular (teoría VSEPR)
Según la teoría de la repulsión de los pares de electrones de la capa de valencia (VSEPR), los pares solitarios ocupan más espacio que los pares compartidos porque su densidad electrónica está más localizada sobre el átomo. Esto provoca ajustes en los ángulos de enlace:
- Moléculas con un par solitario (ej. NH3) tienen ángulos ligeramente menores que el tetraédrico ideal (NH3 ≈ 107° frente a 109,5°).
- Moléculas con dos pares solitarios (ej. H2O) muestran ángulos aún más reducidos (H2O ≈ 104,5°).
- La distribución de pares solitarios entre orbitales híbridos (sp3, sp2, etc.) afecta la forma y la reactividad.
Reactividad: nucleófilos, bases de Lewis y formación de enlaces
Un par solitario convierte a un átomo en un sitio potencialmente nucleófilo o base de Lewis porque puede donar ese par para formar un enlace con un centro deficiente en electrones (electrófilo o ácido de Lewis). Algunos puntos clave:
- Basicidad y nucleofilicidad: dependen de la electronegatividad del átomo que porta el par, de la solvatación, del efecto de resonancia y del impedimento estérico. Por ejemplo, NH3 es una base y nucleófilo más fuerte que H2O.
- Enlace coordinado: muchos complejos de coordinación en química inorgánica se forman cuando ligandos donan pares solitarios a metales.
- Reactividad orgánica: en grupos carbonilo, el par solitario del oxígeno puede atacar protones o estabilizar cargas; además, las transiciones fotoquímicas n→π* (par solitario a orbital antienlazante) son importantes en fotquímica.
Resonancia y pares solitarios deslocalizados
Cuando un par solitario está en conjugación con sistemas π (por ejemplo, en amidas, anilinas o en algunos aniones), puede deslocalizarse mediante resonancia. La deslocalización:
- Reduce la densidad electrónica localizada y suele disminuir la basicidad del par solitario.
- Afecta las longitudes de enlace y la estabilidad de la molécula.
Interacciones y propiedades físicas
Los pares solitarios participan en interacciones no covalentes importantes:
- Puentes de hidrógeno: los pares solitarios de átomos electronegativos (O, N, F) actúan como aceptores de puentes de hidrógeno, influyendo en puntos de ebullición, solubilidad y estructura supramolecular.
- Espectroscopía: transiciones electrónicas como n→π* son observables en UV/Vis y tienen repercusiones en la fotoreactividad; en IR, la presencia de pares solitarios altera frecuencias de vibración por acoplamiento y cambios en fuerza de enlace.
Ejemplos comunes
- H2O: cada átomo de oxígeno tiene dos pares solitarios; esto explica la forma angular y su capacidad para formar puentes de hidrógeno.
- NH3: el nitrógeno tiene un par solitario responsable de su basicidad y su capacidad para coordinar metales.
- Cl−: ión cloruro con tres pares solitarios, fuerte nucleófilo en soluciones no proticas.
- Carbonilos (C=O): el oxígeno posee pares solitarios, uno de los cuales suele participar en resonancia con el enlace C=O, afectando la reactividad (ataque nucleofílico, protonación).
Consideraciones avanzadas
En elementos pesados del bloque p aparece a veces el llamado efecto del par inerte, donde los pares solitarios se comportan de manera menos reactiva por efectos relativistas y de apantallamiento. Además, en química organometálica los pares solitarios de ligandos heteroátomos y s-electrones pueden influir en la geometría electrónica y en la catálisis.
En resumen, los pares solitarios son determinantes para la geometría molecular, la polaridad, la reactividad como nucleófilos o bases de Lewis y para múltiples interacciones físico-químicas. Reconocer su presencia y su comportamiento (localizado o deslocalizado) es esencial para predecir propiedades y mecanismos en química.