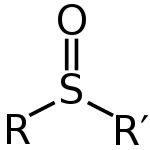
Un sulfóxido es una molécula que tiene un átomo de azufre unido a dos carbonos y un átomo de oxígeno. Procede de la oxidación de los tioéteres, sin llegar a la sulfona. Como muchas moléculas que contienen azufre, el sulfóxido puede a veces oler mucho.
Los sulfóxidos pueden escribirse con la fórmula general R-S(=O)-R'. El azufre tiene un doble enlace con el oxígeno y enlaces simples con los carbonos. Esto deja un par solitario en el átomo. Esto significa que la forma en ese átomo es tetraédrica. También significa que el azufre puede ser un centro quiral. Los sulfóxidos se utilizan como buenos ligandos para los metales de transición.
Una molécula importante de este tipo es el dimetilsulfóxido. También se denomina DMSO. Se utiliza como disolvente en muchas reacciones, especialmente en bioquímica.
Estructura y estereoquímica
La representación general R–S(=O)–R' refleja que el azufre está enlazado a dos sustituyentes orgánicos y al oxígeno. El par solitario en el azufre hace que la geometría alrededor de este átomo sea aproximadamente tetraédrica (a menudo descrita como piramidal), y no plana. Por ello muchos sulfóxidos con dos grupos diferentes en el azufre son quirales y pueden existir como enantiómeros configuracionales estables en condiciones normales. Esta propiedad se aprovecha en síntesis asimétrica y como auxiliares quirales.
Obtención y reactividad
Los sulfóxidos se obtienen fácilmente por la oxidación controlada de tioéteres (R–S–R'). Oxidantes comunes en laboratorio incluyen peróxidos suaves como el peróxido de hidrógeno o reactivos orgánicos como m-CPBA; con oxidación adicional se forma la sulfona (R–S(=O)2–R').
Reacciones y transformaciones importantes:
- Reducción: los sulfóxidos pueden reducirse a los tioéteres originales con agentes reductores adecuados.
- Pummerer y reordenamientos: los sulfóxidos activados pueden sufrir reacciones de Pummerer que generan sustituciones en la posición α al azufre.
- Uso como reactivo: el DMSO puede actuar no solo como disolvente, sino como reactivo en oxidaciones selectivas (por ejemplo, la oxidación de Swern, donde DMSO activado transforma alcoholes en aldehídos o cetonas).
- Coordinación: los sulfóxidos son ligandos versátiles para metales de transición. Pueden coordinar típicamente por el oxígeno (modo μ-O) con metales “duros”, y en algunos casos por el azufre con metales “blandos”; el modo de coordinación influye en la reactividad del complejo metálico.
Propiedades físicas destacadas
- Polaridad alta: muchos sulfóxidos son polares; el DMSO, por ejemplo, tiene un momento dipolar elevado, lo que le confiere elevada capacidad para disolver tanto compuestos polares como no polares.
- Miscibilidad: el DMSO es miscible con agua y con la mayoría de disolventes orgánicos; su punto de ebullición es relativamente alto, lo que facilita reacciones a temperaturas elevadas sin pérdida rápida de solvente.
- Olor: algunos sulfóxidos o sus productos de degradación (p. ej. dimetilsulfuro) tienen olores sulfurosos o a ajo, especialmente si son metabolizados o descompuestos.
Usos y aplicaciones (énfasis en DMSO)
El dimetilsulfóxido (DMSO) es el sulfóxido de mayor presencia industrial y de laboratorio. Entre sus aplicaciones principales se encuentran:
- Disolvente universal en síntesis orgánica y en bioquímica por su capacidad para disolver una amplia variedad de solutos y por su estabilidad química.
- Reactivo en transformaciones orgánicas (p. ej. oxidaciones tipo Swern).
- Crioprotector celular: se usa en crioconservación (por ejemplo, en congelación de células y tejidos) a concentraciones típicas alrededor del 10 % (v/v) porque reduce el daño por formación de cristales de hielo.
- Vehículo transdérmico: el DMSO facilita la penetración cutánea de otras moléculas, por lo que se emplea en formulaciones farmacéuticas y en investigación para entregar compuestos a través de la piel (esto exige precauciones por riesgo de transportar contaminantes).
- Medicina: el DMSO está aprobado en algunos países para aplicaciones médicas concretas (p. ej. tratamiento intravesical en cistitis intersticial) y se ha estudiado por sus propiedades antiinflamatorias y analgésicas tópicas.
- Química de coordinación: los sulfóxidos sirven como ligandos en catálisis homogénea y en la preparación y estabilización de complejos de metales de transición.
Seguridad y precauciones
Aunque el DMSO y muchos sulfóxidos son relativamente poco tóxicos comparados con otros disolventes orgánicos, requieren precauciones:
- El DMSO penetra la piel y puede transportar disueltos (solutos, impurezas, etc.) hacia la circulación; por eso no debe manipularse con las manos sin guantes adecuados y nunca debe usarse para aplicar sustancias desconocidas sobre la piel.
- Puede provocar irritación cutánea y reacciones alérgicas en algunas personas. La exposición sistémica puede causar un olor corporal tipo ajo por metabolitos sulfurosos.
- En uso farmacéutico se deben respetar contraindicaciones y dosis; algunos usos requieren receta o supervisión médica (p. ej. instilaciones intravesicales).
- Al desecharlo o emplearlo en síntesis, considerar su alta miscibilidad con agua y su persistencia: respetar normativas locales de gestión de residuos químicos.
En resumen, los sulfóxidos constituyen una familia funcional versátil en química orgánica y coordinación: su estructura con un par solitario en el azufre les confiere propiedades estereoquímicas y reactivas particulares, y compuestos como el DMSO son herramientas esenciales en investigación, síntesis y aplicaciones biomédicas cuando se usan con las debidas precauciones.