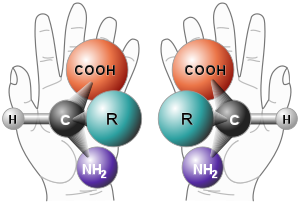
La quiralidad es cuando un objeto está presente en dos formas que son imágenes especulares entre sí.
Las dos formas no pueden superponerse. Las manos humanas son quirales. La mano izquierda es una imagen especular de la mano derecha. No se puede girar o mover una de las manos para que sea exactamente igual a la otra. Por eso no se puede poner un guante para zurdos en la mano derecha, ni estrechar la mano derecha de una persona con la mano izquierda.
Definición ampliada
En términos generales, un objeto o una molécula es quiral cuando no coincide con su imagen especular; si coincide, se dice que es achiral. Dos formas especulares no superponibles se llaman enantiómeros (en química). La quiralidad es una propiedad geométrica y puede aparecer en objetos cotidianos (manos, tornillos, hélices) y en estructuras moleculares.
Quiralidad en moléculas
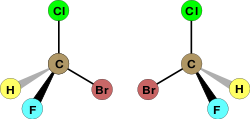
En química orgánica la quiralidad suele deberse a un átomo de carbono unido a cuatro sustituyentes diferentes (llamado centro estereogénico o estereocentro). Sin embargo, hay quiralidad sin estereocentro: por ejemplo, en allenes, helicenos o en ciertos complejos metálicos. Los enantiómeros tienen las mismas propiedades físicas (puntos de fusión, ebullición, espectros simples), salvo en cómo interactúan con la luz polarizada y con otros objetos quirales.
Propiedades y nomenclatura
- Actividad óptica: los enantiómeros rotan el plano de la luz polarizada en direcciones opuestas. Una mezcla equimolar de ambos enantiómeros (racemato) no rota la luz.
- Designación R/S: el sistema de Cahn–Ingold–Prelog asigna prioridad a los sustituyentes y determina la configuración absoluta como R (rectus) o S (sinister).
- Diferencia con diastereómeros: los diastereómeros son estereoisómeros no especulares y tienen propiedades físicas distintas.
Ejemplos comunes
- Manos humanas: ejemplo clásico de quiralidad macroscópica.
- Moléculas biológicas: aminoácidos (excepto glicina) y azúcares son quirales y la vida usa preferentemente una sola forma (por ejemplo, los aminoácidos L y los azúcares D).
- Ácido láctico: tiene dos enantiómeros con sabores y propiedades biológicas distintas.
- Fármacos: muchos medicamentos son quirales; los enantiómeros pueden tener actividad terapéutica diferente o efectos adversos distintos.
Importancia biológica y farmacéutica
Las biomoléculas (enzimas, receptores) son quirales y reconocen preferentemente una de las formas. Por eso, un enantiómero de un fármaco puede ser beneficioso mientras que el otro es menos activo o incluso tóxico. Esto hace que la separación, el control y la designación de la quiralidad sean críticos en la industria farmacéutica y en la investigación biomédica.
Cómo se detecta y separa la quiralidad
- Polarimetría: mide la rotación del plano de luz polarizada.
- Espectroscopía de dicroísmo circular: útil para proteínas y cromóforos quirales.
- RMN con reactivos quirales: permite distinguir enantiómeros en algunos casos.
- Cromatografía quiral: separa enantiómeros usando fases estacionarias quirales.
- Resolución química o enzimática: métodos para separar o transformar selectivamente un enantiómero.
Notas históricas y etimología
La palabra quiral proviene del griego cheir, que significa “mano”, y fue introducida por Lord Kelvin en el siglo XIX. El concepto ha sido fundamental en la comprensión de la estructura molecular y en el desarrollo de la química orgánica y la bioquímica modernas.
Resumen
La quiralidad describe la falta de superponibilidad con la propia imagen especular. Es una propiedad clave en química, biología y tecnología, porque determina comportamientos distintos frente a otros objetos quirales (como las enzimas) y frente a la luz polarizada. Comprender y controlar la quiralidad es esencial en áreas como la síntesis orgánica y la producción de fármacos seguros y eficaces.