La estereoquímica es el estudio de cómo las moléculas se ven afectadas por la forma en que sus átomos están dispuestos en el espacio. También se conoce como química 3D, ya que la palabra estéreo significa tridimensional. Gracias a la estereoquímica, los químicos pueden averiguar las relaciones entre diferentes moléculas compuestas por los mismos átomos. Además, pueden estudiar el efecto de estas relaciones sobre las propiedades físicas o biológicas de las moléculas. Cuando estas relaciones influyen en la reactividad de las moléculas, se denomina estereoquímica dinámica.
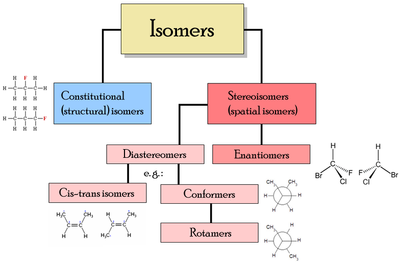
En química, algunas moléculas tienen más de un isómero. Esto significa que las moléculas pueden tener formas diferentes, aunque todas las formas estén compuestas por los mismos átomos. Hay dos grandes categorías de isómeros: los isómeros constitutivos tienen los mismos átomos, pero están unidos de forma diferente. Los estereoisómeros tienen los mismos átomos, están unidos de la misma manera, pero los átomos están dispuestos de forma diferente en el espacio. Una parte importante de la estereoquímica es el estudio de las moléculas quirales. Estas moléculas parecen casi idénticas, salvo que una molécula es la imagen especular de la otra.
En la mayoría de los enlaces químicos, los átomos de una molécula pueden moverse libremente sin romper los enlaces. Cuando una molécula tiene un doble enlace o una estructura de anillo, la molécula puede clasificarse en diferentes isómeros. Se trata de moléculas con la misma estructura química pero con formas diferentes.
El estudio de los problemas estereoquímicos abarca toda la gama de la química orgánica, inorgánica, biológica, física y supramolecular. A continuación se describen con más detalle los conceptos clave y los tipos de isómeros que aparecen con más frecuencia.
Tipos principales de isómeros
- Isómeros constitutivos (o estructurales): tienen la misma fórmula molecular pero diferente conectividad entre átomos. Ejemplos: cadenas ramificadas frente a lineales, posiciones distintas de un grupo funcional.
- Estereoisómeros: conservan la conectividad pero difieren en la disposición espacial de los átomos. Se subdividen en:
- Enantiómeros: pares de moléculas que son imágenes especulares no superponibles entre sí (como las manos derecha e izquierda). Se relacionan con la quiralidad.
- Diastereómeros: estereoisómeros que no son imágenes especulares. Incluyen epímeros (difieren en un solo centro estereogénico) y ciertas formas geométricas.
- Isomería geométrica (cis/trans o E/Z): aparece cuando la rotación libre está restringida, por ejemplo por un doble enlace o un anillo, dando distintas posiciones relativas de sustituyentes.
- Isómeros conformacionales: resultan de la rotación alrededor de enlaces sencillos. Aunque suelen interconvertirse fácilmente, algunas conformaciones (por ejemplo en sistemas rígidos o atropisómeros) pueden ser lo suficientemente estables para aislarse.
Quiralidad: qué es y por qué importa
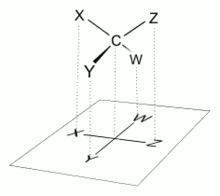
Una molécula es quiral si no puede superponerse con su imagen especular. La presencia de un centro estereogénico más comúnmente un átomo de carbono unido a cuatro sustituyentes distintos, genera quiralidad. Pero la quiralidad también puede surgir de:
- ejes quirales (axial), por ejemplo en biarilos impedidos (atropisomerismo),
- planos quirales,
- y helicidades en estructuras helicoidales.
Las moléculas quirales tienen propiedades físicas idénticas (puntos de ebullición, masa molecular, etc.) salvo la interacción con la luz polarizada y con otros sistemas quirales. Por ejemplo, los enantiómeros rotan el plano de la luz polarizada en direcciones opuestas (actividad óptica) y suelen tener interacciones biológicas muy diferentes: un enantiómero de un fármaco puede ser activo mientras que el otro es inactivo o incluso tóxico.
Notación y reglas
- Reglas de Cahn–Ingold–Prelog (R/S): permiten asignar la configuración absoluta de un centro estereogénico como R (rectus) o S (sinister) según el orden de prioridad de los sustituyentes.
- Notación E/Z: para dobles enlaces, donde E (entgegen) indica sustituyentes principales en lados opuestos y Z (zusammen) en el mismo lado, basada en prioridades CIP.
- Cis/trans: forma simplificada para sustituentes idénticos en sistemas cíclicos o dobles enlaces en casos simples.
Conceptos adicionales clave
- Compuestos meso: moléculas con centros estereogénicos internas pero que son globalmente achirales por tener un plano de simetría.
- Racemato: mezcla 1:1 de dos enantiómeros que no muestra actividad óptica neta. La separación de enantiómeros se llama resolución.
- Estereoquímica dinámica: estudios sobre cómo la forma y la reactividad cambian con el tiempo por procesos de inversión de configuración, epimerización, racemización o intercambio conformacional.
- Stereoselectividad y estereospecificidad: en reacciones químicas, la estereoselectividad indica preferencia por formar un estereoisómero sobre otro; la estereospecificidad indica que el mecanismo determina un único estereoisómero según el sustrato.
Métodos para estudiar la estereoquímica
- Polarimetría: mide la rotación del plano de luz polarizada para cuantificar la actividad óptica.
- Espectroscopía (RMN, CD, IR con quimiosensibilidad estérica): permite distinguir configuraciones y conformaciones en solución.
- Cromatografía en fases quirales y métodos de resolución para separar enantiómeros.
- Difracción de rayos X: proporciona la estructura absoluta y disposiciones tridimensionales en estado sólido.
- Modelado molecular y cálculos teóricos: predicen conformaciones, barreras de rotación y selectividad estereoquímica en reacciones.
Importancia práctica
La estereoquímica es crucial en áreas como:
- Química farmacéutica: la eficacia y seguridad de fármacos dependen a menudo de su configuración estereoquímica.
- Bioquímica: enzimas y receptores distinguen entre enantiómeros de forma muy selectiva.
- Síntesis orgánica: el diseño de rutas asimétricas y catalizadores quiral es un campo central para obtener compuestos con la configuración deseada.
- Materiales y catálisis: la disposición espacial afecta propiedades electrónicas, ópticas y mecánicas.
En resumen, la estereoquímica describe cómo la geometría tridimensional de las moléculas condiciona sus propiedades y reacciones. Comprender y controlar la estereoquímica permite diseñar moléculas con funciones específicas, optimizar procesos sintéticos y prever el comportamiento biológico y físico de sustancias químicas.