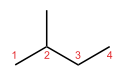El isomerismo estructural (la IUPAC lo llama isomerismo constitucional) es un tipo de isomerismo en el que dos sustancias químicas tienen la misma fórmula molecular pero las moléculas se han enlazado en órdenes distintos, es decir, los átomos están conectados entre sí de diferente manera. Lo contrario del isomerismo estructural es el estereoisomerismo, donde la conectividad es la misma pero difiere la disposición espacial. El isomerismo estructural da lugar a compuestos con propiedades físicas y químicas notablemente diferentes (punto de ebullición, solubilidad, reactividad, etc.).
Tipos principales de isomerismo estructural
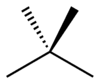
- Isómeros esqueléticos (o de cadena): cambian la disposición del esqueleto carbonado. Ejemplo clásico: C4H10 tiene dos isómeros esqueléticos, n-butano y 2-metilpropano (isobutano). También se incluyen los casos de cadena lineal frente a cadena ramificada.
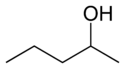
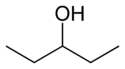
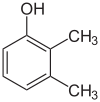
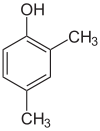
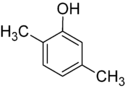
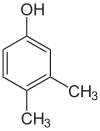
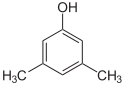
- Isómeros posicionales (regioisómeros): los mismos átomos y el mismo grupo funcional, pero con la posición del grupo funcional o de un sustituyente diferente en la cadena. Por ejemplo, C4H10O incluye 1-butanol (butan-1-ol) y 2-butanol (butan-2-ol) como isómeros posicionales; cambian propiedades como el punto de ebullición y la reactividad.
- Isómeros funcionales: los isómeros presentan diferente grupo funcional a pesar de tener la misma fórmula molecular. Un ejemplo típico es C2H6O, que puede ser etanol (un alcohol) o dimetil éter (un éter). Dentro de este grupo se consideran los tautómeros, que son casos especiales donde hay un equilibrio dinámico entre dos estructuras que difieren en la posición de un protón y de un doble enlace (por ejemplo, las formas keto-enol).
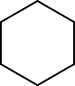
- Isomerismo anillo-cadena: cuando un compuesto puede existir en forma cíclica o en cadena abierta con la misma fórmula. Un ejemplo simple es C6H12, que puede presentarse como ciclohexano (compuesto cíclico) o como hexenos (compuestos con una doble enlace en cadena).
Sobre los tautómeros
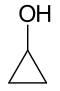
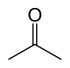
Los tautómeros son un caso particular de isómeros funcionales en el cual las formas se interconvierten mediante transferencia de un protón (H+) y reacomodo de enlaces π. El ejemplo más citado es la tautomería keto-enol: una cetona o aldehído puede presentar una forma enol, con distinta reactividad y propiedades espectroscópicas. Esta interconversión suele estar en equilibrio y depende del disolvente, pH y temperatura. En bioquímica, la tautomería puede afectar la apareamiento de bases y, por tanto, la genética.
Cómo distinguir isómeros constitucionales
- Propiedades físicas: puntos de fusión y ebullición, densidad y solubilidad pueden diferir sensiblemente entre isómeros.
- Reactividad química: distintos grupos funcionales o posiciones funcionales reaccionan de manera diferente con reactivos específicos.
- Técnicas espectroscópicas: espectros de RMN, IR, espectrometría de masas (MS) y espectros UV/Vis permiten identificar la conectividad y los grupos funcionales.
- Cromatografía (GC, HPLC) para separar y caracterizar mezclas de isómeros.
Importancia y aplicaciones
El isomerismo constitucional es crucial en química orgánica, farmacología y diseño de materiales. Isómeros con la misma fórmula pueden tener toxicidades, niveles de actividad farmacológica o propiedades físicas muy distintas; por eso la identificación y la síntesis selectiva de un isómero concreto son tareas fundamentales en investigación y desarrollo industrial.
En resumen, el isomerismo estructural (o constitucional) agrupa varios modos en los que la conectividad atómica cambia sin alterar la fórmula molecular: isómeros de cadena, posicionales (regioisómeros), funcionales (incluidos tautómeros) y anillo-cadena. Cada tipo modifica las propiedades del compuesto y requiere técnicas analíticas específicas para su identificación y separación.