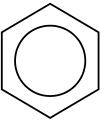
Un hidrocarburo aromático, o areno, es un compuesto anular de hidrocarburo. Tiene enlaces dobles y simples alternados entre los átomos de carbono formando anillos. Muchos de estos compuestos tienen un olor dulce, de ahí el término "aromático". El anillo de seis átomos de carbono de los compuestos aromáticos se conoce como anillo de benceno, en honor al anillo de hidrocarburo más simple posible, el benceno. Los hidrocarburos aromáticos pueden ser monocíclicos (MAH) o policíclicos (PAH).
Algunos compuestos no bencénicos, llamados heteroarenos, que siguen la regla de Hückel, también son compuestos aromáticos. En estos compuestos, al menos un átomo de carbono se sustituye por uno de oxígeno, nitrógeno o azufre.
Estructura y aromaticidad
La aromaticidad es una propiedad electrónica que hace a ciertos anillos especialmente estables. Para que un sistema sea aromático debe cumplir criterios clásicos: ser cíclico, plano, totalmente conjugado (es decir, tener orbitales p solapados a lo largo del anillo) y poseer (4n + 2) electrones π según la regla de Hückel (donde n es un número entero). Por ejemplo, el benceno tiene 6 electrones π (n = 1) distribuidos de forma deslocalizada; esto produce energías de resonancia, longitudes de enlace intermedias y mayor estabilidad frente a reacciones que romperían la aromaticidad.
Tipos de hidrocarburos aromáticos
- Monocíclicos (MAH): anillos individuales como el benceno y derivados sencillos (tolueno, fenol cuando hay OH, etc.).
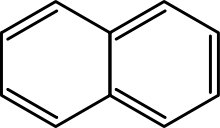
- Policíclicos (PAH): dos o más anillos condensados o fusionados (naphthaleno, antraceno, fenantreno). Pueden ser lineales o angularmente condensados.
- Heteroarenos: anillos aromáticos que contienen heteroátomos como oxígeno, nitrógeno o azufre (p. ej. furanos, pirroles, tiofenos, piridinas). A menudo mantienen aromaticidad si respetan la regla de Hückel.
- Arenos sustituidos: arenos que llevan grupos funcionales (alquil, nitro, halógeno, acilo). La naturaleza del sustituyente controla la reactividad y la orientación de nuevas sustituciones.
Reacciones características
La reacción más típica de los arenos es la sustitución electrófila aromática (SEAr), en la que un sustituyente del anillo es reemplazado por un electrófilo sin perder la aromaticidad. Ejemplos comunes:
- Nitración (introducción de -NO2).
- Sulfonación (introducción de -SO3H).
- Halogenación (Cl, Br) en presencia de catalizadores (FeCl3, AlCl3).
- Acilación y alquilación de Friedel–Crafts (introducción de grupos acilo o alquilo).
Otras reacciones incluyen la hidrogenación (convierte el anillo en cicloalcanos, por ejemplo, benceno → ciclohexano bajo alta presión y catalizador), la oxidación de cadenas laterales (p. ej. tolueno → ácido benzoico) y reacciones de acoplamiento en síntesis orgánica. Los heteroarenos presentan reactividad diferente según el heteroátomo; por ejemplo, la piridina es menos reactiva a SEAr pero participa en reacciones de sustitución nucleófila.
Propiedades físicas y spectroscópicas
Los arenos suelen ser relativamente estables, poco solubles en agua y más solubles en disolventes orgánicos. Tienen C–H aromáticos con frecuencias de estiramiento cerca de 3030 cm⁻¹ en espectros IR y señales características en RMN: los protones aromáticos aparecen típicamente entre 6–9 ppm en 1H-NMR. Los PAH presentan bandas UV–Vis intensas y desplazadas a longitudes de onda mayores conforme aumenta la conjugación.
Métodos de obtención
Industrialmente, muchos arenos (como el benceno, tolueno y xileno) se obtienen por reformado catalítico del petróleo, craqueo y procesos de refinación. En laboratorio se emplean reacciones de síntesis orgánica: Friedel–Crafts, acoplamientos catalizados (Suzuki, Heck), deshidrogenaciones y ciclaciones aromatizantes.
Ejemplos representativos
- Benceno (C6H6): prototipo de anillo aromático.
- Tolueno (metilbenceno): solvente común y precursor de compuestos industriales.
- Naphthaleno: PAH de dos anillos fusioandos (ej. naftaleno).
- Antraceno y fenantreno: PAH de tres anillos con diferencias en su disposición y propiedades ópticas.
- Piridina, furan y tiofeno: ejemplos de heteroarenos con N, O y S respectivamente.
Aplicaciones
Los hidrocarburos aromáticos y sus derivados son fundamentales en la industria: solventes, materias primas para polímeros, colorantes, fármacos, explosivos y productos agroquímicos. Muchos procesos químicos se diseñan para introducir o transformar grupos en anillos aromáticos porque estos núcleos confieren estabilidad y propiedades físico-químicas útiles.
Riesgos y consideraciones ambientales
Algunos PAH son persistentes, bioacumulativos y carcinógenos (por ejemplo, el benzo[a]pireno). La combustión incompleta de materia orgánica (carbón, petróleo, madera) genera mezclas de PAH que contaminan aire, suelo y agua. Es importante controlar emisiones industriales y manejar con precaución disolventes aromáticos: muchos son tóxicos, irritantes o nocivos por inhalación y contacto.
Resumen
Los hidrocarburos aromáticos (arenos) son compuestos anulares con electrones π deslocalizados que confieren aromaticidad y estabilidad. Pueden ser monocíclicos, policíclicos o heteroarenos y participan en reacciones típicas como la sustitución electrófila aromática. Tienen amplia utilidad industrial, pero algunos presentan riesgos para la salud y el medio ambiente, por lo que su manejo requiere precaución.