Benceno: definición, propiedades, usos y riesgos para la salud
Benceno: qué es, propiedades, usos industriales y riesgos para la salud. Descubre exposición, efectos cancerígenos, uso en combustibles y plásticos y cómo prevenir daños.
El benceno, también conocido como benzol, es un compuesto químico orgánico de fórmula C6 H6. Es un líquido incoloro e inflamable con un olor dulce y característico. Las moléculas de benceno forman un anillo de seis átomos de carbono unidos cada uno a un átomo de hidrógeno; es un compuesto aromático, lo que en química orgánica indica que el anillo presenta electrones π deslocalizados (resonancia) en lugar de enlaces dobles fijos, lo que le confiere estabilidad y reactividad particular frente a reacciones de sustitución.
Propiedades físicas y químicas
- Masa molar: 78,11 g·mol⁻¹.
- Punto de ebullición: aproximadamente 80,1 °C.
- Punto de fusión: aproximadamente 5,5 °C.
- Densidad: cerca de 0,88 g·cm⁻³ a 20 °C (más liviano que el agua).
- Solubilidad: prácticamente insoluble en agua, pero miscible con muchos solventes orgánicos.
- Inflamabilidad: líquido altamente inflamable y con baja temperatura de inflamación; forma vapores que pueden explotar al mezclarse con el aire.
- Reactividad: relativamente estable por su aromaticidad; sin embargo sufre reacciones típicas como la nitración, sulfonación y halogenación, y se usa como bloque de construcción en síntesis orgánica.
Usos
El benceno tiene múltiples aplicaciones industriales y es materia prima en la síntesis de numerosos productos. Entre sus usos más habituales se incluyen:
- Como aditivo o componente presente en la gasolina y otros combustibles.
- Precursor en la producción de plásticos y polímeros (por ejemplo, para fabricar estireno y nylon).
- Materia prima para la obtención de caucho sintético.
- Fabricación de tintes y colorantes, así como de intermediarios químicos usados en la industria textil y química fina.
- Uso como disolvente industrial para grasas, aceites, resinas y en procesos de extracción y limpieza (aunque su uso ha disminuido por motivos de salud).
- Está presente de forma natural en el petróleo crudo y, por tanto, en derivado como la gasolina. Además, partes de la estructura de muchos medicamentos y productos químicos industriales derivan del benceno.
Riesgos para la salud
El benceno es un cancerígeno humano reconocido y se asocia especialmente con trastornos hematológicos. Los riesgos dependen de la vía y duración de la exposición:
- Vías de exposición: principalmente inhalación de vapores; también puede absorberse por la piel o, en menor medida, por ingestión.
- Efectos agudos: exposición a concentraciones altas puede causar mareo, dolor de cabeza, náuseas, confusión, aturdimiento y, en casos extremos, pérdida de conciencia o depresión del sistema nervioso central.
- Efectos crónicos: la exposición prolongada puede producir supresión de la médula ósea (anemia aplásica), trastornos de la sangre y aumento del riesgo de leucemia (especialmente leucemia mieloide aguda). También se han descrito efectos inmunológicos y reproductivos en estudios animales y ocupacionales.
- Poblaciones sensibles: trabajadores expuestos habitualmente, embarazadas y personas con enfermedades respiratorias pueden ser más vulnerables.
Prevención, control y primeros auxilios
- Prevención en el trabajo: emplear controles de ingeniería (ventilación local, cabinas), medición ambiental y vigilancia médica. Usar equipos de protección personal adecuados (respiradores, guantes resistentes a solventes, gafas de seguridad). Sustituir benceno por alternativas menos tóxicas cuando sea posible.
- Almacenamiento: conservar en recipientes cerrados, en lugares bien ventilados, alejados de fuentes de ignición y tierra adecuadamente para evitar cargas electrostáticas.
- Primeros auxilios:
- Inhalación: sacar a la persona al aire fresco; si hay dificultad respiratoria, buscar atención médica inmediata y, si es necesario, administrar oxígeno por personal capacitado.
- Contacto con la piel: retirar ropa contaminada y lavar la piel con agua y jabón durante al menos 15 minutos; buscar atención si aparecen síntomas.
- Contacto con los ojos: enjuagar con abundante agua durante 15 minutos y consultar a un especialista.
- Ingestión: no inducir el vómito; buscar atención médica urgente.
- En caso de incendio: por ser muy inflamable, usar agentes extintores adecuados (espuma, polvo químico, dióxido de carbono) y equipos de protección para bomberos; evitar usar chorros directos de agua que pueden dispersar el producto.
Impacto ambiental y manejo de derrames
El benceno es volátil y puede liberarse al aire durante la producción, el transporte o por combustión incompleta. Se mueve fácilmente en suelos y aguas subterráneas y puede ser tóxico para organismos acuáticos. El manejo de derrames requiere contención (barreras/booms), adrenalización (absorción con materiales adecuados), y, cuando proceda, recuperación y tratamiento del suelo o aguas afectadas (excavación, tratamiento biológico o químico). Las comunidades y los gestores ambientales deben seguir planes de respuesta ante emergencias y regulaciones locales.
Regulación y límites de exposición
Dadas sus propiedades tóxicas y cancerígenas, múltiples agencias de salud y seguridad laboral establecen límites de exposición muy bajos y normas para su manejo. Estos límites varían según el país y la agencia; por ello es importante consultar la normativa local y las fichas de datos de seguridad (FDS) para valores específicos y obligaciones regulatorias.
Alternativas y consideraciones finales
Aunque el benceno es valioso como precursor químico, su uso directo como disolvente o aditivo ha disminuido frente a alternativas menos peligrosas y a mejoras en los procesos industriales. En muchos casos es posible sustituirlo por disolventes menos tóxicos, emplear métodos sin solventes o aplicar principios de química verde para reducir la exposición y el impacto ambiental. En cualquier caso, siempre debe respetarse la normativa de seguridad y la formación del personal que maneje sustancias que contienen benceno.
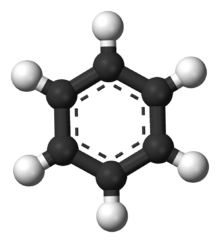
Modelo de una molécula de benceno. Los átomos de carbono se muestran en negro y el hidrógeno en blanco.
_1964,_MiNr_440.jpg)
En 1964, el servicio postal alemán emitió un sello en conmemoración de los 100 años del descubrimiento del benceno
Estructura
El benceno tiene unas propiedades especiales denominadas aromaticidad. Los seis átomos de carbono del anillo están en el mismo plano. Para explicar todos los enlaces en un anillo de seis carbonos, debe haber dobles enlaces de carbono alternados (sistema conjugado):
Si el benceno tuviera tres dobles enlaces, tres lados de su anillo serían más cortos que los otros tres. La difracción de rayos X muestra que los seis enlaces carbono-carbono del benceno tienen la misma longitud de 140 picómetros (pm). Las longitudes de los enlaces C-C son mayores que las de un enlace doble (135 pm) pero menores que las de un enlace simple (147 pm). Esta distancia intermedia es coherente con la deslocalización de electrones: los electrones del enlace C-C se distribuyen por igual entre cada uno de los seis átomos de carbono. La molécula es plana. Una representación es que la estructura existe como una superposición de las llamadas estructuras de resonancia, en lugar de cualquiera de las dos formas por separado. (En otras palabras, los dobles enlaces de la molécula cambian rápidamente entre pares de átomos de carbono). La deslocalización de los electrones es una de las explicaciones de la estabilidad termodinámica del benceno y los compuestos aromáticos relacionados. Es probable que esta estabilidad contribuya a las peculiares propiedades moleculares y químicas conocidas como aromaticidad. Para indicar la naturaleza deslocalizada del enlace, el benceno suele representarse con un círculo dentro de una disposición hexagonal de átomos de carbono.
Como es habitual en química orgánica, los átomos de carbono del diagrama anterior se han dejado sin etiquetar. Teniendo en cuenta que cada carbono tiene 2 electrones p, cada carbono dona un electrón al anillo deslocalizado por encima y por debajo del anillo de benceno. El solapamiento de los orbitales p por encima y por debajo del anillo es lo que produce las nubes pi.
En 1986, algunos químicos rebatieron la visión deslocalizada del benceno en un artículo publicado en la revista Nature. Demostraron que los electrones del benceno están casi ciertamente localizados en determinados átomos de carbono. Demostraron que las propiedades aromáticas del benceno provienen del acoplamiento de espines y no de la deslocalización de los electrones. Otros científicos escribieron artículos en apoyo de este punto de vista en Nature en 1987. Sin embargo, los químicos tardan en cambiar la visión de los electrones deslocalizados.
Los derivados del benceno aparecen con suficiente frecuencia como componente de las moléculas orgánicas como para que exista un símbolo Unicode en el bloque técnico de Varios con el código U+232C (⌬) para representarlo con tres dobles enlaces, y U+23E3 (⏣) para una versión deslocalizada.
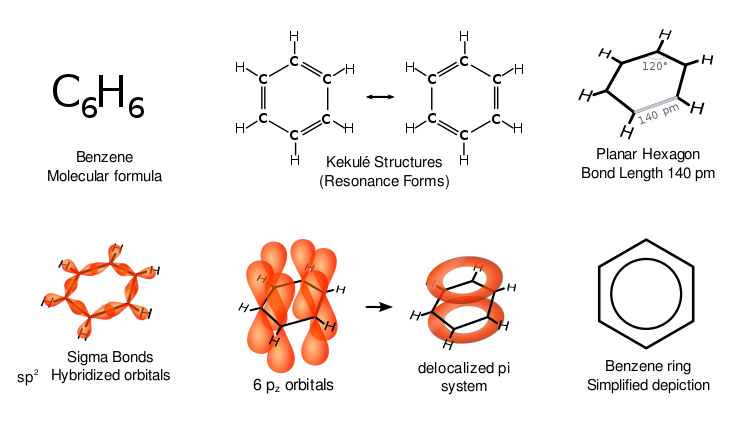
Las distintas representaciones del benceno
Preguntas y respuestas
P: ¿Qué es el benceno?
R: El benceno es un compuesto químico orgánico.
P: ¿Cuál es la fórmula química del benceno?
R: La fórmula química del benceno es C6H6.
P: ¿Cuál es el aspecto y el olor del benceno?
R: El benceno es un líquido incoloro e inflamable con un olor dulce.
P: ¿Cuál es la estructura de una molécula de benceno?
R: Una molécula de benceno es un anillo de seis átomos de carbono unidos cada uno a un átomo de hidrógeno. Es un compuesto aromático, lo que significa que el anillo tiene enlaces dobles alternados.
P: ¿Es cancerígeno el benceno?
R: Sí, el benceno es cancerígeno, lo que significa que puede provocar cáncer.
P: ¿Cuáles son algunos usos del benceno en el mundo real?
R: El benceno se utiliza como aditivo en la gasolina, los plásticos, el caucho sintético, los tintes y es un disolvente industrial, lo que significa que puede disolver muchas otras moléculas químicas. Muchos medicamentos también contienen partes fabricadas con benceno.
P: ¿Dónde se encuentra el benceno?
R: El benceno es una parte natural del petróleo crudo y, por tanto, está presente en la gasolina.
Buscar dentro de la enciclopedia