Sistema conjugado (química): definición, propiedades y ejemplos
Sistema conjugado (química): definición clara, propiedades, ejemplos y aplicaciones — descubre cómo la deslocalización electrónica influye en estabilidad, color y conductividad.
En química, un sistema conjugado es un sistema de orbitales p conectados con electrones deslocalizados. Los sistemas conjugados se crean mediante varios enlaces múltiples, cada uno de ellos separado por enlaces simples. En general, los sistemas conjugados pueden reducir la energía global de la molécula y aumentar su estabilidad. Pueden contener pares solitarios, radicales o iones de carbenio. El compuesto puede ser cíclico, acíclico, lineal o mixto. En la mayoría de los casos, los átomos de una molécula se mantienen unidos mediante enlaces simples (en los que los orbitales de los átomos adyacentes se solapan). Las moléculas que tienen un sistema conjugado tienen propiedades únicas, diferentes de las de los compuestos normales, creadas por el reparto de los electrones deslocalizados entre muchos átomos.
La conjugación es el solapamiento de un orbital p con otro a través de un enlace sigma (o enlace simple) que se encuentra entre ambos. (Los orbitales d de los átomos más grandes también pueden contribuir a un sistema conjugado).
Un sistema conjugado tiene una región de orbitales p superpuestos, que tienden un puente sobre los enlaces simples que se encuentran entre ellos. Permiten una deslocalización de los electrones pi a través de todos los orbitales p adyacentes alineados. Los electrones pi no pertenecen a un solo enlace o átomo, sino a un grupo de átomos.
Los sistemas conjugados más grandes (con el mayor número de electrones compartidos) se encuentran en el grafito, los polímeros conductores y los nanotubos de carbono.
Propiedades principales
- Estabilización por deslocalización: la distribución de electrones pi sobre varios átomos reduce la energía total de la molécula. Esta ganancia de estabilidad suele describirse como energía de resonancia o deslocalización.
- Igualación parcial de longitudes de enlace: en un sistema conjugado las longitudes de enlace entre átomos tienden a valores intermedios entre enlace simple y doble, debido a la naturaleza compartida de los electrones.
- Variación en reactividad: los centros conjugados pueden comportarse de forma distinta frente a reacciones electrofílicas o nucleofílicas (por ejemplo, la adición 1,2 vs. 1,4 en dienos conjugados o la adición conjugada / reacción de Michael en enonas).
- Propiedades ópticas y electrónicas: la conjugación reduce la brecha HOMO–LUMO; cuanto mayor es la conjugación, menor suele ser la energía de absorción en UV-Vis (desplazamiento batocrómico), lo que provoca color en muchas moléculas orgánicas. También aumenta la movilidad electrónica en polímeros conjugados, favoreciendo la conductividad.
- Efectos en espectroscopía: la deslocalización modifica desplazamientos químicos en RMN y patrones de absorción en infrarrojo y UV-Vis; en sistemas aromáticos aparecen corrientes de anillo que afectan el apantallamiento magnético.
Cómo identificar un sistema conjugado
- Presencia de enlaces múltiples alternados con enlaces simples (por ejemplo, C=C–C=C).
- Lone pairs (pares solitarios) o cargas adyacentes a un doble enlace que puedan participar mediante solapamiento de orbital p (p. ej., en enoles o enolatos).
- Configuración geométrica que permita el alineamiento de orbitales p: si los fragmentos quedan girados (por ejemplo, bifenilos ortogonales), la conjugación se interrumpe.
- Diferenciar entre sistemas conjugados lineales, cíclicos y cruzados: la conjugación cruzada ocurre cuando un doble enlace se conecta a dos sistemas conjugados pero éstos no están entre sí conjugados.
Ejemplos típicos
- Benceno (sistema aromático): los seis electrones pi están completamente deslocalizados sobre el anillo; presenta una estabilización especial (regla de Hückel 4n+2 para aromaticidad).
- 1,3-Butadieno: ejemplo clásico de dieno conjugado; muestra dos tipos de adición (1,2 y 1,4) y posee orbitales moleculares extendidos sobre cuatro átomos.
- Sistemas conjugados extensos: poli(acetileno), polímeros conductorres y cadenas conjugadas en pigmentos y colorantes, donde la longitud de conjugación determina color y conductividad.
- Carbaniones, cationes o radicales estabilizados por conjugación (p. ej., catión alílico o anión alílico), donde la carga o el radical se distribuyen sobre varios átomos.
- Enonas (C=C–C=O): la conjugación entre el doble enlace y el grupo carbonilo modifica tanto la reactividad como las propiedades espectroscópicas.
Conjugación vs otros casos
- Cumulados (p. ej., allenos): en los cumulenos las dobles están consecutivas (C=C=C) y no forman conjugación lineal de la misma manera; la geometría de los orbitales p es distinta.
- Interrupción por torsión: la conjugación requiere solapamiento efectivo de orbitales p; un giro que haga ortogonales esos orbitales impide la deslocalización.
- Aromaticidad y antiaromaticidad: los sistemas cíclicos conjugados pueden ser aromáticos si cumplen la regla de Hückel (4n+2 electrones pi) o antiaromáticos si tienen 4n electrones, con consecuencias drásticas en su estabilidad.
Consecuencias químicas y aplicaciones
- Reactividad selectiva: los dienos conjugados participan en reacciones pericíclicas como la reacción de Diels–Alder; las enonas experimentan adición conjugada (Michael).
- Materiales funcionales: pigmentos, colorantes, polímeros conductores y componentes optoelectrónicos (OLEDs, celdas solares) basan su funcionamiento en extensos sistemas conjugados.
- Biomoléculas: muchos cromóforos biológicos (p. ej., carotenoides) deben su color y propiedades fotosensibles a sistemas conjugados largos.
Notas finales y consejos prácticos
- Para evaluar si una molécula está conjugada, busque alternancia de enlaces o pares solitarios que puedan participar y compruebe la geometría (plana o casi plana favorece conjugación).
- Recuerde que la conjugación suele aumentar la estabilidad relativa, pero el efecto exacto depende del contexto electrónico y estérico de la molécula.
- Herramientas experimentales (UV-Vis, RMN, difracción de rayos X) y cálculos teóricos (MO, DFT) permiten cuantificar y visualizar la deslocalización electrónica.

El cinamaldehído, un tipo de compuesto fenólico con un sistema conjugado
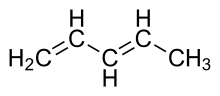
1,3-pentadieno
Mecanismo
Diferentes tipos de estructuras moleculares pueden dar lugar a la conjugación. Para la conjugación, todos los átomos vecinos de una cadena deben tener un orbital p disponible. En muchos casos, los sistemas conjugados son una serie de enlaces simples seguidos por un enlace doble. Existen otros sistemas. Por ejemplo, el furano (ver imagen) es un anillo de cinco miembros con dos dobles enlaces alternados y un oxígeno en posición 1. El oxígeno del furano tiene dos pares solitarios, uno de los cuales llena un orbital p en esa posición. El electrón del par solitario hace posible la conjugación en un anillo de cinco miembros. La presencia de un nitrógeno en el anillo puede ser una fuente de orbitales pi necesarios para la conjugación. Además, los orbitales pi necesarios para la conjugación pueden proceder de grupos sustituyentes α al anillo como: un grupo carbonilo (C=O), un grupo imina (C=N), un grupo vinilo (C=C) o un anión.
Cromóforos
Los sistemas conjugados son los principales componentes de los cromóforos. Los cromóforos son partes de una molécula que absorben la luz y pueden hacer que un compuesto tenga un color visible. Los cromóforos suelen estar presentes en diversos compuestos orgánicos y, a veces, en polímeros que se colorean o brillan en la oscuridad. Los cromóforos suelen estar formados por una serie de enlaces conjugados y/o sistemas de anillos, que pueden incluir enlaces C-C, C=C, C=O o N=N. Muchas veces, los cromóforos tienen anillos aromáticos.
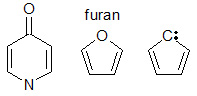
Conjugación con diferentes tipos de grupos donadores de orbitales p
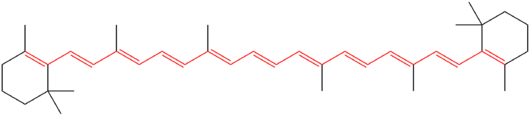
Estructura química del betacaroteno. Los once dobles enlaces conjugados que forman el cromóforo de la molécula están resaltados en rojo.
Ejemplos comunes
Páginas relacionadas
- Resonancia (química)
- Hiperconjugación
- Conjugación cruzada
- Polieno
Preguntas y respuestas
P: ¿Qué es un sistema conjugado en química?
R: Un sistema conjugado es un sistema de orbitales p continuos y paralelos con electrones deslocalizados.
P: ¿Cómo se crean los sistemas conjugados?
R: Los sistemas conjugados se crean mediante varios enlaces múltiples, cada uno separado por enlaces simples.
P: ¿Qué cosas pueden encontrarse en un sistema conjugado?
R: Los sistemas conjugados pueden contener pares solitarios, radicales o iones de carbonio.
P: ¿Un compuesto con un sistema conjugado puede ser cíclico?
R: Sí, un compuesto con un sistema conjugado puede ser cíclico, acíclico, lineal o mixto.
P: ¿Cuáles son las propiedades únicas de las moléculas con un sistema conjugado?
R: Las moléculas con un sistema conjugado tienen propiedades únicas diferentes de los compuestos normales, creadas por el reparto de los electrones deslocalizados entre muchos átomos.
P: ¿Cuál es el solapamiento implicado en la conjugación?
R: La conjugación es el solapamiento de un orbital p con otro a través de un enlace sigma (o enlace simple) que se encuentra entre ambos.
P: ¿Dónde se encuentran los sistemas conjugados más grandes?
R: Los sistemas conjugados más grandes (con el mayor número de electrones compartidos) se encuentran en el grafito, los polímeros conductores y los nanotubos de carbono.
Buscar dentro de la enciclopedia