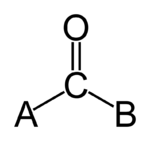
Un carbonilo es el grupo funcional formado por un átomo de carbono y un átomo de oxígeno unidos mediante un doble enlace (C=O). Aparece como parte de muchas moléculas orgánicas: por ejemplo, es el fragmento C=O en una cetona, en un aldehído, en un éster, en un ácido carboxílico, en una amida o en un haluro de acilo.
Estructura y hibridación
El carbono del carbonilo es típicamente sp2 hibridizado; forma tres enlaces sigma (dos con sustituyentes y uno con el oxígeno) y un enlace pi con el oxígeno. El oxígeno aporta pares electrónicos no enlazantes y también puede describirse con una hibridación cercana a sp2, lo que explica la planaridad parcial de este fragmento y la existencia de resonancia entre las estructuras canónicas (con carga parcial positiva en el carbono y negativa en el oxígeno).
Polaridad y propiedades electrónicas
Como el oxígeno es más electronegativo que el carbono, los electrones del enlace se desplazan hacia el oxígeno, generando un dipolo Cδ+=Oδ−. Por eso el carbono carbonílico es electrofílico y susceptible al ataque de nucleófilos. Además, en presencia de un ácido o de agentes protonantes, un protón tiende a protonar el oxígeno, lo que aumenta aún más la reactividad del carbono.
Reactividad: reacciones típicas
El grupo carbonilo es uno de los centros reactivos más versátiles en química orgánica. Entre las reacciones más importantes destacan:
- Adición nucleófila: ataque de nucleófilos al carbono carbonílico, formando intermediarios tetraédricos. Ejemplos: formación de hemiacetales y acetales, cianohidrinas, hidrólisis de derivados acílicos.
- Reducción: reducción a alcoholes mediante hidruros (p. ej. NaBH4, LiAlH4) o catalíticamente (H2/Pd).
- Oxidación: por ejemplo la oxidación de aldehídos a ácidos carboxílicos.
- Reacciones ácido–base en posiciones alfa: los hidrógenos alfa al carbonilo son relativamente ácidos y pueden formar enolatos, que participan en condensaciones (Claisen, Aldol) y alquilaciones.
- Reacciones específicas de derivados: los ésteres, amidas, anhídridos y haluros de acilo muestran reactividad nucleofílica diferente debido a la estabilización por resonancia o a la presencia de buenos grupos salientes.
Variaciones por conjugación y sustituyentes
Si el carbonilo está conjugado con un doble enlace o un anillo aromático, la energía del enlace y su reactividad cambian: la conjugación estabiliza el sistema y suele disminuir la frecuencia de estiramiento C=O en espectros IR y moderar la electrophilicidad del carbono. Sustituyentes electron‑donantes o -atrayentes también modifican la polaridad y la facilidad de ataque nucleofílico.
Importancia biológica y tecnológica
Los carbonilos aparecen en numerosas moléculas naturales y fármacos. Ejemplos relevantes: enlaces peptídicos (amidas) en proteínas, grupos carboxílicos en ácidos grasos y metabolitos, y grupos cetona o aldehído en azúcares y vitaminas. Su reactividad permite diseñar rutas sintéticas en la industria farmacéutica y en la síntesis orgánica.
Identificación experimental
Es fácil detectar un carbonilo por técnicas espectroscópicas:
- En la espectroscopia de infrarrojos, el estiramiento C=O produce una banda fuerte y característica. Los valores típicos son alrededor de 1700 cm−1 para cetonas y aldehídos; los ésteres suelen aparecer cerca de 1735 cm−1, las amidas más abajo (≈1650 cm−1) y la conjugación o la formación de puentes de hidrógeno desplazan la banda hacia frecuencias menores.
- En la espectroscopia de RMN de carbono (13C), el carbono carbonílico da señales a frecuencias muy altas (desplazamientos químicos grandes, típicamente entre ≈160–220 ppm según el tipo de carbonilo), alejadas de los picos de carbonos alifáticos.
- Otras técnicas útiles son la espectrometría de masas (fragmentación característica) y la espectroscopía UV–Vis en carbonilos conjugados (absorciones en el UV).
Resumen y notas prácticas
- El carbonilo (C=O) es polar, planario y muy reactivo frente a nucleófilos.
- Su química permite transformar y construir moléculas con gran diversidad funcional —reducción, adición, condensación, entre otras—.
- Su presencia se confirma fácilmente por IR y 13C‑RMN; su comportamiento varía mucho según el entorno químico (conjugación, sustituyentes, presencia de grupos salientes).
En síntesis, el grupo carbonilo es central en la química orgánica y bioquímica: su combinación de polaridad, estabilidad relativa y reactividad controlable lo convierte en una herramienta clave en síntesis, catálisis y diseño de fármacos.