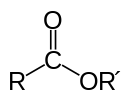
Un éster es un carbonilo con un grupo éter en el átomo de carbono. El grupo puede escribirse como COOR. Se pueden fabricar haciendo reaccionar un ácido carboxílico con un alcohol con algún ácido.
Los ésteres son un grupo funcional muy importante. Pueden encontrarse en muchas sustancias. Son muy comunes en las grasas y los aceites. A veces tienen un olor muy fuerte y agradable. Pueden utilizarse para fabricar perfumes. Los poliésteres se encuentran en los plásticos.
Los ésteres también pueden realizar muchas reacciones. Es muy fácil cambiar la parte de éter de la molécula por otra similar. También es posible reducir el éster a una cetona o a un alcohol, que pueden realizar muchas reacciones diferentes. La adición nucleofílica también es una buena reacción, aunque un poco más difícil que con las cetonas.
Hay muchas formas de averiguar si una molécula tiene un grupo éster. La espectroscopia de infrarrojos da señales muy nítidas, que son diferentes a las de otros carbonilos. La espectroscopia de RMN del carbono tiene características similares.
Estructura y nomenclatura
Un éster tiene la fórmula general R–C(=O)–OR', donde R y R' pueden ser cadenas alquílicas o grupos aromáticos. El carbono carbonílico está deshidratado y enlazado a un átomo de oxígeno que a su vez enlaza a R'. Por resonancia, el grupo carbonilo del éster es polar y presenta una densidad electrónica que condiciona su reactividad.
En la nomenclatura IUPAC, el nombre de un éster se forma indicando primero el grupo alcoxi (R') como sustituyente y luego el nombre del ácido carboxílico correspondiente cambiando la terminación “-ico” por “-ato” (por ejemplo, CH3COOCH2CH3 = etanoato de etilo, conocido también como acetato de etilo).
Síntesis: métodos comunes
- Esterificación de Fischer: reacción reversible entre un ácido carboxílico y un alcohol en presencia de un ácido (por ejemplo, H2SO4) como catalizador. La reacción se desplaza hacia los ésteres si se elimina el agua formada o se usa exceso de uno de los reactivos.
- Transesterificación: intercambio de grupos alcoxi entre un éster y un alcohol, útil para obtener un nuevo éster o para el refinado de biocombustibles.
- Derivados de ácidos activados: convertir primero el ácido a cloruro de ácido o anhídrido y luego reaccionarlo con un alcohol da ésteres en condiciones más rápidas y a menudo con mejor rendimiento.
Propiedades físicas y olor
Los ésteres alifáticos de bajo peso molecular suelen ser líquidos volátiles con olores frutales agradables (por ejemplo, acetato de etilo, butirato de metilo) y por ello se usan en sabores y perfumes. Aumentando la masa molar, los ésteres tienen puntos de ebullición mayores, pero en general son menos polares que los ácidos carboxílicos y no forman enlaces de hidrógeno intermoleculares tan fuertes, por lo que su solubilidad en agua disminuye con el alargamiento de la cadena.
Reactividad y transformaciones importantes
Los ésteres participan principalmente en reacciones de sustitución nucleofílica en el carbono carbonílico (mecanismo de acilo). Algunas transformaciones relevantes:
- Hidrólisis: en medio ácido la hidrólisis es reversible (regresa al ácido y alcohol), mientras que en medio básico (saponificación) es prácticamente irreversible y produce la sal del ácido y el alcohol.
- Reducciones: con LiAlH4 un éster se reduce a dos alcoholes (reducción completa a alcohol primario). La reducción parcial a aldehído puede conseguirse con DIBAL-H a baja temperatura. Para obtener cetonas a partir de ésteres se usan rutas específicas, por ejemplo reacción con reactivos organometálicos o conversión previa a derivados más reactivos.
- Transesterificación y intercambios son fáciles y se emplean industrialmente (síntesis de biodiésel, modificación de polímeros).
- Condensaciones: algunos ésteres en presencia de bases pueden sufrir condensaciones tipo Claisen formando β‑cetoésteres, útiles en síntesis orgánica.
Identificación por espectroscopía
Los ésteres presentan señales características fáciles de reconocer:
- Infrarrojo (IR): banda fuerte del grupo carbonilo (C=O) en torno a ~1735–1750 cm−1 para ésteres alifáticos; la frecuencia puede bajar si hay conjugación. Además muestran bandas por estiramiento C–O alrededor de 1050–1300 cm−1.
- RMN 1H: protones en el carbono adyacente al oxígeno (R'–O–CH2–) aparecen típicamente en 3.5–4.5 ppm; otros protones alquílicos en rangos habituales.
- RMN 13C: el carbono carbonílico del éster aparece en una región desblindada, alrededor de 160–185 ppm; los carbonos del grupo O–CH suelen aparecer en 50–80 ppm según sustitución.
Aplicaciones y ejemplos
Algunos usos y ejemplos prácticos:
- Ésteres frutales como el acetato de etilo o el butirato de metilo se usan en aromas y perfumes.
- Los triglicéridos (grasas y aceites) son triésteres de glicerol y ácidos grasos, componentes clave de la bioquímica y la industria alimentaria.
- Los poliésteres (por ejemplo PET) son polímeros formados por unidades éster y se emplean en fibras y envases plásticos.
- Como disolventes, muchos ésteres se usan en procesos industriales y en laboratorio por su capacidad para disolver resinas y polímeros.
Seguridad y manejo
Aunque muchos ésteres de bajo peso son relativamente poco tóxicos, son inflamables y a menudo volátiles; deben manipularse con ventilación adecuada. Algunos ésteres pueden causar irritación o sensibilización cutánea. Para reacciones enzimáticas o biológicas (como las lipasas que hidrolizan ésteres en grasas) se deben considerar las condiciones específicas de pH y temperatura.
En resumen, el grupo funcional éster es central en química orgánica por su presencia en moléculas naturales y sintéticas, su reactividad en sustituciones nucleofílicas y su importancia industrial en sabores, polímeros y disolventes.