La cristalografía de rayos X es una técnica experimental para determinar la estructura tridimensional de una molécula o de un sólido cristalino con precisión atómica. La nube de electrones de los átomos desvía los rayos X y, al registrar cómo se dispersan esos rayos, se puede reconstruir una "imagen" de la distribución electrónica y, por tanto, de la posición de los átomos. Los longitudes de onda de los rayos X son comparables a las distancias interatómicas (≈1 Å), lo que hace la técnica especialmente adecuada para medir distancias y ángulos entre átomos. Aunque en muchos casos la muestra puede recuperarse tras la medida, hay que tener en cuenta que los cristales biológicos son susceptibles a daño por radiación, por lo que hoy en día se usan técnicas como el criocooling o fuentes de rayos X de femtosegundo (XFEL) para minimizar ese efecto.
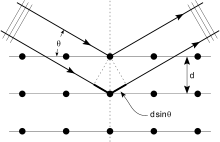
La técnica fue desarrollada de forma decisiva por Sir William Bragg (1862-1942) y su hijo Sir Lawrence Bragg (1890-1971), que formularon la ley de Bragg y aplicaron métodos de difracción para deducir arreglos cristalinos; por esto recibieron el Premio Nobel de Física de 1915. Lawrence Bragg sigue siendo la persona más joven en recibir un premio Nobel por su trabajo. Más adelante, la cristalografía de rayos X fue clave en el descubrimiento de la estructura del ADN en 1953 por James D. Watson, Francis Crick, Maurice Wilkins y Rosalind Franklin, cuando Lawrence Bragg dirigía el Laboratorio Cavendish de la Universidad de Cambridge.
El método más antiguo de cristalografía de rayos X es la difracción de rayos X (DRX): se expone un cristal a un haz de rayos X y la forma en que el haz se dispersa produce un patrón de manchas (reflejos) característico. Esos patrones se analizan para determinar la disposición de los átomos dentro del cristal.
Método y pasos principales
- Preparación y cristalización: para la cristalografía de moléculas pequeñas y macromoléculas (proteínas, ácidos nucleicos) es necesario obtener cristales de calidad adecuada; este paso suele ser el más laborioso.
- Montaje y protección del cristal: el cristal se monta en un soporte (palo o buje) y con frecuencia se congela rápidamente (crioprotección) para reducir el daño por radiación.
- Recogida de datos: se irradia el cristal mientras se rota, y se registran los patrones de difracción con detectores modernos. Hoy se usan fuentes de laboratorio, sincrotrones de alta intensidad y, para casos especiales, fuentes XFEL.
- Procesamiento de datos: indexación de los reflejos, integración y escalado para obtener intensidades y factores estructurales.
- Resolución del problema de fases: las intensidades de difracción no contienen directamente la fase. Para resolverla se emplean métodos como molecular replacement (usando estructuras similares), métodos directos (para moléculas pequeñas), sustitución isomorfa o anomalous dispersion (SAD/MAD).
- Construcción del modelo y refinamiento: se construye un modelo atómico acorde con el mapa de densidad electrónica y se refina iterativamente para ajustarlo a los datos experimentales y a restricciones geométricas.
- Validación y publicación: comprobación de la calidad del modelo (químicamente y según parámetros estadísticos) y depósito en bases de datos públicas (por ejemplo, Protein Data Bank para macromoléculas).
Tipos de cristalografía de rayos X
- Difracción de un solo cristal (single-crystal XRD): proporciona estructuras detalladas y es la técnica preferida para determinación atómica precisa.
- Difracción de polvo (powder XRD): se usa cuando no es posible obtener cristales únicos; es muy útil en mineralogía, química de materiales y control de fase en síntesis.
- Crystallografía seriada y XFEL: permiten estudiar cristales muy pequeños o frágiles y, en el caso de XFEL, "capturar" estructuras antes de que ocurra el daño por radiación (crystallography outrunning damage).
Aplicaciones principales
- Química y cristalografía de pequeñas moléculas: determinación de geometrías, estereoquímica y tautomería.
- Biología estructural: estructuras de proteínas, complejos proteína-ligando y ácidos nucleicos; fundamento del diseño racional de fármacos.
- Ciencia de materiales: estudio de aleaciones, semiconductores, polímeros cristalinos y catalizadores.
- Mineralogía y geología: identificación y caracterización de minerales y fases cristalinas.
- Industria farmacéutica: caracterización de formas cristalinas (polimorfos) que afectan solubilidad y estabilidad del fármaco.
Ventajas y limitaciones
- Ventajas: resolución atómica alta, información detallada sobre posiciones y enlaces, método bien establecido con amplio soporte de software (por ejemplo, SHELX, CCP4, PHENIX).
- Limitaciones: exige cristales de buena calidad para single-crystal XRD; las muestras biológicas pueden sufrir daño por radiación; el problema de fases requiere estrategias específicas; las estructuras cristalinas muestran la conformación en el estado sólido/cristalino, que puede diferir ligeramente de la solución.
Requisitos de la muestra y resolución
- La calidad de los cristales condiciona directamente la resolución: para moléculas pequeñas se alcanzan resoluciones mejores a 1 Å; para macromoléculas, resoluciones comunes son 1.5–3.5 Å. Cuanto menor es el número en Å (Angström), mayor es el detalle observable.
- En powder XRD no se requiere un cristal único, pero la información estructural puede ser menos directa y más dependiente de análisis complementarios.
En resumen, la cristalografía de rayos X es una herramienta central en ciencia y tecnología para conocer estructuras a escala atómica. Su evolución—from técnicas clásicas de laboratorio hasta el uso de sincrotrones y XFELs—ha ampliado su alcance, permitiendo hoy resolver problemas complejos en química, biología, física y ciencia de materiales.