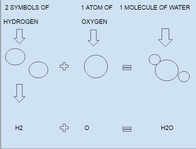
Fórmula química es la forma escrita que usan los químicos para describir la composición de una sustancia. Una fórmula indica qué elementos químicos están presentes y cuántos átomos de cada tipo forman la unidad representada. Dependiendo del tipo de fórmula, también puede dar información sobre cómo se enlazan los átomos o cómo se disponen en el espacio.
Partes y notación básica
Las letras (símbolos) identifican cada elemento químico. Los subíndices colocados después de un símbolo indican el número de átomos de ese elemento en la unidad representada. Por ejemplo:
- El peróxido de hidrógeno se escribe H2O2, lo que significa 2 átomos de hidrógeno y 2 de oxígeno por molécula.
- El metano contiene un átomo de carbono (C) y cuatro de hidrógeno; su fórmula es CH4.
- La glucosa (un tipo de azúcar) tiene seis átomos de carbono, doce de hidrógeno y seis de oxígeno: C6H12O6.
Tipos de fórmulas
Existen varios tipos de fórmulas, cada una útil para diferentes fines:
- Fórmula molecular: indica el número real de átomos de cada elemento en la molécula (ej.: C6H12O6).
- Fórmula empírica: muestra la relación más sencilla entre los átomos (ej.: la glucosa C6H12O6 tiene fórmula empírica CH2O).
- Fórmula estructural: representa cómo se unen los átomos (por ejemplo, mostrando enlaces simples, dobles o la posición de los grupos funcionales). Puede presentarse como fórmulas de Lewis, condensadas o esqueletales.
- Fórmula iónica: indica iones y sus cargas (por ejemplo, Na+, SO42−).
- Fórmulas condensadas y semidesarrolladas: simplifican la estructura mostrando grupos unidos (por ejemplo, CH3CH2OH para etanol).
Convenciones y símbolos adicionales
- El orden de los elementos en una fórmula puede seguir la regla de Hill (C primero, H segundo, luego los demás en orden alfabético) o bien ordenaciones específicas en compuestos iónicos.
- Los coeficientes delante de una fórmula se usan en las ecuaciones químicas para balancear cantidades (ej.: CH4 + 2 O2 → CO2 + 2 H2O).
- Se usan paréntesis para indicar subgrupos repetidos: Ca(OH)2 significa un catión Ca2+ y dos grupos OH−.
- Los puntos (·) indican hidratos o aductos de cristalización, por ejemplo CuSO4·5H2O.
- Las fórmulas pueden incorporar cargas con superíndices (ej.: NH4+).
Ejemplos y significado estructural
Una misma fórmula molecular puede corresponder a varias estructuras diferentes (isómeros). Por ejemplo, C6H12O6 describe moléculas distintas como la glucosa y la fructosa: mismas cantidades de átomos, distinta conexión y propiedades.
En el caso del peróxido de hidrógeno (H2O2), la fórmula simple indica composición, pero la fórmula estructural O–O con sus ángulos y enlaces explica su reactividad (el enlace O–O es relativamente débil). En el metano (CH4), la disposición tetraédrica alrededor del carbono explica su simetría y propiedades físicas.
Uso en reacciones químicas
Las ecuaciones químicas utilizan fórmulas para describir qué sustancias reaccionan y cuáles se forman. Además de las fórmulas, las ecuaciones incluyen coeficientes estequiométricos, estados de agregación y a veces condiciones (temperatura, catalizadores). Las fórmulas ayudan a calcular masas, concentraciones y rendimientos en laboratorio e industria.
El sistema moderno de escritura de fórmulas fue desarrollado en gran parte por el químico sueco del siglo XIX Jöns Jacob Berzelius elaboró, que introdujo los símbolos de los elementos y la notación con subíndices que hoy usamos.