Introducción
La cinética química trata sobre la velocidad de las reacciones químicas y cómo evoluciona la concentración de reactivos y productos con el tiempo. No debe confundirse con la termodinámica: mientras la termodinámica indica si una reacción es favorable, la cinética explica cuánto tarda en alcanzarse esa transformación. La disciplina combina experimentación y modelos matemáticos para describir y predecir ritmos de reacción en sistemas homogéneos y heterogéneos.
Factores que influyen en la velocidad
Varios parámetros modifican la rapidez con la que ocurre una reacción. Entre los más relevantes se incluyen:
- Temperatura: un aumento de la temperatura suele acelerar las reacciones al incrementar la energía cinética de las partículas; véase también efecto de la temperatura.
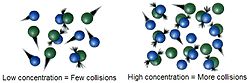
- Concentración: mayores concentraciones de reactivos aumentan la probabilidad de choques efectivos; relacionado con concentración de los reactivos.
- Presión: en gases, elevar la presión equivale a aumentar la concentración, afectando la frecuencia de colisiones (presión).
- Disolvente y entorno: propiedades del medio (polaridad, viscosidad) modifican rutas y velocidades (disolvente).
- Superficie y contacto: en reacciones heterogéneas, el área disponible altera la tasa.
- Presencia de catalizadores: sustancias que aumentan la velocidad sin consumirse, cambiando el mecanismo efectivo.
Leyes de velocidad y orden de reacción
La ley de velocidad es una ecuación empírica que relaciona la velocidad instantánea con las concentraciones de las especies participantes y una constante de velocidad. Por ejemplo, para una reacción A + B → productos, la velocidad puede depender de [A] y [B] mediante exponentes que determinan el orden parcial y el orden global. Estas leyes se obtienen experimentalmente —a menudo por el método de las velocidades iniciales o por integración de las ecuaciones diferenciales— y permiten definir cantidades prácticas como la semivida o la constante de velocidad.
Mecanismos y teorías
Entender el mecanismo implica identificar las etapas elementales que conducen de reactivos a productos. La determinación del mecanismo combina datos cinéticos con técnicas espectroscópicas y, en ocasiones, modelado computacional. Dos marcos teóricos habituales son la teoría de la colisión, que enfatiza choques entre moléculas, y la teoría del estado de transición, que introduce un complejo activado o estado de transición cuya energía de activación controla la probabilidad de reacción. La dependencia de la constante de velocidad con la temperatura suele describirse mediante la ecuación de Arrhenius.
Aplicaciones y métodos experimentales
La cinética es esencial en el diseño de procesos químicos, la síntesis farmacéutica, el control de calidad y la optimización de catalizadores. En laboratorio se emplean técnicas como espectrofotometría, calorimetría, técnicas de flujo detenido (stopped-flow) y análisis por mezclado rápido para medir cambios en milisegundos a horas. Los datos cinéticos informan decisiones sobre escalado, seguridad y eficiencia industrial, y permiten modelar reacciones en atmósfera, agua y sistemas biológicos.
Distinciones y notas relevantes
Además de la distinción con la termodinámica, cabe destacar que un catalizador modifica la velocidad sin alterar la posición del equilibrio; reacciones complejas pueden presentar pasos limitantes que controlan la cinética observada; y en sistemas en superficie o enzimáticos la interpretación requiere modelos específicos. La cinética moderna integra experimentos y simulaciones para proponer y validar mecanismos plausibles, lo que facilita el desarrollo de nuevas tecnologías químicas y farmacéuticas.
En la práctica, recursos y lecturas introductorias ayudan a consolidar conceptos: consulte introducciones que expliquen las velocidades, la influencia de la temperatura y la relación con presión, disolventes, la teoría de las colisiones y las estrategias para esclarecer estados de transición y leyes basadas en concentraciones.