Una cicloadición es una reacción química entre reactivos con dobles enlaces que se sustituyen por una estructura de anillo. Es una reacción química pericíclica en la que "dos o más moléculas insaturadas (o partes de la misma molécula) se combinan con la formación de un aducto cíclico en el que hay una reducción neta de la multiplicidad de enlaces". Se trata de una reacción de ciclización: se forma un nuevo anillo de átomos.
Las cicloadiciones se denominan según el tamaño básico de las moléculas que se unen. De este modo, la reacción de Diels-Alder sería una [4 + 2]cicloadición, y la cicloadición 1,3-dipolar una [3 + 2]cicloadición. Este tipo de reacción es una reacción de adición no polar.
Clasificación y ejemplos comunes
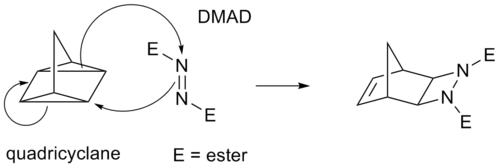
- [4+2] — Diels–Alder: reacción entre un dieno conjugado (4 electrones π) y un dienófilo (2 electrones π) que forma un ciclohexeno o derivados. Muy utilizada en síntesis orgánica por su alta regiocontrol y estereoselectividad.
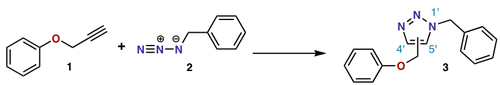
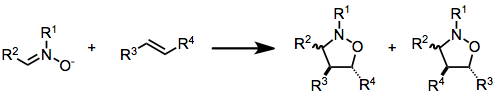
- [3+2] — Cicloadición 1,3-dipolar: reacción entre un dipolo 1,3 (por ejemplo, una azida, óxido nitrógeno o nitrógeno y carbono con carga distribuida) y un dipolarófilo (alqueno o alquino) que forma anillos de cinco miembros. Un ejemplo práctico es la reacción azida–alquino (Huisgen), y su versión catalizada por cobre (click chemistry) que produce 1,2,3-triazoles con alta selectividad.
- [2+2]: forma ciclobutanos. La cicloadición [2+2] es térmicamente prohibida (concertada) por las reglas de conservación de la simetría, pero suele ocurrir bajo irradiación (fotoquímica) o por mecanismos en dos pasos (radicales o iónicos).
- Otras combinaciones: [6+4], [5+2] y otras cicloadiciones más exóticas aparecen en síntesis y en química de materiales.
Mecanismo y teoría de orbitales
Muchas cicloadiciones son reacciones concertadas, es decir, los enlaces se forman y se rompen en un único estado de transición sin intermedios detectables. La explicación moderna se basa en la teoría de orbitales fronterizos (FMO): la interacción favorable entre el HOMO de un reactivo y el LUMO del otro dirige la reactividad, la regioconfiguración y la estereoselectividad.
Las reglas de Woodward–Hoffmann (o reglas de conservación de la simetría) predicen qué procesos concertados son termoquímicamente permitidos o prohibidos, teniendo en cuenta si las interacciones son suprafaciales (misma cara) o antarafaciales (caras opuestas). Por ejemplo, la [4+2]Diels–Alder térmica es suprafacial-suprafacial y está permitida, mientras que la [2+2] concertada térmica está prohibida pero permitida bajo irradiación (fotocatalizada) al cambiar la ocupación electrónica.
Estereo- y regioselectividad
- Estereoespecificidad: en muchas cicloadiciones concertadas la configuración de los reactivos se transmite al producto (p. ej., los sustituyentes cis en un dienófilo permanecen cis en el producto del Diels–Alder).
- Regioselectividad: se predice mediante las interacciones FMO (coeficientes orbitalarios) y por efectos electrostáticos. En Diels–Alder existen reglas empíricas (normalmente el diente más nucleofílico se une al más electrofílico) y a menudo se observa la regla del endo (preferencia por el aducto endo cuando hay grupos aceptores de electrones en el dienófilo, debido a interacciones secundarias en el estado de transición).
Condiciones experimentales y catalizadores
Las cicloadiciones se realizan bajo condiciones térmicas o fotoquímicas según el tipo. Para mejorar rendimiento y selectividad se emplean:
- Ácidos de Lewis (BF3, AlCl3, ZnCl2, etc.) que coordinan al dienófilo y disminuyen su LUMO, acelerando reacciones como el Diels–Alder y a menudo favoreciendo la regla del endo.
- Catalizadores quirales para inducir enantioselectividad en respuestas asimétricas (por ejemplo catalizadores metálicos o organocatalizadores quirales).
- Fotocatálisis para permitir cicloadiciones prohibidas térmicamente (p. ej., [2+2]) o para activar componentes mediante transferencia de energía o electrones.
Mecanismos stepwise y excepciones
No todas las cicloadiciones son estrictamente concertadas: algunas proceden por vías en dos pasos con intermedios radicálicos o iónicos (por ejemplo, ciertas [2+2] térmicas o reacciones en presencia de radicales). La distinción experimental entre mecanismo concertado y paso a paso se realiza mediante estudios cinéticos, isotópicos, y detección de intermedios.
Aplicaciones
- Síntesis de productos naturales y de fármacos: formación eficiente y estereocontrolada de anillos de 5 y 6 miembros.
- Química “click”: la cicloadición 1,3-dipolar azida–alquino (versión catalizada por Cu(I)) es una herramienta valiosa en bioconjugación, materiales y química medicinal.
- Polimerización y materiales: cicloadiciones controladas se usan para obtener redes, monómeros cíclicos y polímeros con propiedades específicas.
Consideraciones prácticas
- Planificar sustituyentes para dirigir regio- y estereoselectividad mediante efectos electrónicos y estéricos.
- Usar catalizadores adecuados (ácidos de Lewis o catalizadores quirales) para mejorar rendimiento y enantioselectividad.
- Evitar condiciones oxidantes o fuentes de radicales si se desea mantener un mecanismo concertado.
Resumen
La cicloadición es una clase central de reacciones en química orgánica que permite construir anillos de manera eficiente y con alto control estereo/regioquímico. Comprender la teoría de orbitales, las reglas de simetría y las condiciones experimentales permite diseñar rutas sintéticas exitosas: desde la clásica reacción de Diels-Alder ([4+2]) hasta las cicloadiciones 1,3-dipolares ([3+2]) y las variantes fotoquímicas ([2+2]).
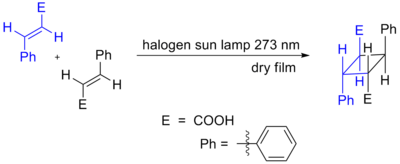
.png)
![Intermolecular Formal [3+3] Cycloaddition Reaction](https://www.alegsaonline.com/image/600px-3+3-cycloaddition.svg.png)