En química orgánica, una reacción pericíclica es un tipo de reacción química entre compuestos orgánicos en la que el estado de transición tiene una geometría cíclica y la transformación progresa de manera concertada (es decir, sin formación de intermedios discretos que puedan detectarse fácilmente). En muchas de estas reacciones se produce una reorganización de enlaces y electrones en un único evento que involucra un anillo de electrones en el estado de transición. Las reacciones pericíclicas suelen ser reacciones de reordenación, y los grupos más importantes son:
- Reacciones electrocíclicas
- Cicloadiciones
- Reacciones sigmatrópicas
- Reacciones de transferencia de grupo
- Reacciones quelotrópicas
- Reacciones diotrópicas
Mecanismo general y características
Las reacciones pericíclicas se caracterizan por:
- Movimiento concertado de electrones: los pares de electrones se reorganizan simultáneamente alrededor de un camino cíclico en el estado de transición.
- Stereospecificidad: el resultado esterequímico (configuración relativa de los sustituyentes) está estrechamente ligado a la geometría del reactivo; por ejemplo, una doble enlace cis/ trans suele dar un producto con estereoisomería definida.
- Dependencia de la simetría molecular: la probabilidad de que una reacción sea favorecida bajo condiciones térmicas o fotocatalíticas está dictada por la conservación de la simetría de las funciones de onda moleculares (reglas de Woodward–Hoffmann).
Reglas de selección: Woodward–Hoffmann y teoría de orbitales fronterizos
Las predicciones sobre si una reacción pericíclica será favorecida térmicamente o por fotones se basan en la conservación de la simetría de los orbitales que participan en el proceso. La teoría de orbitales moleculares frontera (FMO) y las reglas de Woodward–Hoffmann establecen pautas prácticas:
- Para procesos electrocíclicos, la dirección (conrotatoria o disrotatoria) depende del número de electrones π (4n versus 4n+2) y de si la excitación es térmica o fotónica.
- En cicloadiciones, por ejemplo la clásica Diels–Alder ([4+2]), la reacción térmica suprafacial/suprafacial es permitida según las reglas y suele ser concertada y estereospecífica.
- La fotocatálisis puede invertir la preferencia (lo que está prohibido térmicamente puede ser permitido en el estado excitado).
Tipos principales y ejemplos
Reacciones electrocíclicas
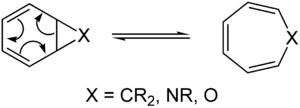
En una reacción electrocíclica se transforma un sistema conjugado abierto en un anillo (o viceversa) por cierre u apertura de un enlace σ. Ejemplos típicos:
- Apertura electróciclica de ciclobutenos a butadienos (térmica: conrotación, fotónica: disrotación en muchos casos).
- Cierre de hexatrienos a ciclohexadienos (dependiendo de 4n o 4n+2 π-electrones se aplica con/dis-rotación).
Cicloadiciones
Las cicloadiciones involucran la formación de dos enlaces σ formando un nuevo anillo. Son muy utilizadas en síntesis:
- Diels–Alder ([4+2]): reacción térmica concertada entre un dieno conjugado y un dienófilo; alto control estereoquímico y amplio uso en síntesis orgánica.
- Cicloadición [2+2]: térmicamente prohibida como proceso suprafacial/suprafacial por las reglas de simetría, aunque puede ocurrir por vía fotoiniciada o mediante rutas paso a paso (radicales) o catálisis metálica.
- 1,3-dipolar cicloadiciones (ej. entre un 1,3-dipolo y un dipolarófilo) forman heterociclos de forma concertada.
Reacciones sigmatrópicas
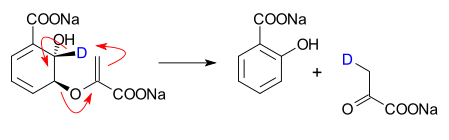
Las reacciones sigmatrópicas implican el desplazamiento de un enlace σ a otra posición a lo largo de un sistema π, acompañadas de la reorganización de los electrones π. Se clasifican por el número de átomos implicados en el movimiento (ej. [1,5]-H, [3,3]-Cope o Claisen):
- Reordenamiento de Cope ([3,3]) y Claisen ([3,3]): reordenamientos sigmatrópicos que conservan la conjugación y presentan alta dependencia estereoquímica.
- Desplazamientos [1,5]-H: importantes en procesos fotoinducidos y en reordenamientos térmicos en algunos sistemas conjugados.
Reacciones de transferencia de grupo, quelotrópicas y diotrópicas
Estos términos abarcan reacciones menos comunes o más específicas:
- Transferencia de grupo: traslado concertado de un átomo o grupo entre posiciones durante un proceso pericíclico.
- Reacciones quelotrópicas: implican el cierre o apertura que afecta a un único átomo que forma y rompe enlaces simultáneamente con varios centros.
- Reacciones diotrópicas: movimientos concertados en los que dos enlaces se forman/rompen de forma sincronizada en un anillo de transición.
Termodinámica, cinética y reversibilidad
En general, las reacciones pericíclicas son procesos reversibles y su posición de equilibrio depende de la diferencia de energía entre reactivos y productos. Como se menciona en el texto original, es posible empujar la reacción en una dirección si el producto es significativamente más estable aplicando el principio de Le Chatelier a un sistema unimolecular. Por otro lado, la velocidad y la ruta pueden alterarse por temperatura, luz o presencia de catalizadores.
Influencia de radicales, metales y rutas no concertadas
Muchas reacciones pericíclicas tienen rutas competidoras o análogas que transcurren por intermediarios radicalarios o iónicos. Los químicos a veces discrepan sobre si un proceso concreto es estrictamente pericíclico. Por ejemplo, la naturaleza concertada de la cicloadición [2+2] depende del sistema: térmicamente está prohibida como proceso suprafacial/suprafacial, pero puede ocurrir por fotodisparo o mediante intermediarios radicales. Asimismo, muchas transformaciones similares pueden catalizarse con catalizadores metálicos; en esos casos el metal suele estabilizar intermedios y la reacción ya no es estrictamente concertada (pierde la característica pericíclica pura).
Evidencia experimental y estudio
La identificación de mecanismos pericíclicos se apoya en:
- Estudios de estereoquímica de productos (conservación o inversión de configuración)
- Experimentos con isotopos (trazado de átomos desplazados)
- Captura de intermediarios cuando existen rutas paso a paso
- Espectroscopía ultrarrápida y cálculos teóricos (QM/DFT) que caracterizan estados de transición y superficies de energía potencial
Aplicaciones y ejemplos notables
Las reacciones pericíclicas son pilares en la síntesis de compuestos complejos, incluidos productos naturales, fármacos y polímeros. El ejemplo clásico de la Diels–Alder aparece en numerosas rutas sintéticas por su alta selectividad. En el texto original se menciona un caso histórico: Se utilizó un gran desplazamiento sigmatrópico de hidrógeno fotoinducido en una síntesis de corrina realizada por Albert Eschenmoser que contenía un sistema 16π, lo que ilustra cómo reordenamientos pericíclicos fotoinducidos pueden ser útiles en síntesis compleja.
Retropericíclicas
Debido al principio de reversibilidad microscópica, existe un conjunto paralelo de reacciones pericíclicas "retro" que realizan la reacción inversa. Muchas transformaciones sintéticas sacan partido de esta reversibilidad para equilibrar rutas o para activar procesos reversibles en fases posteriores de síntesis.
Resumen y consideraciones prácticas
En resumen, las reacciones pericíclicas son reacciones concertadas con un estado de transición cíclico y reglas de selección basadas en la simetría de orbitales. Son estereoespecíficas y de amplio uso en síntesis, aunque en la práctica pueden coexistir rutas no concertadas mediadas por radicales, cationes o metales. La comprensión de sus reglas (Woodward–Hoffmann, FMO) y de las condiciones (térmico vs fotoquímico) es esencial para predecir productos y diseñar rutas sintéticas eficientes.
Muchas reacciones pericíclicas tienen procesos radicales escalonados similares relacionados con ellas. Los químicos no se ponen de acuerdo sobre si algunas reacciones son pericíclicas. Por ejemplo, no se sabe definitivamente si el mecanismo de la cicloadición [2+2] es concertado (o puede depender del sistema reactivo). Muchas reacciones pericíclicas tienen reacciones similares catalizadas por metales. Pero estas reacciones catalizadas por metales tampoco son realmente pericíclicas. Los catalizadores metálicos estabilizan los intermedios de la reacción. Así que la reacción no es concertada, sino estabilizada por metales.