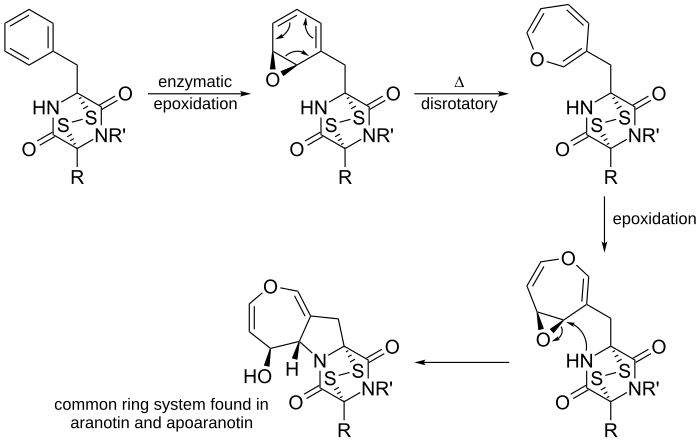
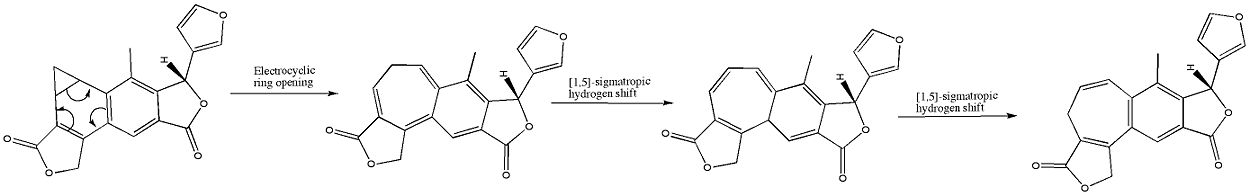
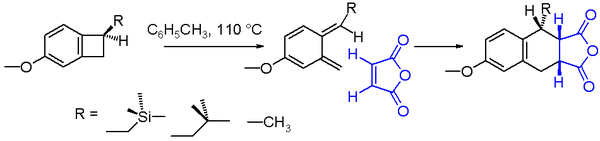
En química orgánica, una reacción electrocíclica es un tipo de reacción de reordenación pericíclica. La reacción se considera electrocíclica cuando el resultado neto es la conversión de un enlace pi que se convierte en un enlace sigma, o viceversa (un enlace sigma que se convierte en un enlace pi). Las reacciones electrocíclicas son procesos concertados que implican la reorganización simultánea de enlaces a lo largo de un sistema conjugado.
Propiedades generales
- las reacciones electrocíclicas son impulsadas por la luz (fotoinducidas) o el calor (térmicas)
- el modo de reacción está determinado por el número de electrones pi en la parte con más enlaces pi
- una reacción electrocíclica puede cerrar un anillo (electrociclización) o abrir un anillo
- la estereoespecificidad está determinada por la formación de un estado de transición conrotatorio o disrotatorio, tal y como predicen las reglas de Woodward-Hoffmann.
Mecanismo y explicación orbital (método del orbital frontera)
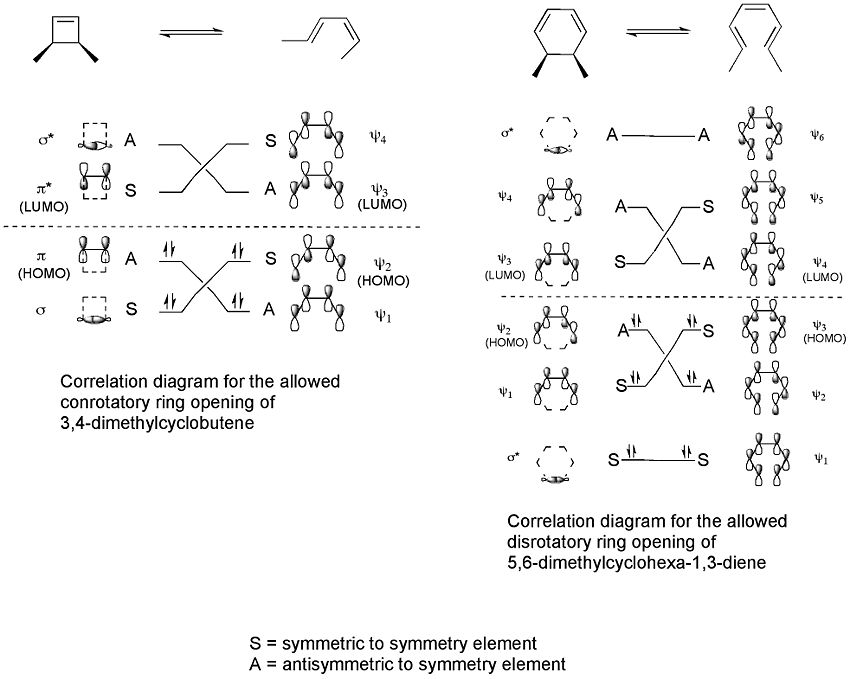
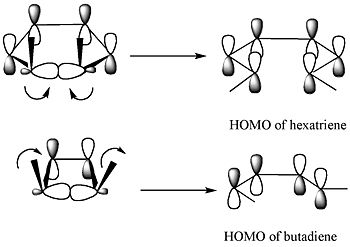
El mecanismo de una reacción electrocíclica se entiende mejor mediante la teoría de orbitales moleculares y el método del orbital frontera: el comportamiento viene dictado por la simetría del orbital molecular de mayor ocupación (HOMO) del sistema conjugado. Durante la apertura o cierre anular, los orbitales p implicados deben enlazarse o desapelazarse de forma que se conserve la simetría orbital a lo largo del proceso. Si la orientación relativa de los lóbulos terminales del HOMO es compatible con la formación del nuevo enlace, la reacción es "permitida" (rápida) bajo las condiciones dadas; si no es compatible, la reacción está "prohibida" por conservación de la simetría y requerirá más energía o vías alternativas.
En la práctica esto se traduce en dos modos de movimiento de los extremos del sistema conjugado:
- Conrotatorio: ambos extremos giran en la misma dirección (ambos en sentido horario o ambos en sentido antihorario).
- Disrotatorio: los extremos giran en direcciones opuestas (uno hacia dentro y otro hacia fuera, o viceversa).
La elección entre conrotatorio y disrotatorio depende del número de electrones pi involucrados y de si la reacción es térmica o fotoinducida, según las reglas de Woodward-Hoffmann descritas más abajo.
Reglas de Woodward–Hoffmann (resumen práctico)
Las reglas de Woodward-Hoffmann aplicadas a electrocilizaciones se pueden resumir así:
- Para reacciones térmicas:
- si el sistema tiene (4n) π electrones → la reacción será conrotatoria (permitida térmicamente)
- si tiene (4n + 2) π electrones → la reacción será disrotatoria (permitida térmicamente)
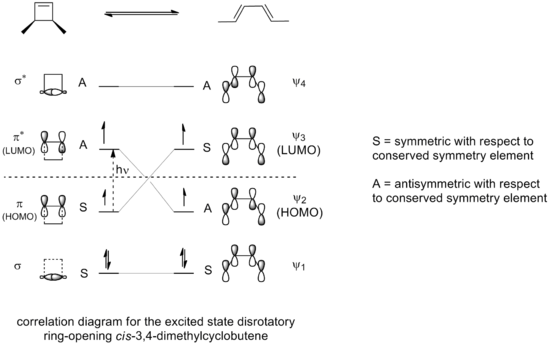
- Para reacciones fotoinducidas (excitación electrónica, inversión de la ocupación orbital):
- si el sistema tiene (4n) π electrones → la reacción será disrotatoria
- si tiene (4n + 2) π electrones → la reacción será conrotatoria
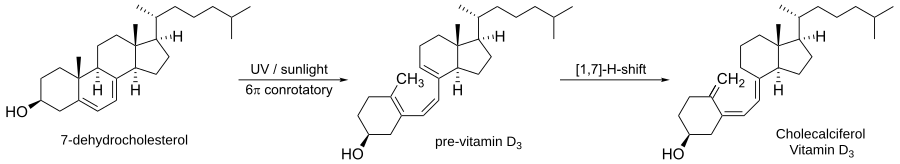
Ejemplos habituales: un sistema de 4 π electrones (como el butadieno/ciclobuteno) sufre una apertura o cierre conrotatorio cuando la reacción es térmica; un sistema de 6 π electrones (como el hexatrieno) cerrará disrotatoriamente en condiciones térmicas.
Estereoespecificidad y torcoselectividad
La estereoespecificidad del producto (configuración relativa de sustituyentes) viene dictada por si el proceso es conrotatorio o disrotatorio: cada modo da una relación geométrica concreta entre los sustituyentes que estaban en los extremos del sistema conjugado.
La torcoselectividad en una reacción electrocíclica se refiere al sentido preferente de rotación de los sustituyentes durante el movimiento conrotatorio/disrotatorio. Por ejemplo, en un proceso conrotatorio los sustituyentes pueden rotar en dos direcciones opuestas; si no existe sesgo, se obtendrá una mezcla de dos productos que son imagen especular (productos enantioméricos). Una reacción torquoselectiva restringe una de estas direcciones (parcial o completamente), produciendo un producto en exceso enantiomérico (un estereoisómero se forma en mayor proporción).
Los factores que generan torcoselectividad incluyen efectos estéricos, interacciones electrónicas (por ejemplo, estabilización de cargas parciales), la presencia de heteroátomos, coordinación a ácidos de Lewis y el uso de catalizadores quirales. En la práctica, la torcoselectividad se aprovecha para obtener productos con elevada enantioselectividad en ciclizaciones electroquímicas o acidificadas.
Ejemplos prácticos
La reacción de ciclización de Nazarov es un ejemplo bien conocido de electrocilización que cierra un anillo. Convierte las divinilcetonas en ciclopentenonas mediante una electrociclización 4π en medio ácido (generalmente pasando por un pentadienilo catiónico). Fue descrita por Ivan Nikolaevich Nazarov (1906–1957) y ha sido ampliamente utilizada y modificado en síntesis orgánica, incluyendo variantes asimétricas con control torcoselectivo mediante catalizadores quirales.
Un ejemplo clásico de apertura anular térmica es la reacción de apertura del anillo del 3,4-dimetilciclobuteno. En condiciones térmicas:
- El isómero cis sólo produce cis,trans-2,4-hexadieno.
- El isómero trans da lugar al dieno trans,trans.
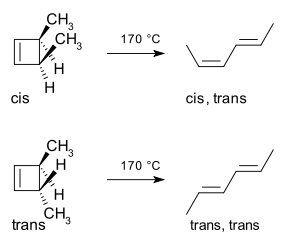
El método del orbital frontera explica este comportamiento: el enlace sigma que se rompe lo hace de forma que los orbitales p resultantes tengan la misma simetría que el HOMO del producto (un butadieno). En el caso térmico del ciclobuteno sustituido, esto sólo puede ocurrir por una apertura anular conrotatoria que deje signos opuestos en los lóbulos terminales implicados; una apertura disrotatoria daría lugar a una combinación de fases que formaría un antienlace y por tanto estaría desaconsejada energéticamente. El siguiente diagrama ilustra ese mecanismo:
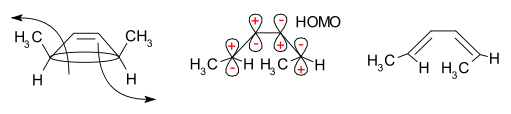
Importancia y aplicaciones
Los químicos se interesan por las reacciones electrocíclicas porque la geometría y la estereoquímica de los productos permiten comprobar predicciones teóricas sobre la conservación de la simetría de los orbitales moleculares hechas por los químicos teóricos. Estas reacciones son herramientas poderosas en síntesis orgánica para construir anillos con control estereoespecífico y para diseñar rutas eficientes a metabolitos naturales y compuestos bioactivos.
Notas finales
En la práctica, muchas electrocilizaciones observadas experimentalmente se ajustan a las reglas de Woodward–Hoffmann, aunque existen excepciones o desviaciones cuando intervienen efectos cinéticos, intermediarios cargados, o mecanismos paso a paso. Por eso, además del análisis orbital, los factores termodinámicos, cinéticos y la presencia de catalizadores deben considerarse al planificar una síntesis basada en una reación electrocíclica.