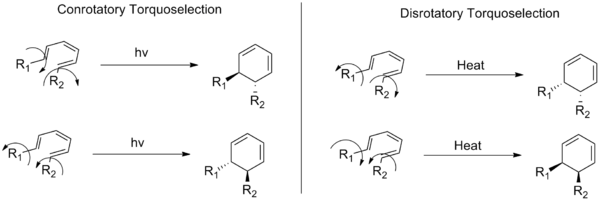
En química orgánica, la torcoselectividad describe las reacciones electrocíclicas que producen un isómero más que otro. Una definición común es «la preferencia por la rotación hacia dentro o hacia fuera de los sustituyentes en reacciones electrocíclicas conrotatorias o disrotatorias». En otras palabras, una reacción es torquoselectiva cuando los grupos unidos a un sistema conjugado (por ejemplo, a un anillo en formación) tienen más probabilidad de girar en una dirección concreta durante el proceso, de modo que un producto (o un enantiómero) se favorece claramente sobre el otro. El término proviene de la imagen mental de un «par de torques» o giros que determinan el resultado esterequímico; el concepto fue desarrollado y popularizado por Kendall N. Houk.
Mecanismo y relación con las reglas de Woodward–Hoffmann
La torquoselectividad se considera una selectividad que va más allá de la distinción básica entre rutas conrotatorias y disrotatorias predichas por las reglas de Woodward–Hoffmann. Es decir, las reglas de simetría orbital indican si una electrociclización es con- o disrotatoria bajo condiciones térmicas o fotocatalíticas, pero no dictan la dirección particular del giro de los sustituyentes. Para entender la torquoselectividad hay que considerar factores energéticos finos: interacciones estéricas, efectos electrónicos (donación o retirada de electrones), estabilización por interacciones orbitales (FMO) y efectos de coordinación con catalizadores. Estos factores sesgan la energía de las trayectorias de giro «hacia dentro» o «hacia fuera», favoreciendo una dirección y, por tanto, un isómero concreto.
Torcoselectividad en cierre y apertura de anillos
Cuando una reacción cierra un anillo, la torquoselectividad coincide frecuentemente con la enantioselectividad: la selección de una dirección de rotación produce preferentemente un único enantiómero del producto ciclado. En un cierre electrocíclico típico, la elección entre modo conrotatorio o disrotatorio puede todavía dar lugar a dos enantiómeros potenciales; la torquoselectividad supone una discriminación entre esos enantiómeros que requiere algún tipo de inducción asimétrica (por ejemplo, un centro quiral cercano o un catalizador quiral).
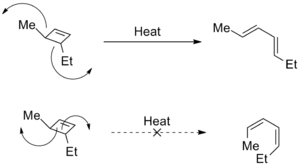
En reacciones electrocíclicas que abren anillos (aperturas electrocícli cas), las distintas direcciones de rotación suelen conducir a isómeros estructurales diferentes (regioisómeros). En estos casos la fuerza motriz suele ser la tensión estérica entre sustituyentes durante la rotación, aunque los efectos electrónicos (grupos donadores vs. retiradores) también pueden invertir o modular la selectividad.
Factores que influyen en la torquoselectividad
- Efectos estéricos: grandes sustituyentes tienden a evitar orientaciones que aumenten el choque estérico durante la rotación, favoreciendo una dirección concreta.
- Efectos electrónicos: grupos donadores o aceptores pueden estabilizar (o desestabilizar) estados de transición particulares por interacciones orbitales, modulando la dirección preferida.
- Coordinación a catalizadores: la complejación con metales o con los catalizadores de ácidos de Lewis quirales puede bloquear una trayectoria y favorecer la otra, además de inducir asimetría.
- Inducción estereoquímica por centros vecinos: un estereocentro próximo actúa como control directo (un caso particular de diastereoselectividad) y puede dictar la dirección del giro.
- Condiciones experimentales: temperatura, disolvente y concentración pueden alterar las barreras relativas de las dos trayectorias y, por tanto, la selectividad observada.
Ejemplos y aplicaciones
Ejemplos clásicos incluyen:
- Electrociclizaciones que generan ciclopentanos o ciclopentenonas mediante la regla de con-/disrotación, donde sustituyentes orientadores producen un enantiómero mayoritario.
- Aperturas de anillos con control torquoselectivo que dirigen la formación de doble enlace hacia un extremo del fragmento abierto, produciendo regioisómeros preferentes.
- Transferencia de quiralidad axial a centros tetraédricos: cuando un fragmento con quiralidad axial (por ejemplo, una allen o un eje biarílico) participa en una transformación electroquímica, esa quiralidad puede transmitirse selectivamente a un nuevo centro quiral en el producto.
Ejemplo ilustrativo: la ciclación de Nazarov de una alenil vinil cetona quiral
Un ejemplo concreto de transferencia de quiralidad axial a tetraédrica es la ciclación torquoselectiva tipo Nazarov de una alenil vinil cetona quiral. En esta reacción, la unidad allenil (con quiralidad axial) controla la dirección preferida de rotación durante la formación del anillo de cinco miembros, de modo que se forma predominantemente un enantiómero de la ciclopentenona resultante. La selectividad se explica por la combinación de efectos estéricos entre sustituyentes axiales y la estabilización electrónica del estado de transición favorecido, y puede mejorarse mediante coordinación a ácidos de Lewis o por diseño del sustituyente en la posición allenil.
Control práctico de la torquoselectividad
Para obtener productos torquoselectivos en síntesis orgánica se emplean varias estrategias prácticas:
- Diseño molecular (control estérico y electrónico de sustituyentes).
- Uso de catalizadores quirales o los catalizadores de ácidos de Lewis quirales, que pueden coordinar y sesgar la trayectoria preferente.
- Introducción de auxiliares quirales o centros estereogénicos vecinos para inducir la dirección de giro por diastereoselectividad.
- Optimización de condiciones (temperatura, disolvente, concentración) para maximizar la diferencia de energía entre las dos trayectorias posibles.
Importancia en síntesis orgánica
La torquoselectividad es una herramienta poderosa para la síntesis de moléculas funcionales y complejas, ya que permite obtener productos con alta enantioselectividad o con regiocontrol sin violar las reglas fundamentales de simetría. Controlar la dirección de rotación en electrociclizaciones abre rutas eficientes hacia anillos funcionalizados, productos naturales y intermediarios sintéticos que requieren una configuración estereoespecífica.
En resumen, la torquoselectividad es una selectividad fina —basada en efectos estéricos, electrónicos y de coordinación— que determina la dirección de rotación de sustituyentes en procesos electrocíclicos y relacionados, y que los químicos pueden explotar mediante diseño molecular y catalítico para dirigir la formación de isómeros deseados.