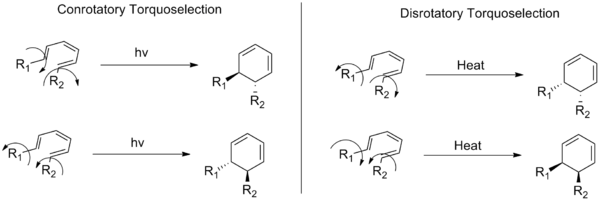
Estos términos describen dos clases de reacciones electrocíclicas (un tipo de reacciones químicas orgánicas). En un modo conrotatorio, los sustituyentes situados en los extremos de un sistema de doble enlace conjugado se mueven en la misma dirección (en el sentido de las agujas del reloj o en sentido contrario) durante la apertura o el cierre del anillo. En un modo disrotatorio, se mueven en direcciones opuestas.
Un ejemplo es la conversión de trans-cis-trans-2,4,6-octatrieno en cis-dimetilciclohexadieno (parte superior de la figura). La mecánica orbital de la reacción necesita un modo disrotatorio. La simetría orbital del orbital molecular de mayor ocupación del octatrieno (HOMO) requiere que los orbitales pi finales se muevan en direcciones opuestas para formar la simetría correcta que se encuentra en el enlace sigma.
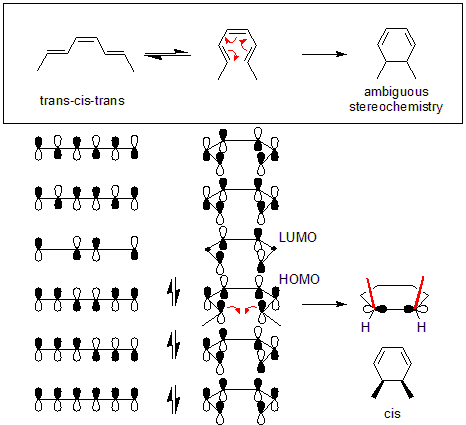
Los reordenamientos térmicos de todos los sistemas conjugados que contienen 4n + 2 electrones pi son estereoespecíficos. Esto se basa en la conservación de la simetría orbital en el orbital molecular más ocupado. Los sistemas que contienen 4n electrones pi muestran el modo conrotatorio opuesto. Esto también es cierto para los reordenamientos de 4n + 2 pi (donde n es un número entero) electrones impulsados por la luz (fotoinducidos). Los reordenamientos fotoinducidos de sistemas de 4n electrones pi (donde el número de electrones es divisible por 4) siguen la regla disrotatoria.
Las reglas de Woodward-Hoffmann resumen las diferentes reacciones anteriores.
La siguiente imagen también muestra la diferencia entre las reacciones conrotatorias y disrotatorias: