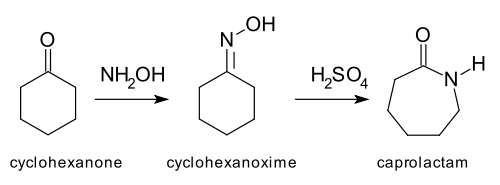
Las reacciones de reordenación son reacciones orgánicas en las que el esqueleto de carbono de una molécula se reordena. El resultado es un isómero estructural de la molécula original. A menudo, un sustituyente se desplaza de un átomo a otro en la misma molécula. En el siguiente ejemplo, el sustituyente R se desplaza del átomo de carbono 1 al átomo de carbono 2:
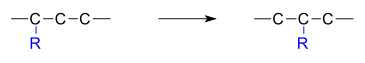
También se producen reordenamientos intermoleculares.
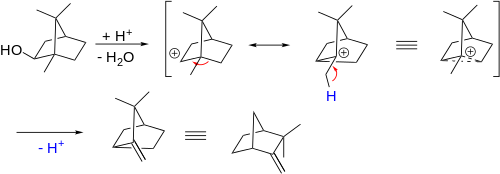
A veces los químicos dibujan diagramas con flechas que muestran cómo se transfieren los electrones entre los enlaces durante una reacción de reordenación. Muchos libros de texto de química orgánica tienen estos diagramas. Pero no cuentan la historia completa del mecanismo de la reacción. El mecanismo real de un reordenamiento con un grupo alquilo en movimiento es que el grupo se deslice suavemente a lo largo de un enlace, no la ruptura y formación de enlaces iónicos. Un ejemplo de esto es el reordenamiento Wagner-Meerwein:
Mecanismos generales
Las reordenaciones pueden ocurrir por varios mecanismos. En términos generales se distinguen dos grandes modos:
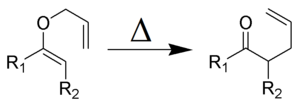
- Mecanismos concertados: El reordenamiento ocurre en un solo paso sin intermediarios cargados claramente definidos. Es típico de las reacciones pericíclicas y de muchos reordenamientos sigmatrópicos (por ejemplo, las reacciones de Cope y Claisen). Aquí las interacciones orbitales y la conservación de la simetría (reglas de Woodward–Hoffmann) determinan la viabilidad y la esterequímica de la reacción.
- Mecanismos paso a paso: Involucran intermedios detectables o al menos conceptuales, como carbocationes, radicales o aniones. Ejemplos clásicos son los desplazamientos 1,2 (hydride shift o alkyl shift) que suelen pasar por carbocationes, o reordenamientos en condiciones ácidas o con catalizadores de Lewis.
Tipos importantes y ejemplos
- 1,2-Reordenamientos
- Desplazamiento de hidruro (hydride shift): movimiento de un H− desde un carbono vecino hacia un carbocatión para formar un carbocatión más estable. Importante en mecanismos de reacciones de sustitución y en rearrangements ácidos.
- Desplazamiento de alquilo (Wagner–Meerwein): migración de un grupo alquilo o arilo para estabilizar un carbocatión. El ejemplo mostrado (isoborneol → camphene) ilustra cómo se reorganiza el esqueleto carbonado en terpenos.
- Pinacol y reordenamiento pinacolítico: conversión de un diol 1,2 a una cetona o aldehído mediante migración de grupo bajo condiciones ácidas.
- Reacciones pericíclicas
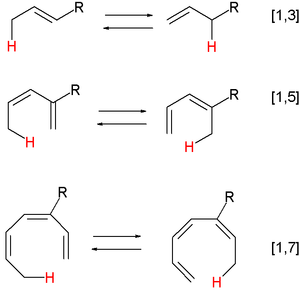
- Sigmatrópicas: reorganizaciones [i,j] donde un fragmento se traslada y los electrones se reorganizan concertadamente (ej.: reordenamiento Cope, Claisen). La estereoquímica (suprafacial vs antarafacial) está controlada por la conservación de la simetría orbital.
- Electrocíclicas y adiciones cicloadiciones: también consideradas pericíclicas cuando implican reordenamientos de enlaces en un anillo conjugado.
- Reordenamiento alílico
- En reacciones alílicas el movimiento de carga/electrones puede generar intermediarios resonantes estabilizados (carbocations o carbaniones alílicos), produciendo isomerización de dobles enlaces o traslados de sustituyentes alílicos.
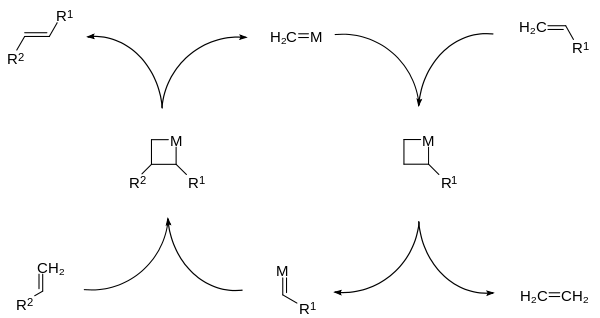
- Metátesis de olefinas
- Reacciones catalizadas por metales (Ru, Mo, W, etc.) donde se intercambian fragmentos alquílicos de dobles uniones mediante intermediarios carbeno-metálicos. El mecanismo de Chauvin (intercambio de fragmentos metal-carbeno) explica la formación de nuevos olefinas a partir de olefinas existentes.
Aspectos cinéticos y termodinámicos
Un reordenamiento está gobernado por la competencia entre la estabilidad del producto y la energía de activación para alcanzar dicho producto. Factores importantes:
- Estabilidad del carbocatión/intermedio: en reordenamientos paso a paso, la migración suele favorecer la formación del intermedio más estable (terciario > secundario > primario).
- Capacidad de migración (migration aptitude): ciertos grupos migran con mayor facilidad (por ejemplo, arilos y grupos con mejor estabilidad de transición migratoria).
- Condiciones y catalizadores: ácidos fuertes, ácidos de Lewis, bases o catalizadores metálicos facilitan o cambian la ruta del reordenamiento.
- Término cinético vs termodinámico: algunos reordenamientos dan productos cinéticos (más rápidos pero menos estables) que pueden isomerizarse a productos termodinámicos más estables si se calienta o cambia condición.
Evidencia experimental y consideraciones mecanísticas
La interpretación de flechas en los diagramas de mecanismos es útil pero puede simplificar en exceso la realidad. Herramientas que confirman mecanismos incluyen:
- Etiquetado isotópico (por ejemplo, 13C o D) para seguir el movimiento de un átomo durante la reacción.
- Estudios cinéticos para determinar órdenes de reacción y detectar intermediarios.
- Espectroscopía (NMR, IR, MS) para identificar intermedios o productos iniciales y finales.
- Computación química para modelar superficies de energía y visualizar transiciones concertadas frente a rutas paso a paso.
Aplicaciones sintéticas y biológicas
Los reordenamientos son herramientas valiosas en síntesis orgánica para remodelar esqueletos carbonados y acceder a estructuras complejas con control estereoquímico. Ejemplos:
- Síntesis de terpenos y alcaloides mediante reordenamientos 1,2 y migraciones intramoleculares (p. ej., Wagner–Meerwein en biosíntesis terpénica).
- Transformaciones en química medicinal para ajustar posiciones de sustituyentes en heterociclos y esqueletos aromáticos.
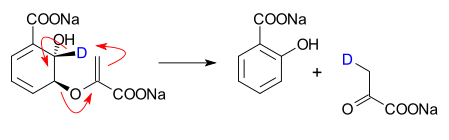
- Reacciones enzimáticas en metabolismos biológicos donde reordenamientos concertados o paso a paso ocurren con alta especificidad —la
mostrada arriba ilustra una conversión biológica (Isochorismate Pyruvate Lyase) que implica reordenamientos enzimáticos específicos.
Consejos prácticos para el laboratorio
- Si se espera un reordenamiento indeseado (p. ej., durante una deshidratación o protodeshalogenación), considere condiciones más suaves, temperaturas bajas o protección del grupo susceptible.
- Para promover un reordenamiento útil, elegir el catalizador adecuado (ácido de Lewis, protónico o catalizador de metales para metátesis) y controlar la concentración y la temperatura.
- Siempre verificar productos potenciales por técnicas analíticas y, si es crítico, usar etiquetado isotópico para confirmar la ruta.
En resumen, las reacciones de reordenación abarcan una familia diversa de procesos —desde movimientos concertados gobernados por simetría orbital hasta migraciones iónicas paso a paso— y son fundamentales tanto en síntesis orgánica como en química bioquímica. Tres reacciones de reordenación importantes son las de 1,2 reordenaciones, las reacciones pericíclicas y la metátesis de olefinas.
.png)