La reacción SN1 es un tipo de reacción de sustitución en química orgánica en la que la sustitución nucleofílica ocurre por un mecanismo de dos pasos. El nombre indica que el paso que controla la velocidad es unimolecular: el paso que determina la velocidad depende de la concentración de una sola molécula del sustrato.
Mecanismo y etapas
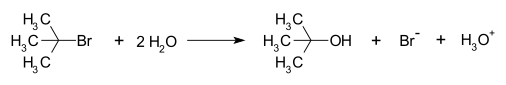
El mecanismo SN1 suele describirse en dos etapas principales:
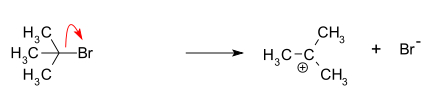
- Ionización: pérdida del grupo saliente para formar un carbocatión. Este intermedio es electrónicamente deficiente y su estabilidad determina en gran medida si la vía SN1 es favorable.
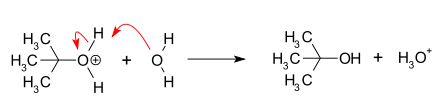
- Ataque del nucleófilo: el nucleófilo reacciona con el carbocatión para formar el producto sustituido; si procede, puede seguir una etapa de desprotonación hasta alcanzar el producto final.
Cinetica y características clave
- La velocidad observada típicamente sigue una ley de primer orden: v = k[sustrato].
- El estado de transición de la etapa lenta es la separación del grupo saliente, no el ataque del nucleófilo.
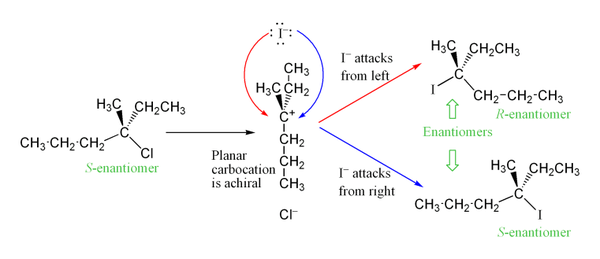
- Debido a la formación de un carbocatión plano, los centros asimétricos formados por SN1 suelen dar lugar a productos racémicos o parcialmente racemizados.
Sustratos y condiciones que favorecen SN1
Algunos factores que favorecen el mecanismo SN1 son:
- Estabilidad del carbocatión: terciario > secundario >> primario.
- Solventes polares próticos, que estabilizan el carbocatión y el grupo saliente.
- Grupos salientes buenos (por ejemplo, haluros) y condiciones que faciliten la ionización.
En la práctica:
- Los haluros de alquilo secundarios o terciarios son sustratos comunes que pueden reaccionar por SN1 cuando la formación del carbocatión está favorecida.
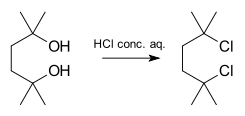
- Los alcoholes secundarios o terciarios a menudo reaccionan por SN1 bajo condiciones ácidas, donde la protonación del hidroxilo convierte al grupo saliente en uno mejor.
- En condiciones básicas fuertes la vía SN1 suele ser menos competitiva frente a mecanismos como SN2 o eliminaciones, salvo en casos particulares donde el carbocatión es especialmente estable.
Comparación con SN2 y otras vías
- En sustratos primarios predomina la reacción SN2, mientras que SN1 es rara en primarios. En casos secundarios la competencia entre ambas vías depende de solvente, nucleófilo y sustituyentes.
- Cuando la ionización es difícil, la reacción puede seguir la vía alternativa SN2 u otros mecanismos como eliminaciones (E1/E2).
Reordenamientos y productos
La formación del carbocatión puede ir seguida de reordenamientos (desplazamientos de hidruro o metilo) que conduzcan a carbocationes más estables y, por tanto, a productos diferentes a los esperados por una simple sustitución directa. Estos reordenamientos son una característica importante a considerar al predecir productos de SN1.
Evidencia experimental
- La observación de racemización parcial o completa en centros quirales es consistente con un carbocatión plano como intermedio.
- Estudios cinéticos que muestran dependencia de primer orden respecto al sustrato apoyan el carácter unimolecular del paso determinante de la velocidad.
Historia
El término y la descripción del mecanismo fueron propuestos por químicos como Christopher Ingold y colaboradores alrededor de 1940, cuando comenzaron a distinguirse los distintos mecanismos de sustitución nucleofílica en función de su cinética y de los intermedios involucrados.