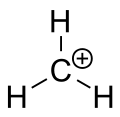
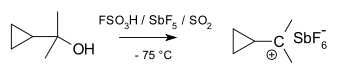
Un carbocatión es un ion con un átomo de carbono cargado positivamente. El átomo de carbono cargado en un carbocatión tiene normalmente un "sexteto" —es decir, sólo dispone de seis electrones en su capa de valencia exterior en lugar de los ocho que marca la regla del octeto. Debido a esa deficiencia electrónica y a la presencia de una carga formal positiva, los carbocationes son especies altamente reactivas y buscan recuperar estabilidad electrónica, por ejemplo mediante ataques nucleofílicos o reordenamientos internos.
Estructura y hibridación
Aunque la lógica elemental podría sugerir que un carbocatión tiene un 3 orbital sp3 vacío que acumula la carga positiva, la evidencia experimental y teórica muestra que la hibridación más consistente con su geometría es 2 sp2. En la práctica, un carbocatión "clásico" presenta:
- Geometría planar trigonal: los tres sustituyentes enlazados al carbono cargado y los orbitales sp2 ocupados están en un mismo plano.
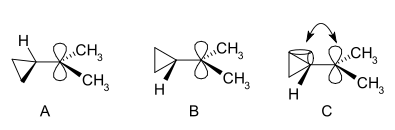
- Orbital p vacío: perpendicular al plano, existe un orbital p no ocupado que contiene la carga positiva parcial y acepta densidad electrónica de nucleófilos o de sustituyentes vecinos (por resonancia o hiperconjugación).
Factores que estabilizan o desestabilizan
La estabilidad relativa de un carbocatión depende de varios efectos que pueden aumentar o disminuir la carga positiva en el carbono:
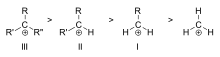
- Hiperconjugación: los enlaces C–H y C–C de los grupos vecinos pueden donar densidad al orbital p vacío, estabilizando el carbocatión. Por eso: terciario > secundario > primario.
- Efecto inductivo: grupos alquilo liberadores de electrones (efecto +I) estabilizan; sustituyentes electronegativos lo desestabilizan.
- Resonancia (mesomería): carbocationes benzílicos o alílicos se estabilizan cuando la carga puede delocalizarse sobre un sistema π (por ejemplo, el carbocatión benzílico o el alílico).
- Solvatación: disolventes polares y nucleófilos (p. ej. agua, alcoholes) estabilizan carbocationes por interacción electrostática y formación de complejos soluto–solvente.
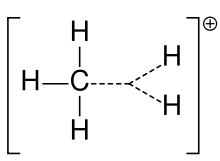
- Carbocationes no clásicos: en algunos sistemas (p. ej. el ion bridgado 2-norbornilio) la carga está deslocalizada sobre varios centros mediante enlaces puente, lo que puede conferir estabilidad o propiedades reactivas atípicas.
Tipos de carbocationes
- Primario, secundario, terciario: según el número de grupos alquilo unidos al carbono cargado; la estabilidad aumenta con el número de grupos alquilo.
- Benzylico y alílico: especialmente estables por resonancia.
- Aromáticos carbocatiónicos especiales: por ejemplo, el catión tropilio (tropylium) es aromático y notablemente estable.
Formación y reactividad típica
Los carbocationes se forman por varios procesos comunes en síntesis orgánica:
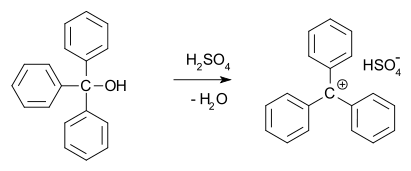
- Heterólisis de enlaces C–X: ruptura heterolítica de un enlace carbono–halógeno o carbono–oxígeno (p. ej. ionización en reacciones SN1 o en solvolisis) genera un carbocatión.
- Protonación de dobles enlaces: al protonar un alqueno se genera un carbocatión intermedio que puede ser capturado por nucleófilos.
- Eliminación y rearrangements: en mecanismos E1 y en muchas reacciones ácido-catalizadas aparecen carbocationes como intermediarios.
Una vez formados, los carbocationes pueden sufrir:
- Ataque nucleofílico: reacción rápida con nucleófilos (iones, solventes, aniones) para formar nuevos enlaces C–X o C–C.
- Eliminación: pérdida de un protón vecino para dar alqueno (E1).
- Reordenamientos (rearrangements): desplazamientos de hidruro o de grupos alquilo hacia el centro carbocatiónico pueden producir carbocationes más estables y explicar productos inesperados en reacciones.
Ejemplos y aplicaciones
Los carbocationes son intermediarios claves en numerosas reacciones orgánicas: reacciones de alquilación (Friedel–Crafts), hidraciones ácido-catalizadas, eliminación E1, y procesos en bioquímica (por ejemplo, algunas enzimas generan intermedios semejantes a carbocationes durante la biosíntesis de terpenos). Además, el estudio de carbocationes ha llevado a la identificación de especies especiales como el catión tropilio y a la caracterización de carbocationes no clásicos.
Detección y vida media
La existencia de carbocationes ha sido confirmada por métodos experimentales como espectroscopía (NMR en matrices frías, espectroscopía ultravioleta), métodos de captura con nucleófilos y técnicas de espectrometría de masas. En solución, su vida media depende de su estabilidad y de las condiciones (disolvente, temperatura, presencia de nucleófilos); muchos son transitorios y reaccionan en tiempos extremadamente cortos, aunque algunos carbocationes estabilizados pueden detectarse y caracterizarse directamente.
Resumen: un carbocatión es un ion carbono con carga positiva, típicamente con hibridación sp2 y un orbital p vacío que favorece una geometría planar trigonal; su reactividad y estabilidad están determinadas por hiperconjugación, efectos inductivos, resonancia y solvatación, y juegan un papel central en multitud de reacciones orgánicas.