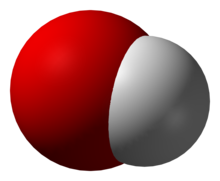
El hidróxido en química es un nombre dado al anión diatómico OH− , formado por átomos de oxígeno e hidrógeno. La mayoría de los compuestos químicos que contienen hidróxidos son bases.
Una base de Arrhenius es una sustancia que, cuando se disuelve en una solución acuosa, produce iones de hidróxido. Por tanto, los iones de hidróxido están muy implicados en las reacciones ácido-base.
Muchas reacciones o procesos químicos útiles implican hidróxido o iones de hidróxido. El hidróxido de sodio se utiliza en la industria como base fuerte, el hidróxido de potasio se utiliza en la agricultura y los minerales de hidróxido de hierro, como la goethita y la limonita, se han utilizado como mineral de hierro. El mineral de aluminio, la bauxita, se compone principalmente de hidróxidos de aluminio.
La mayoría de las sales inorgánicas de hidróxido no se disuelven en el agua.
Propiedades básicas del ion hidróxido (OH−)
Estructura: el ion OH− es diatómico, con un enlace covalente O–H y una carga negativa localizada principalmente en el oxígeno. Presenta pares electrónicos no compartidos que explican su basicidad y su capacidad para actuar como nucleófilo.
Comportamiento ácido-base: en agua existe en equilibrio con los protones según la ionización del agua: H2O ⇌ H+ + OH−. En soluciones acuosas, un aumento de OH− corresponde a una disminución de H+ (pH más alto).
Solubilidad: muchos hidróxidos metálicos son poco solubles en agua. Excepciones importantes son los hidróxidos de los metales alcalinos (por ejemplo, LiOH, NaOH, KOH) que son solubles y funcionan como bases fuertes. Algunos hidróxidos de metales alcalinotérreos (p. ej. Ba(OH)2) tienen solubilidad apreciable, mientras que la mayoría de los hidróxidos de metales de transición son insolubles y precipitan.
Reacciones químicas clave
- Neutralización ácido–base: ácido + hidróxido → sal + agua. Ejemplo: HCl + NaOH → NaCl + H2O.
- Formación de precipitados: iones metálicos con OH− pueden dar hidróxidos sólidos. Ejemplo: Fe3+ + 3 OH− → Fe(OH)3(s).
- Comportamiento anfótero: ciertos hidróxidos (p. ej. Al(OH)3, Zn(OH)2) reaccionan tanto con ácidos como con bases fuertes. Por ejemplo, Al(OH)3 + OH− → [Al(OH)4]− (complejo soluble en medio básico).
- Desprotonación: OH− actúa como base para extraer protones de ácidos más débiles, formando agua.
- Electrólisis en soluciones alcalinas: en la electrólisis del agua en medio básico se genera OH− en el cátodo: 2 H2O + 2 e− → H2 + 2 OH−.
- Saponificación: los hidróxidos fuertes como NaOH reaccionan con ésteres de grasas para producir jabones y glicerol (saponificación de triglicéridos).
Preparación y obtención
Los hidróxidos se obtienen por diversas vías:
- Disolución directa de hidróxidos solubles (NaOH, KOH) en agua.
- Neutralización de una base con una sal soluble o por tratamiento de óxidos con agua: CaO + H2O → Ca(OH)2 (cal hidratada).
- Precipitación a partir de soluciones de sales metálicas añadiendo una base: Mn+ + n OH− → M(OH)n(s).
- Procesos industriales: p. ej. la electrólisis del cloruro de sodio produce NaOH como subproducto en la industria química.
Usos y aplicaciones
- Industria química: NaOH y KOH se usan como reactivos y como bases fuertes en síntesis orgánica e inorgánica.
- Tratamiento de aguas: hidróxidos como Ca(OH)2 se usan para ajustar el pH y como precipitantes de metales pesados.
- Agricultura: KOH tiene aplicaciones en la fabricación de fertilizantes y en procesos de ajuste de pH del suelo.
- Metalurgia y extracción: la bauxita (hidróxidos de aluminio) se procesa mediante métodos que implican álcalis; óxidos e hidróxidos de hierro son importantes como minerales de hierro (goethita, limonita).
- Farmacia y salud: hidróxidos como Mg(OH)2 y Al(OH)3 se emplean como antiácidos.
- Industria alimentaria y doméstica: saponificación (jabones), limpieza (NaOH como desengrasante y limpiador), y conservación de alimentos en algunos procesos.
Aspectos ambientales y de seguridad
Los hidróxidos fuertemente alcalinos (NaOH, KOH) son corrosivos: pueden causar quemaduras en piel y ojos y dañar tejidos. Se deben manejar con protección (guantes, gafas, ventilación). En el medio ambiente, el vertido de álcalis puede elevar el pH local, afectando a organismos acuáticos.
Notas finales
El ion OH− es central en la química ácido–base y en numerosos procesos industriales y biológicos. Aunque muchos hidróxidos son insolubles, su presencia como fases sólidas o como iones en solución determina la reactividad, la solubilidad de metales y el equilibrio ácido-base de los sistemas. Comprender su comportamiento —solubilidad, capacidad de precipitar, reactividad anfótera y alcalinidad— es esencial en química inorgánica, ambiental y tecnológica.