Las enzimas son moléculas proteicas de las células que funcionan como catalizadores biológicos. Las enzimas aceleran las reacciones químicas en el organismo, pero no se agotan en el proceso, por lo que pueden utilizarse una y otra vez.
Casi todas las reacciones bioquímicas de los seres vivos necesitan enzimas. Con una enzima, las reacciones químicas van mucho más rápido de lo que irían sin ella.p39Otros biocatalizadores son las moléculas de ARN catalítico, llamadas ribozimas.
Las sustancias que se encuentran al principio de una reacción se denominan sustratos. Las sustancias que se encuentran al final de una reacción son los productos. Las enzimas actúan sobre los sustratos y los convierten en productos. El estudio de las enzimas se llama enzimología.
La primera enzima fue encontrada en 1833 por Anselme Payen.
Cómo funcionan
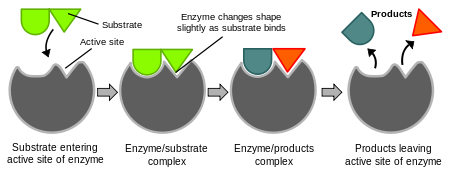
Las enzimas aceleran reacciones químicas disminuyendo la energía de activación necesaria para que la reacción ocurra. Tienen un sitio activo —una cavidad o superficie— donde se une el sustrato. La interacción entre sitio activo y sustrato estabiliza el estado de transición de la reacción.
Modelos que explican la unión: modelo llave-cerradura (el sitio activo encaja con el sustrato) y modelo de ajuste inducido (la enzima cambia ligeramente de forma al unirse al sustrato). Muchas enzimas requieren además cofactores (iones metálicos como Mg2+, Zn2+) o coenzimas (moléculas orgánicas derivadas de vitaminas) para ser activos.
Tipos de enzimas (clasificación general)
Las enzimas se clasifican según el tipo de reacción que catalizan. Una clasificación ampliamente usada distingue seis grupos principales:
- Oxidorreductasas: catalizan transferencias de electrones (p. ej., deshidrogenasas).
- Transferasas: transfieren grupos funcionales entre moléculas (p. ej., quinasas que transfieren grupos fosfato).
- Hidrolasas: rompen enlaces mediante la adición de agua (p. ej., proteasas, amilasas, lipasas).
- Liasas: eliminan grupos para formar dobles enlaces o añaden grupos a dobles enlaces (p. ej., descarboxilasas).
- Isomerasas: catalizan cambios intramoleculares, formando isómeros (p. ej., racemasas).
- Ligasas (sintetasas): unen dos moléculas usando energía (p. ej., DNA ligasa).
Factores que afectan la actividad enzimática
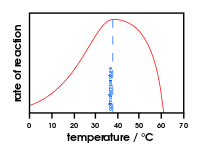
- Temperatura: cada enzima tiene una temperatura óptima; temperaturas elevadas provocan desnaturalización y pérdida de actividad.
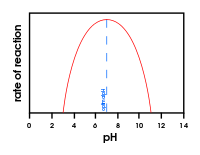
- pH: también hay un pH óptimo; cambios en la acidez afectan la ionización de grupos en el sitio activo.
- Concentración de sustrato: al aumentar, la velocidad de reacción sube hasta alcanzar un máximo (Vmax) cuando la enzima está saturada.
- Inhibidores: pueden reducir o bloquear la actividad. Tipos comunes: inhibición competitiva (el inhibidor compite con el sustrato por el sitio activo) y no competitiva (el inhibidor se une a otro sitio y altera la actividad).
- Activadores: algunas moléculas aumentan la actividad enzimática.
- Ionicidad y presión: cambios en la fuerza iónica y en la presión pueden modificar la estructura y función enzimática.
Regulación de las enzimas
La actividad enzimática se regula por varios mecanismos para asegurar el control metabólico:
- Regulación alostérica: moléculas reguladoras se unen a sitios distintos al activo y modifican la actividad.
- Modificación covalente: por ejemplo, fosforilación/desfosforilación que activa o inactiva la enzima.
- Inhibición por retroalimentación: el producto final de una vía metabólica inhibe una enzima temprana para evitar sobreproducción.
- Activación por proteólisis: muchas enzimas se sintetizan como zimosenos inactivos (p. ej., pepsinógeno → pepsina) y se activan por corte proteolítico.
- Control de la expresión génica: la cantidad de enzima producida puede aumentar o disminuir según las necesidades celulares.
Cinética enzimática (conceptos básicos)
La cinética estudia la velocidad de las reacciones enzimáticas. Un modelo fundamental es la ecuación de Michaelis-Menten, que relaciona la velocidad de reacción con la concentración de sustrato. De ella derivan dos parámetros importantes:
- Vmax: velocidad máxima cuando la enzima está saturada de sustrato.
- Km (constante de Michaelis): concentración de sustrato a la que la velocidad es la mitad de Vmax; indica afinidad relativa entre enzima y sustrato (Km baja = alta afinidad).
Importancia biológica y aplicaciones prácticas
En los seres vivos, las enzimas son esenciales para procesos como la digestión (amilasa, lipasa, proteasas), la producción de energía (ATP sintasa), la replicación y reparación del ADN (DNA polimerasa, ligasa), y la señalización celular (quinasas, fosfatasas).
Aplicaciones en medicina e industria:
- Diagnóstico clínico: niveles de ciertas enzimas en sangre indican daño tisular (p. ej., transaminasas hepáticas).
- Fármacos: muchos medicamentos actúan como inhibidores enzimáticos (p. ej., inhibidores de la enzima convertidora de angiotensina, estatinas que inhiben la HMG-CoA reductasa).
- Biotecnología: la PCR usa Taq polimerasa; enzimas industriales en detergentes, producción de alimentos (quesos, pan), y biocombustibles.
- Medio ambiente: enzimas para biorremediación y degradación de contaminantes.
- Terapias: la terapia de reemplazo enzimático trata ciertas enfermedades lisosomales; además se usan enzimas recombinantes en distintas terapias.
Medición, nomenclatura y ejemplos
La actividad enzimática se mide en unidades (U), donde 1 U suele definirse como la cantidad de enzima que convierte 1 micromol de sustrato por minuto en condiciones específicas. Los nombres de las enzimas suelen acabar en -asa (en español) o -ase (en inglés), p. ej. amilasa, lactasa, ATP sintasa, DNA polimerasa.
Ejemplos representativos: amilasa (rompe almidón), pepsina y tripsina (proteasas digestivas), lactasa (descompone lactosa), ATP sintasa (genera ATP en la cadena respiratoria), Taq polimerasa (reacción en cadena de la polimerasa).
Notas históricas y biocatalizadores no proteicos
Como se menciona, la primera enzima identificada experimentalmente fue descrita por Anselme Payen en 1833 (la diastasa). Además de las enzimas proteicas, existen ribozimas —moléculas de ARN con actividad catalítica— que amplían la noción de catalizadores biológicos y tienen roles importantes, por ejemplo, en el corte y empalme del ARN y en la peptidil transferasa del ribosoma.
En resumen, las enzimas son catalizadores fundamentales para la vida: específicas, regulables y esenciales tanto en procesos celulares como en numerosas aplicaciones biotecnológicas e industriales.