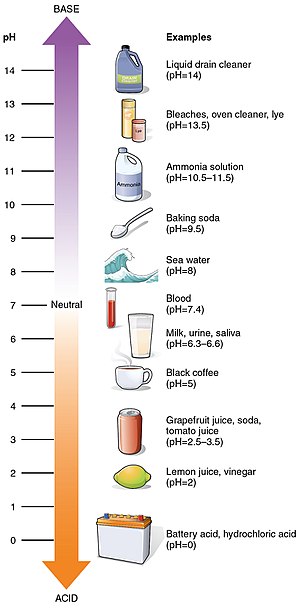
El pH es una escala que cuantifica la acidez o alcalinidad de una solución, normalmente posicionada entre 0 y 14. Indica el grado de acidez o alcalinidad de una sustancia: las soluciones más ácidas tienen un pH más bajo y las más alcalinas un pH más alto. Una solución neutra tiene pH 7. Los ácidos tienen un pH inferior a 7 y los álcalis tienen un pH superior a 7. La escala es logarítmica: un cambio de una unidad de pH representa un cambio de diez veces en la concentración de iones H+. Por ejemplo, una solución con pH 3 tiene diez veces más iones H+ que otra con pH 4.
Algunos ejemplos de pH
- Jugo de limón: pH ≈ 2
- Vinagre: pH ≈ 2–3
- Sangre humana: pH ≈ 7.35–7.45
- Agua de mar: pH ≈ 8.1
- Jabón: pH ≈ 9–11
- Ácidos o bases muy concentrados pueden tener pH < 0 o > 14
S.P.L. Sørensen introdujo este concepto en el año 1909. La p corresponde al alemán potenz, que significa potencia o concentración, y la H al ion hidrógeno (H )+.
Definición matemática
La forma más habitual de definir el pH es mediante el logaritmo negativo de la concentración de iones hidrógeno en la solución:
pH = - log 10 [ H + ] {\displaystyle {\mbox{pH}}=-log _{10}\left[{\mbox{H}^{+}]}
La expresión [H+] indica la concentración de iones H+ (también se escribe [H3O+], la misma concentración de iones de hidronio), medida en moles por litro (también conocida como molaridad).
Sin embargo, la ecuación correcta es en realidad:
pH = - log 10 [ a H + ] {\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{mathrm {H^{+}} }\right]}
donde a H + {{displaystyle a_{mathrm {H^{}} }}
Actividad frente a concentración
La actividad aH+ considera efectos no ideales debidos a la interacción entre iones (fuerza iónica) y difiere de la concentración real [H+]. En soluciones muy diluidas o cuando la precisión no necesita ser extrema, se usa [H+] en lugar de aH+. En análisis más rigurosos (salmuera, soluciones muy concentradas), hay que corregir mediante coeficientes de actividad.
Medición del pH
- Potenciómetro (pH-metro): electrodo de vidrio conectado a un medidor que lee el potencial y lo convierte en pH. Requiere calibración con soluciones tampón (pH conocidos) y cuidado en el mantenimiento del electrodo.
- Indicadores de pH: sustancias que cambian de color en un rango determinado de pH (ej.: tornasol, fenolftaleína). Útiles para aproximaciones y titulaciones.
- Tiras indicadoras (papel pH): sencillas y rápidas para estimar el pH en campo, con resolución limitada.
Relaciones útiles y temperatura
- En agua pura a 25 °C, el producto iónico del agua Kw = [H+][OH-] ≈ 1·10-14, por lo que pH + pOH ≈ 14. Esta relación depende de la temperatura (a temperaturas distintas de 25 °C el valor de Kw cambia).
- Para soluciones amortiguadoras, la ecuación de Henderson–Hasselbalch permite estimar el pH: pH = pKa + log([A-]/[HA]).
Ejemplos de cálculo
- Si [H+] = 1·10-3 mol/L, pH = 3.
- Si [H+] = 1·10-7 mol/L, pH = 7 (solución neutra a 25 °C).
- Si [H+] = 0.01 mol/L = 1·10-2, pH = 2.
Aplicaciones e importancia
El pH es un parámetro crítico en numerosas áreas:
- Biología: el pH influye en la actividad de enzimas y el funcionamiento celular (ej.: el pH sanguíneo debe mantenerse en márgenes estrechos).
- Medio ambiente: la acidez del suelo y del agua afecta la vida acuática y la disponibilidad de nutrientes; la lluvia ácida altera ecosistemas.
- Industria y química: procesos de fabricación, tratamiento de aguas, control de reacciones, y seguridad (sustancias muy ácidas o básicas son corrosivas).
- Alimentación: conservación y preparación de alimentos dependen del pH (fermentaciones, seguridad microbiológica).
La mayoría de las sustancias tienen un pH en el rango de 0 a 14, aunque las sustancias extremadamente ácidas o alcalinas pueden tener un pH < 0, o un pH > 14.
Las sustancias alcalinas tienen, en lugar de iones de hidrógeno, una concentración de iones de hidróxido (OH-), y la relación entre [H+] y [OH-] está dada por Kw.
En resumen, el pH es una medida logarítmica de la acidez o alcalinidad basada en la concentración o actividad de iones H+, con amplio uso práctico en ciencia, salud, industria y medio ambiente.
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)