Tioéster: definición, propiedades y papel en bioquímica y ATP
Tioéster: descubre su estructura, propiedades y papel clave en bioquímica y producción de ATP — reactividad, síntesis y funciones energéticas esenciales.
Tioéster es el nombre que recibe un compuesto con el grupo funcional R–C(=O)–S–R'. Un molécula típica de tioéster se diferencia de un los ésteres porque tiene un átomo de azufre en lugar del átomo de oxígeno que aparece en los ésteres normales. La unidad formal puede describirse como un grupo acilo unido a un tiol (R–C(=O)–S–R'). En síntesis orgánica, los tioésteres pueden obtenerse a partir de ácidos carboxílicos mediante activación del grupo carboxilo y sustitución por un tiol, de modo análogo a la formación de ésteres a partir de un alcohol.
Propiedades químicas
- Reactividad del carbonilo: Debido a que el azufre es menos electronegativo y tiene menos solapamiento p–π con el carbono que el oxígeno, los tioésteres muestran menor estabilización por resonancia del grupo C=O. Esto hace al carbonilo más electrofílico y, en general, los tioésteres son más reactivos hacia ataques nucleófilos que los ésteres y muchas amidas.
- Hidrólisis y energía: La hidrólisis de un tioéster suele ser más exotérmica que la de un éster oxigenado análogo; por eso en bioquímica se aprovecha su mayor energía libre de hidrólisis para impulsar reacciones desfavorables mediante transferencia de acilo.
- Estabilidad: Aunque son más reactivos, muchos tioésteres son lo bastante estables en condiciones no catalíticas; en sistemas biológicos su reactividad se controla por enzimas.
- Espectroscopía: En IR y RMN el grupo carbonilo de un tioéster aparece desplazado respecto al de un éster oxígeno, y la presencia del enlace C–S puede detectarse por bandas características en espectroscopía vibracional.
Síntesis y reactividad típica
- Preparación: Vías comunes incluyen acoplar un ácido carboxílico activado (p. ej. acil cloruro o anhidrido) con un tiol, o usar agentes de acoplamiento como DCC/EEDQ para formar el tioéster directamente desde el ácido y el tiol. También pueden formarse por transesterificación desde ésteres adecuados.
- Reacciones de acilación: Actúan como buenos donadores de acilo en sustituciones nucleofílicas (formación de amidas, ésteres, cetonas a través de acoplamientos cruzados, etc.).
- Aplicaciones en síntesis de péptidos: Los tioésteres de péptidos se utilizan en la ligación química nativa (native chemical ligation) para unir fragmentos peptídicos mediante ataque de un residuo cisteína, permitiendo la síntesis de proteínas completas por métodos químicos.
- Transformaciones especiales: Los tioésteres participan como intermedios en numerosas reacciones orgánicas y en acoplamientos que permiten construir cetonas y otros derivados carbonílicos.
Papel en la bioquímica y relación con el ATP
Los tioésteres desempeñan funciones centrales en el metabolismo. Se forman y utilizan continuamente durante las reacciones que implican transferencia de grupos acilo y en la síntesis y degradación de ácidos grasos.
- Acil‑CoA y transporte de acilos: En las células, muchos acilos se activan como tioésteres con la coenzima A (CoA), formando compuestos como el acetil‑CoA o acil‑CoA. Estos sirven como transportadores de acilo y donantes en multitud de reacciones biosintéticas y catabólicas.
- Acoplamiento energético: La hidrólisis de tioésteres es suficientemente exergónica como para ser aprovechada por rutas metabólicas. Un ejemplo claro es la reacción catalizada por la succinil‑CoA sintetasa en el ciclo del ácido cítrico: la transformación de succinil‑CoA (un tioéster) a succinato permite la formación de GTP o ATP por fosforilación a nivel de sustrato. También, la utilización de acetil‑CoA en el ciclo de Krebs contribuye indirectamente a la producción de ATP a través de la fosforilación oxidativa.
- Donación de grupos acilo: Los tioésteres facilitan la transferencia de grupos acilo en reacciones de biosíntesis (p. ej. elongación de ácidos grasos, biosíntesis de lípidos) y en modificaciones postraduccionales (acetilación de proteínas) debido a su mayor capacidad para ceder el grupo acilo comparado con ésteres oxigenados.
- Intermediarios metabólicos: Por su reactividad controlada mediante enzimas, los tioésteres actúan como intermediarios clave en muchas vías que conducen a la formación o consumo de la energía al cuerpo.
Usos en química y biotecnología
- En química, los tioésteres suelen emplearse como electrófilos versátiles en síntesis orgánica: su mayor reactividad frente a ésteres y amidas facilita muchas transformaciones de acilación selectiva.
- Se usan en la síntesis de péptidos por ligación nativa y en métodos de química para preparar compuestos complejos donde se necesita un donador de acilo reactivo pero controlable.
- En biotecnología, la formación enzimática y la manipulación de tioésteres (p. ej. acil‑CoA) son esenciales para diseñar vías metabólicas y producir compuestos de interés (biocombustibles, lípidos, productos farmacéuticos).
Reactividad comparada y ejemplos de reacciones
- Los tioésteres participan en reacciones de sustitución nucleofílica del carbonilo, y por su mayor electrofilia pueden reaccionar en condiciones más suaves que un éster.
- Pueden participar en reacciones tipo reacciones de aldol cuando se transforman en derivados que generan enolatos, y sirven como precursores para sintetizar cetonas y amidas mediante acoplamientos adecuados.
- En la síntesis orgánica moderna se emplean en acoplamientos y en la formación de enlaces C–C o C–N mediante procedimientos catalíticos o con reactivos nucleófilos selectivos.
En resumen, los tioésteres son compuestos con un balance útil entre estabilidad y reactividad: su menor estabilización por resonancia los hace buenos donadores de acilo y les confiere un papel central tanto en rutas metabólicas (activación y transferencia de acilos, generación indirecta de ATP) como en síntesis orgánica y biotecnológica.
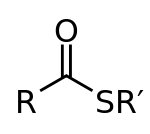
Estructura general de un tioéster
Buscar dentro de la enciclopedia