La epigenética es el estudio de los cambios en la actividad de los genes que no están causados por cambios en la secuencia del ADN. Es el estudio de la expresión de los genes, la forma en que éstos provocan sus efectos fenotípicos.
Estos cambios en la actividad de los genes pueden permanecer durante el resto de la vida de la célula y durar muchas generaciones de células a través de las divisiones celulares. Sin embargo, no hay ningún cambio en la secuencia de ADN subyacente del organismo. En lugar de mutaciones, factores epigenéticos —como la metilación del ADN— hacen que los genes se comporten (se expresen) de forma diferente.
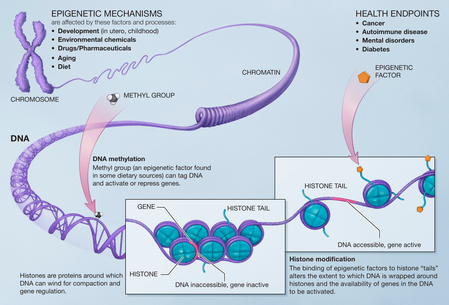
Mecanismos epigenéticos principales
- Metilación del ADN: adición de grupos metilo (–CH3) a citosinas en el ADN, especialmente en regiones CpG. Suele asociarse con la represión de la transcripción.
- Modificaciones de histonas: las histonas (proteínas alrededor de las que se enrolla el ADN) pueden acetilarse, metilarse, fosforilarse, entre otras modificaciones. Estas marcas modulan la estructura de la cromatina y la accesibilidad del ADN.
- Remodelado de la cromatina: complejos proteicos que mueven o reconfiguran los nucleosomas, facilitando o impidiendo el acceso de la maquinaria transcripcional.
- ARNs no codificantes: microARNs, lncRNAs y otros ARN reguladores modulan la estabilidad y traducción de ARNm y también participan en la regulación epigenética local de la cromatina.
Herencia epigenética: mitótica y transgeneracional
Cuando un cambio epigenético se transmite durante las divisiones celulares en el organismo, hablamos de herencia mitótica. Esto es común y permite que células diferenciadas mantengan su identidad (por ejemplo, una célula hepática sigue siendo hepática).
La herencia transgeneracional —es decir, la transmisión de marcas epigenéticas a través de la línea germinal a generaciones siguientes— es más limitada. Durante la gametogénesis y el desarrollo embrionario ocurre un amplio reprogramado epigenético que borra la mayor parte de las marcas, aunque algunas (por ejemplo, el imprinting genómico) pueden evitar este borrado. Por eso, aunque hay ejemplos documentados de efectos ambientales que afectan a generaciones siguientes, la persistencia de marcas epigenéticas a largo plazo sigue siendo un área activa de investigación.
Ejemplos y consecuencias
- Imprinting genómico: ciertos genes se expresan solo desde el alelo materno o paterno por marcas epigenéticas específicas.
- Inactivación del cromosoma X: en hembras de mamíferos, uno de los dos cromosomas X se silencia para equilibrar la dosis génica entre sexos.
- Desarrollo y diferenciación: la epigenética dirige programas de expresión génica que permiten la formación de tejidos distintos a partir del mismo genoma.
- Enfermedades: alteraciones epigenéticas están implicadas en cáncer, trastornos metabólicos, enfermedades neurodegenerativas y psiquiátricas.
- Efectos ambientales: dieta, estrés, exposición a tóxicos o fármacos pueden modificar marcas epigenéticas y afectar la salud.
- Modelo del ratón Agouti: un ejemplo clásico donde la metilación del promotor del gen Agouti determina el color y la susceptibilidad a la obesidad; la dieta materna puede cambiar ese patrón.
Cómo se estudia la epigenética
- Secuenciación de bisulfito: para analizar patrones de metilación del ADN a alta resolución.
- ChIP-seq (inmunoprecipitación de cromatina seguida de secuenciación): identifica modificaciones de histonas o factores asociados al ADN.
- ATAC-seq y DNase-seq: miden accesibilidad de la cromatina.
- RNA-seq: evalúa la expresión de ARN codificante y no codificante.
- Arrays de metilación: soluciones de mayor throughput para perfiles de metilación en estudios poblacionales.
Reversibilidad y aplicaciones terapéuticas
Una característica clave de muchas marcas epigenéticas es su reversibilidad. Esto abre la puerta a intervenciones terapéuticas: por ejemplo, inhibidores de metiltransferasas de ADN (DNMT) o de histona deacetilasas (HDAC) se usan en ciertos cánceres. La epigenética también inspira estrategias en medicina personalizada, nutrición y prevención.
Limitaciones y preguntas abiertas
- Determinar cuándo los cambios epigenéticos son causa o consecuencia de una enfermedad sigue siendo difícil.
- La estabilidad y la transmisibilidad a largo plazo de muchas marcas epigenéticas en humanos requieren más evidencia.
- Interacciones complejas entre genética, epigenética y ambiente complican la interpretación de hallazgos.
En resumen, la epigenética describe cómo la información sobre cuándo, dónde y en qué cantidad se expresan los genes puede cambiar sin alterar la secuencia de ADN. Es un campo central para comprender el desarrollo, la adaptación al ambiente y muchas enfermedades, con importantes implicaciones para la investigación biomédica y la salud pública.