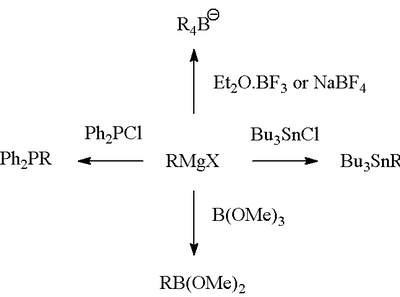
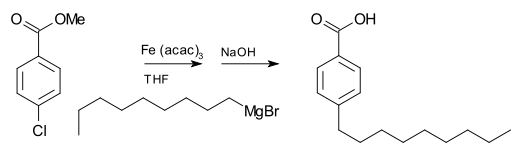
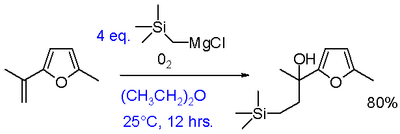
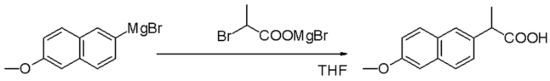
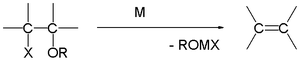
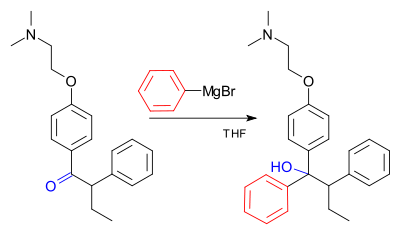
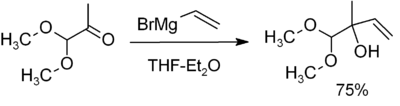La reacción de Grignard (pronunciado /ɡriɲar/) es una reacción química organometálica en la que los haluros de alquilo o arilo‑magnesio (reactivos de Grignard, RMgX) atacan a centros carbonílicos y otros carbonos electrófilos presentes en enlaces polares, formando nuevos enlaces carbono–carbono (y también enlaces carbono–heteroátomo en reacciones específicas). Los reactivos de Grignard actúan como nucleófilos y, tras la adición nucleofílica, el centro carbonílico cambia de hibridación (de sp2 a sp3). Además de la clásica formación de alcoholes, los reactivos de Grignard permiten la introducción de grupos alquilo o arilo en múltiples funciones y la síntesis de una amplia variedad de compuestos orgánicos.
Mecanismo general
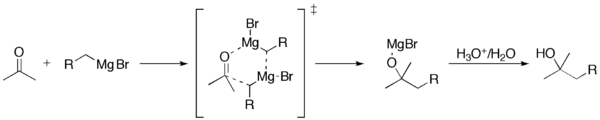
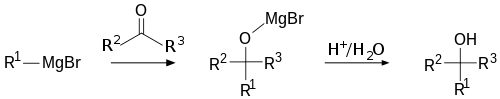
La reacción de Grignard es una adición organometálica nucleófila que suele describirse en dos etapas principales:
- Formación del reactivo de Grignard: inserción del magnesio en el enlace carbono–halógeno del haluro de alquilo o arilo (R–X → RMgX). En solución, el RMgX no existe como un carbanión libre sino como un complejo organomagnesio coordinado por moléculas de éter (por ejemplo, dietil éter o THF): RMgX·(éter)n.
- Adición nucleofílica al electrófilo (p. ej., un carbonilo): el grupo R ataca al carbono electrófilo formando un alcóxido organomagnesiano; tras el trabajo de limpieza (protonación o hidrólisis), se obtiene el alcohol correspondiente.
La alta basicidad del fragmento R (equivalente a la base conjugada de un alcano con pKa ≈ 45–50) explica su gran reactividad frente a protones ácidos y hace que su protonación sea prácticamente irreversible. Conviene señalar que en solución pueden existir equilibrios de agregación (por ejemplo, la Schlenk equilibrium: 2 RMgX ⇌ R2Mg + MgX2) que influyen en la reactividad.
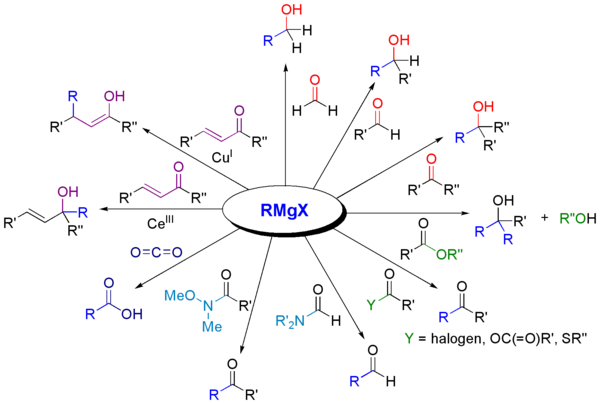
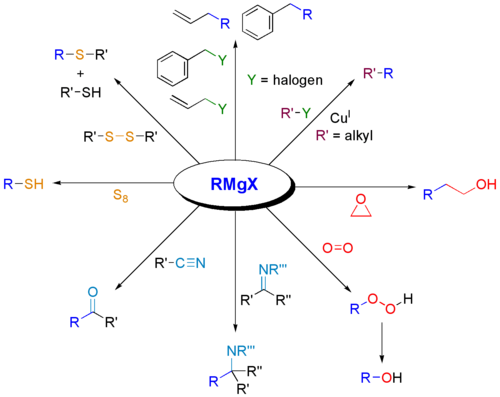
Tipos de reacciones y productos típicos
- Aldehídos y cetonas → alcoholes: con formaldehído se obtienen alcoholes primarios; con otros aldehídos, alcoholes secundarios; con cetonas, alcoholes terciarios (previa protonación del alcóxido).
- Ésteres y haluros acílicos → alcoholes terciarios: suelen requerir 2 equivalentes de RMgX (el primero forma una cetona intermedia que reacciona de nuevo con RMgX).
- Carboxilación (CO2) → ácidos carboxílicos: reacción útil para convertir R en ácido carboxílico tras posterior hidrólisis ácida.
- Apertura de epóxidos → alcoholes con nueva cadena: el ataque ocurre en el carbono menos sustituido (condiciones típicas) y produce alcoholes con elongación de cadena.
- Nitrilos → cetonas: adición a nitrilos seguida de hidrólisis da como resultado una cetona tras trabajo posterior.
- Transmetilación y formación de compuestos organometálicos: RMgX puede transmetalarse a otros metales (Cu, Zn, etc.) para obtener reactivos con selectividad mejorada (por ejemplo, reactivos de Gilman para acoplamientos).
Preparación y condiciones experimentales
Los reactivos de Grignard se preparan típicamente haciendo reaccionar un haluro de alquilo o arilo (R–X) con magnesio metálico en un éter (dietil éter o tetrahidrofurano, THF), que coordina y estabiliza al magnesio. Para obtener buenos rendimientos es crucial:
- Trabajar en atmósfera inerte (N2 o Ar) y con vidrio seco: los reactivos son muy sensibles al agua y otros protones.
- Eliminar humedad de los recipientes (técnicas como secado a la llama) y, a veces, activar la superficie del magnesio (añadiendo yodo, 1,2‑dibromoetano, o usando ultrasonidos o magnesio activado tipo Rieke) para iniciar la reacción.
- Usar solventes éteres apirogénicos que coordinen el Mg y estabilicen el complejo (diésteres no son adecuados: deben ser éteres como dietil éter o THF).
- Controlar la temperatura y agregar los reactivos de forma que no se produzcan reacciones violentas o acoplamientos indeseados.
Limitaciones y selectividad
Hay que tener en cuenta varias limitaciones prácticas:
- Los reactivos de Grignard reaccionan inmediatamente con disolventes próticos (agua, alcoholes, aminas) y con grupos funcionales ácidos (–OH, –NH, –CO2H), por lo que estos grupos deben estar protegidos o ausentes.
- La humedad atmosférica afecta el rendimiento en la preparación de RMgX a partir de magnesio y R–X; por ello se emplean técnicas de manejo anhidro.
- Los haluros de alquilo no siempre reaccionan bien con RMgX por un mecanismo SN2: mecanismo SN 2. En muchos casos ocurren transferencias de un electrón o acoplamientos (reacciones tipo Wurtz), de modo que para ciertos acoplamientos se prefieren reactivos cupratos u otros métodos.
- La presencia de heteroátomos vecinos o grupos electronegativos puede inhibir la formación del reactivo o cambiar su reactividad.
Mecanismos alternativos y equilibrio de Schlenk
En solución los organomagnesianos pueden existir como dimeros y agregados coordinados por éter; además se establecen equilibrios (Schlenk) que afectan la disponibilidad de R– como nucleófilo frente a la formación de R2Mg o MgX2. En reacciones con haluros de alquilo, la sustitución bimolecular directa suele ser poco favorable; en su lugar pueden darse procesos de transferencia de un electrón único y rutas radicalarias.
Aplicaciones en síntesis orgánica
Los reactivos de Grignard son herramientas esenciales en síntesis orgánica para:
- Construcción de enlaces C–C en síntesis de fármacos, fragancias y productos naturales.
- Formación de precursores funcionalizados (alcoholes, ácidos, cetonas) mediante adiciones a carbonilos o carboxilación.
- Transmetilación y preparación de reactivos para acoplamientos cruzados y otros procedimientos organometálicos.
Trabajo posterior y seguridad
Tras completar la etapa de adición, la reacción se "traba" o se hidroliza cuidadosamente (por ejemplo, con agua o una solución ácida diluida) para protonar el alcóxido y obtener el alcohol correspondiente. La adición de agua o ácido debe realizarse lentamente y a temperaturas controladas debido a la liberación de calor y la posible formación de gases o reacciones violentas.
Precauciones de seguridad: los solventes éter son inflamables y pueden formar peróxidos; los reactivos de Grignard reaccionan violentamente con agua y ácidos y deben manipularse bajo atmósfera inerte y con equipo de protección adecuado. Los procedimientos deben ser llevados a cabo por personal formado y en campanas extractoras apropiadas.
Historia
François Auguste Victor Grignard descubrió estos reactivos y sus reacciones. Llevan el nombre de este químico francés (Universidad de Nancy, Francia), quien recibió el Premio Nobel de Química en 1912 por este trabajo. Desde entonces la reacción de Grignard ha sido una piedra angular de la química orgánica sintética.