La química organometálica es el estudio de los compuestos químicos que contienen enlaces entre el carbono y un metal. Combina aspectos de la química inorgánica (el estudio de los enlaces no carbónicos) y de la química orgánica (el estudio de los enlaces carbónicos). Este campo abarca desde especies con enlaces muy covalentes hasta compuestos con carácter iónico o con enlaces de tipo η (hapto), e incluye tanto metales de transición como metales alcalinos y metaloides.
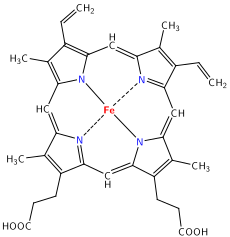
Algunos ejemplos de compuestos organometálicos son el tetraetilo de plomo, que se utilizaba como aditivo para el combustible (gasolina con plomo) en el pasado. También la metilcobalamina (vitamina B12) es un compuesto organometálico común. Además de estos, entre los organometálicos de importancia práctica y teórica se encuentran los reactivos de Grignard (RMgX), el ferroceno (Fe(C5H5)2) y complejos de paladio usados en reacciones de acoplamiento cruzado.
Tipos de enlaces y conceptos clave
Los enlaces metal‑carbono pueden clasificarse según su naturaleza:
- Enlaces covalentes polares: comunes en metales de transición y en compuestos orgánicos con electronegatividades moderadas.
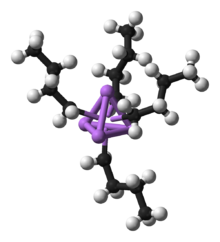
- Enlaces iónicos o carbaniónicos: característicos de compuestos de metales alcalinos o alcalinotérreos (por ejemplo, organolitio y organomagnesio), donde el carbono tiene carácter nucleófilo fuerte.
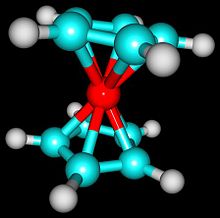
- Enlaces η (hapto): cuando un ligando π (como un anillo de ciclo‑pentadienilo o etileno) se coordina al metal usando varios átomos de carbono simultáneamente (p. ej., ferroceno, complejos η5‑C5H5).
Otros conceptos importantes incluyen la regla de los 18 electrones (que ayuda a predecir estabilidad electrónica), el conteo de electrones, la haptiticidad (η^n) y la influencia de ligandos π‑donadores o π‑aceptores en la reactividad.
Reacciones y mecanismos típicos
Muchos procesos en química organometálica se describen mediante pasos fundamentales:
- Adición oxidativa: el metal aumenta su estado de oxidación al formar dos nuevos enlaces (p. ej., R–X → M–R y M–X).
- Eliminación reductiva: paso inverso de la adición oxidativa, liberando un enlace carbono‑carbono o carbono‑heteroátomo.
- Transmetalación: transferencia de un grupo orgánico entre dos metales (clave en acoplamientos cruzados).
- Inserción migratoria: inserción de un ligando (como CO o un olefino) en un enlace metal‑carbono.
Ejemplos representativos
- Tetraetilo de plomo (Pb(C2H5)4): usado históricamente como aditivo en la gasolina (para el combustible), hoy ampliamente prohibido por su toxicidad.
- Metilcobalamina (vitamina B12): un ejemplo biomédico de complejo con enlace metal‑carbono (vitamina B12).
- Ferroceno (Fe(C5H5)2): compuesto “sandwich” clásico que impulsó avances teóricos y aplicaciones en materiales y catálisis.
- Reactivos de Grignard (RMgX) y organolitios: herramientas fundamentales en síntesis orgánica para formar enlaces carbono‑carbono.
- Cisplatino (Pt(NH3)2Cl2): fármaco anticancerígeno cuya acción está ligada a la química del metal con ligandos orgánicos.
Aplicaciones
- Catálisis homogénea: hidrogenaciones, hidroformilaciones y, especialmente, reacciones de acoplamiento cruzado (Suzuki, Heck, Negishi) que dependen de complejos de paladio y han transformado la síntesis orgánica moderna.
- Catálisis heterogénea y polimerización: catalizadores de Ziegler‑Natta y metallocenos para producir polímeros con control de estereoquímica y peso molecular.
- Materiales y electrónica: compuestos organometálicos como precursores para películas conductoras, OLEDs y materiales magnéticos.
- Medicina: uso de complejos metálicos en fármacos (cisplatino), radiosensibilizadores y en investigación sobre agentes terapéuticos basados en metales.
- Síntesis orgánica: formación selectiva de enlaces C–C y C–heteroátomo, funcionalización dirigida de moléculas complejas.
Seguridad y medio ambiente
Muchos compuestos organometálicos presentan toxicidad y riesgos ambientales. El tetraetilo de plomo es un ejemplo de cómo un aditivo organometálico puede causar daños generalizados, lo que llevó a su prohibición en muchos países. Otros metales (plomo, mercurio, cadmio) y ciertos ligandos orgánicos pueden ser persistentes o bioacumulativos. Por ello, en investigación y en la industria se trabaja en el diseño de catalizadores más eficientes, en la minimización de residuos y en la sustitución por alternativas menos tóxicas.
Breve historia y reconocimientos
El desarrollo de la química organometálica se aceleró en el siglo XX con el descubrimiento de compuestos como el ferroceno y el establecimiento de teoría sobre ligandos π y hapticity. La importancia del campo se refleja en premios Nobel relacionados, por ejemplo, los galardones por descubrimientos en catálisis y acoplamientos cruzados que han revolucionado la síntesis orgánica y la industria química.
En resumen, la química organometálica es un área interdisciplinaria fundamental para la comprensión de la reactividad del carbono unido a metales, con aplicaciones que van desde la síntesis de fármacos hasta la producción de materiales avanzados y la catálisis industrial. Su estudio combina teoría electrónica, diseño de ligandos y consideración de seguridad y sostenibilidad.