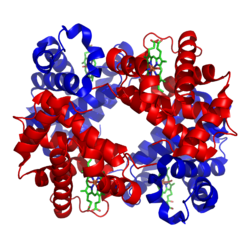
La hemoglobina es una proteína de los glóbulos rojos que contiene hierro. Sirve para transportar el oxígeno por el cuerpo humano. La hemoglobina se encuentra en los glóbulos rojos de todos los vertebrados, salvo los peces de sangre blanca. También se encuentra en algunos invertebrados. Otros invertebrados utilizan otras sustancias químicas como la hemocianina
La hemoglobina participa en el transporte de otros gases. Transporta parte del dióxido de carbono respiratorio del cuerpo (alrededor del 20-25% del total).
Los glóbulos rojos obtienen su color de la hemoglobina, que es roja. Hay millones de moléculas de hemoglobina en cada glóbulo rojo y millones de glóbulos rojos en el cuerpo humano. Cuando la hemoglobina tiene oxígeno unido, se llama oxihemoglobina.
Estructura y composición
La hemoglobina humana adulta típica (llamada HbA) es una proteína tetramérica formada por cuatro cadenas polipeptídicas: dos cadenas alfa y dos cadenas beta. Cada cadena contiene un grupo prostético llamado hemo, que incluye un átomo de hierro ferroso (Fe2+). Es en el hierro del grupo hemo donde se une reversiblemente una molécula de oxígeno (O2).
- Molécula de hemo: porción no proteica que contiene hierro y permite la unión del oxígeno.
- Cadenas globina: determinan las propiedades funcionales y la afinidad por el oxígeno.
Transporte de oxígeno y mecanismos
La hemoglobina permite el transporte eficiente de oxígeno desde los pulmones hasta los tejidos y la devolución del dióxido de carbono hacia los pulmones. Sus propiedades incluyen:
- Cooperatividad: la unión de O2 a una subunidad facilita la unión en las demás, lo que produce una curva de saturación sigmoidea. Esto permite captar O2 con eficiencia en los pulmones y liberarlo en tejidos con menor presión parcial de oxígeno.
- Efecto Bohr: un descenso del pH (o aumento de CO2 y temperatura) reduce la afinidad de la hemoglobina por el oxígeno, favoreciendo su liberación en tejidos metabolmente activos.
- Modulación por 2,3-BPG: el 2,3-bisfosfoglicerato, presente dentro de los glóbulos rojos, disminuye la afinidad por O2 y facilita la entrega de oxígeno a los tejidos.
Transporte de dióxido de carbono y otros roles
El dióxido de carbono (CO2) se transporta en la sangre de tres formas principales:
- Como bicarbonato (HCO3−): la mayor parte, resultado de la reacción catalizada por la anhidrasa carbónica dentro de los glóbulos rojos.
- Carbaminohemoglobina: aproximadamente el 20–25% del CO2 se une directamente a grupos amino de las cadenas globina formando carbaminohemoglobina.
- Disuelto en plasma: una pequeña fracción viaja disuelta en el plasma sanguíneo.
Además, la hemoglobina tiene importancia en el mantenimiento del equilibrio ácido-base y actúa como amortiguador (buffer) en la sangre.
Variantes y formas especiales
- Hemoglobina fetal (HbF): formada por dos cadenas alfa y dos gamma; tiene mayor afinidad por O2 que la HbA, lo que facilita la transferencia de oxígeno de la sangre materna al feto.
- Hemoglobinas anormales: mutaciones en los genes de las globinas producen enfermedades como la anemia de células falciformes (hemoglobina S, HbS) y las talasemias (déficit en la producción de cadenas alfa o beta).
- Methemoglobina: forma en la que el hierro está oxidado a Fe3+ y no puede unir O2 eficazmente; niveles elevados producen hipoxia a pesar de una buena oxigenación.
- Carboxihemoglobina: hemoglobina unida al monóxido de carbono (CO), que tiene una afinidad por la hemoglobina mucho mayor que el O2 y provoca intoxicación por CO.
Importancia clínica
La medición de la hemoglobina es una prueba básica en medicina. Sus alteraciones más importantes incluyen:
- Anemia: niveles bajos de hemoglobina que reducen la capacidad de transporte de oxígeno; causas frecuentes: deficiencia de hierro, pérdidas sanguíneas, enfermedades crónicas, defectos en la síntesis de globina.
- Policitemia: niveles elevados de hemoglobina y de glóbulos rojos, que aumentan la viscosidad sanguínea.
- Enfermedades hereditarias: como la anemia falciforme y las talasemias, que afectan la función y/o la cantidad de hemoglobina.
Métodos de medida y valores habituales
La concentración de hemoglobina en sangre se expresa habitualmente en g/dL. Valores aproximados normales en adultos:
- Hombres: ~13.5–17.5 g/dL
- Mujeres: ~12.0–15.5 g/dL
Las cifras pueden variar según edad, altitud y laboratorio. Herramientas relacionadas: la co-oximetría distingue variantes como carboxihemoglobina y methemoglobina; la oximetría de pulso estima la saturación arterial de oxígeno (SpO2) pero no informa sobre la concentración total de hemoglobina ni sobre algunas formas anómalas.
Nutrientes y prevención
El hierro es esencial para la síntesis de hemoglobina. Una dieta adecuada con fuentes de hierro (carnes, legumbres, vegetales de hoja verde, alimentos fortificados) y, en algunos casos, suplementos, ayuda a prevenir la anemia por déficit de hierro. Ciertas condiciones (pérdidas crónicas de sangre, malabsorción, embarazo) incrementan las necesidades.
Resumen
La hemoglobina es la proteína clave del transporte de oxígeno y de parte del dióxido de carbono en la sangre. Su estructura tetrámera con grupos hemo que contienen hierro permite la unión reversible del oxígeno, y sus propiedades alostéricas (cooperatividad, efecto Bohr, regulación por 2,3-BPG) optimizan el aporte de O2 según las necesidades del organismo. Variantes genéticas y alteraciones adquiridas pueden afectar su función y producir enfermedades con repercusión clínica importante.