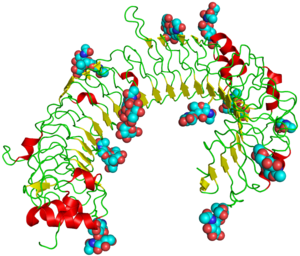
Los receptores tipo Toll (TLR) son proteínas que actúan en el sistema inmunitario innato y en el sistema digestivo. Se extienden por la membrana, es decir, llegan desde el exterior de la célula hasta el interior.
Los TLR reconocen las moléculas procedentes de los microbios. Una vez que los microbios atraviesan las barreras físicas, como la piel o la mucosa del tracto intestinal, son reconocidos por los TLR. Los TLR ponen en marcha una respuesta celular inmunitaria.
La señalización de los TLR conduce a la inducción o supresión de genes que orquestan la respuesta inflamatoria. En total, miles de genes son activados por la señalización de los TLR, y los TLR son uno de los medios más importantes de modulación genética.
También se ha demostrado que los receptores tipo Toll son un importante vínculo entre la inmunidad innata y la adaptativa a través de su presencia en las células dendríticas.
Estructura y localización
Los TLR son receptores tipo transmembrana que comparten tres dominios principales:
- Un dominio extracelular con repeticiones ricas en leucina (LRR) que reconoce ligandos microbianos (PAMPs) y señales de daño (DAMPs).
- Una hélice transmembrana que ancla el receptor en la membrana plasmática o en membranas endosómicas.
- Un dominio intracelular TIR (Toll/IL-1 receptor) que inicia la señalización intracelular al reclutar adaptadores.
En mamíferos, algunos TLR están en la superficie celular (por ejemplo, TLR1, TLR2, TLR4, TLR5, TLR6) y otros en compartimentos endosómicos (por ejemplo, TLR3, TLR7, TLR8, TLR9), lo que facilita el reconocimiento de distintos tipos de patógenos (bacterias, virus, hongos, parásitos) según su localización.
Qué reconocen (ligandos)
Cada TLR se especializa en reconocer patrones moleculares conservados. Algunos ejemplos importantes:
- TLR4: lipopolisacárido (LPS) de bacterias Gram-negativas (cooperación con MD-2 y CD14).
- TLR2 (en heterodímero con TLR1 o TLR6): lipoproteínas/lipopéptidos bacterianos y componentes de hongos.
- TLR5: flagelina (proteína de flagelos bacterianos).
- TLR3: ARN doble cadena (dsRNA), típico de algunos virus.
- TLR7 y TLR8: ARN monocatenario (ssRNA) viral o metabólicos.
- TLR9: ADN desmetilado CpG bacteriano/viral.
Vías de señalización y efectos celulares
Tras la detección de un ligando, los dominios TIR reclutan proteínas adaptadoras que determinan la vía de señalización y la respuesta final:
- MyD88-dependiente: es la vía más común; activa NF-κB y MAP quinasas, conduciendo a la producción de citocinas proinflamatorias (p. ej., TNF-α, IL-6, IL-1β) y quimiocinas.
- TRIF-dependiente: activada por TLR3 y por TLR4 en una vía alternativa; promueve la activación de IRF3/IRF7 y la producción de interferones tipo I (IFN-α/β), importantes contra virus.
- Otras adaptadoras: TIRAP/MAL y TRAM ayudan a reclutar MyD88 o TRIF a receptores específicos.
Estas vías producen cambios rápidos en la expresión génica, inflamación local, maduración de células presentadoras de antígeno y reclutamiento de células inmunes al sitio de infección.
Papel en la inmunidad innata y en la activación de la adaptativa
Los TLR constituyen la primera línea de detección de invasores y promueven respuestas inmediatas (fagocitosis, producción de péptidos antimicrobianos, liberación de citocinas). Además:
- Maduran células dendríticas, incrementan la expresión de moléculas coestimuladoras y favorecen la presentación de antígenos, conectando así la inmunidad innata con la adaptativa.
- Dirigen el tipo de respuesta adaptativa (por ejemplo, respuestas Th1 frente a virus/intracelulares o Th17 frente a hongos/extracelulares) según las señales y citocinas producidas.
Homeostasis intestinal y tolerancia
En el sistema digestivo, los TLR ayudan a distinguir entre patógenos y microbiota comensal. Señalización controlada por TLR contribuye a la barrera epitelial, reparación tisular y tolerancia inmunológica. La desregulación de estas señales puede favorecer inflamación crónica, como en la enfermedad inflamatoria intestinal.
Implicaciones clínicas y terapéuticas
Los TLR están implicados en múltiples condiciones:
- Infecciones: reconocimiento rápido de patógenos; variantes genéticas en TLR o adaptadores pueden modificar susceptibilidad a infecciones o gravedad (p. ej., sepsis).
- Enfermedades autoinmunes e inflamatorias: activación inapropiada o reconocimiento de DAMPs puede contribuir a enfermedades autoinmunes y autoinflamatorias.
- Terapias: agonistas de TLR (p. ej., CpG para TLR9, MPL para TLR4) se usan como adyuvantes en vacunas y en inmunoterapia contra cáncer; antagonistas o moduladores de TLR se investigan para reducir inflamación excesiva en sepsis o enfermedades autoinmunes.
Es importante considerar que la estimulación excesiva de TLR puede conducir a una respuesta inflamatoria sistemática dañina (p. ej., tormenta de citocinas), por lo que las aplicaciones terapéuticas requieren regulación cuidadosa.
Breve nota histórica
Los receptores Toll fueron inicialmente descritos en Drosophila por su papel en el desarrollo embrionario; más tarde se descubrió su función en la defensa inmunitaria innata, lo que llevó al reconocimiento de TLR como componentes esenciales y conservados de la inmunidad en animales.
Resumen
Los TLR son receptores fundamentales del sistema inmunitario innato, especializados en detectar patrones moleculares microbianos y señales de daño, iniciar vías de señalización que regulan la inflamación y la producción de interferones, y coordinar la respuesta adaptativa a través de células presentadoras de antígeno. Su equilibrio es clave para la protección frente a infecciones y para evitar la inflamación crónica.