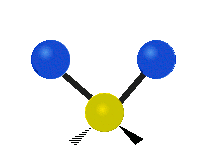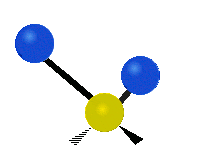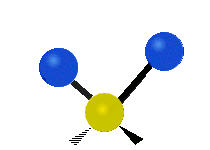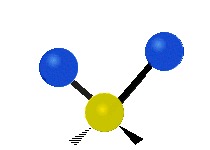
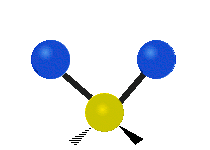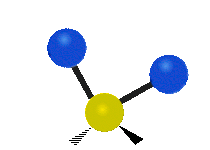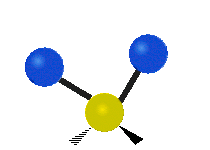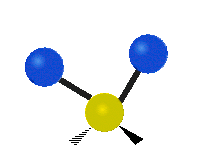
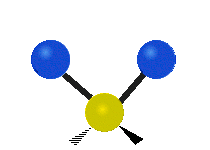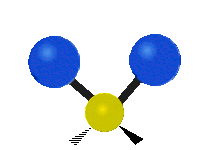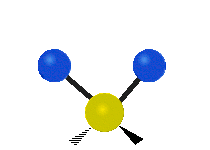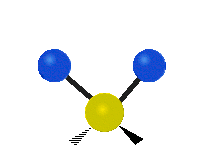
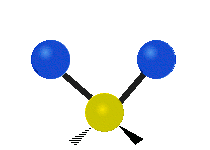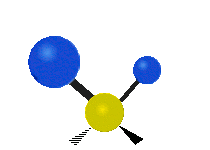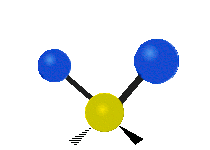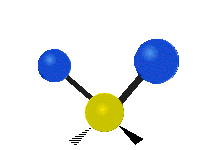
Las vibraciones moleculares son uno de los tres tipos diferentes de movimiento de las moléculas, junto con el movimiento de traslación (cuando toda la molécula se desplaza en la misma dirección) y el movimiento de rotación (cuando la molécula gira, como una peonza). Estas vibraciones corresponden a movimientos relativos entre los átomos que componen la molécula: estiramientos y variaciones en los ángulos entre enlaces, que pueden describirse de forma intuitiva como si los átomos fueran bolas conectadas por muelles.
El movimiento vibratorio de una molécula se produce cuando los enlaces entre los átomos de una molécula se mueven. Piensa en los átomos como si fueran bolas redondas unidas por un muelle que puede estirarse hacia delante y hacia atrás. Un ejemplo de este movimiento es el estiramiento, el ejemplo más simple de una vibración para una molécula y que ocurre entre sólo dos átomos. Algunos ejemplos de moléculas que exhiben este tipo de vibración en su forma más simple son el hidrógeno H 2, el nitrógeno N 2 y el oxígeno O 2.
Tipos básicos de vibraciones
- Estiramiento (stretching): cambio en la distancia entre dos átomos unidos. Puede ser sintético (simétrico) o asimétrico según si los enlaces se alargan/contraen al mismo tiempo o de forma opuesta.
- Flexión o doblamiento (bending): cambio en el ángulo entre tres átomos. Incluye modos como scissoring (tijera), rocking (balanceo), wagging (menear) y twisting (torsión).
- Modos fuera del plano: en moléculas no lineales, algunos átomos se mueven perpendicularmente al plano definido por otros átomos (ej. modo de "paraguas" en NH3).
Modos normales y número de vibraciones
Cualquier molécula con N átomos tiene un número finito de modos vibracionales independientes, llamados modos normales. El número total de modos normales es:
- 3N − 5 para moléculas lineales
- 3N − 6 para moléculas no lineales
Estos modos son combinaciones de movimientos individuales de los átomos que ocurren con frecuencias bien definidas y que, en el caso ideal, no intercambian energía entre sí.
Enfoque cuántico y clásico
Clásicamente, las vibraciones pueden modelarse como masas unidas por muelles (oscilador armónico). Cuánticamente, cada modo vibracional tiene niveles discretos de energía: E = (v + 1/2)hν, donde v es el número cuántico vibracional, h la constante de Planck y ν la frecuencia del modo. Incluso en el estado más bajo existe energía residual denominada energía de punto cero. La aproximación armónica es válida para pequeños desplazamientos; desviaciones dan lugar a anharmonicidad, que explica fenómenos como la separación desigual entre niveles energéticos y la posibilidad de sobretonos.
Detección: espectroscopía infrarroja y Raman
Las vibraciones moleculares se estudian principalmente con espectroscopia infrarroja (IR) y espectroscopia Raman. Cada técnica tiene reglas de selección distintas:
- En IR, una vibración es activa si produce un cambio en el momento dipolar de la molécula durante el movimiento.
- En Raman, una vibración es activa si provoca un cambio en la polarizabilidad de la molécula.
Las frecuencias se suelen expresar en número de onda (cm−1) o en terahercios (THz). Ejemplos típicos de posiciones de bandas: estiramientos O–H alrededor de 3200–3600 cm−1, estiramientos C=O cerca de 1650–1750 cm−1, estiramientos C–H en 2800–3100 cm−1.
Ejemplos básicos
- Diatómicos (H 2, N 2, O 2): sólo tienen un modo vibracional de estiramiento. Sus espectros vibracionales son simples y sirven como modelos para el oscilador armónico.
- Triatómicas lineales (CO2): tienen 3N−5 = 4 modos; dos estiramientos (simétrico y asimétrico) y dos modos de flexión degenerados. El estiramiento asimétrico es activo en IR, el simétrico generalmente no lo es pero puede ser Raman activo.
- Triatómicas no lineales (H2O): tienen 3N−6 = 3 modos: dos estiramientos (simétrico y asimétrico) y un modo de flexión (bending).
- Moléculas más grandes: presentan muchas más bandas; la interpretación requiere modelos y cálculos teóricos (química computacional) para asignar modos normales a bandas experimentales.
Importancia y aplicaciones
El estudio de las vibraciones moleculares es esencial en química y física para:
- Identificar grupos funcionales en compuestos orgánicos mediante IR y Raman.
- Caracterizar materiales, polímeros y nanotubos.
- Investigar procesos dinámicos como reacciones químicas y transferencia de energía.
- Astrofísica y detección remota: muchas moléculas en el espacio se identifican por sus bandas vibracionales.
En resumen, las vibraciones moleculares son movimientos internos de los átomos en una molécula que determinan propiedades espectroscópicas y termodinámicas clave. Desde el modelo simple del muelle hasta la descripción cuántica y las técnicas experimentales modernas, su estudio permite comprender y caracterizar la estructura y comportamiento molecular en múltiples disciplinas científicas.