El cloroformo (también llamado triclorometano) es una sustancia química. Es un compuesto orgánico. El cloroformo es una de las sustancias intermedias que aparecen en la producción de politetrafluoroetileno, más conocido como teflón. El cloroformo se utiliza como disolvente. En el siglo XIX, era un anestésico muy utilizado.
Definición y fórmula
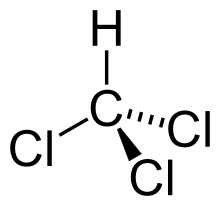
El cloroformo es el nombre común del triclorometano, cuya fórmula química es CHCl3. Es un derivado halogenado del metano en el que tres átomos de hidrógeno han sido sustituidos por átomos de cloro.
Propiedades físicas y químicas
- Apariencia: líquido incoloro con olor característico, algo dulce.
- Fórmula molecular: CHCl3.
- Masa molar: ≈ 119,38 g·mol−1.
- Punto de ebullición: ≈ 61,2 °C.
- Punto de fusión: ≈ −63,5 °C.
- Densidad: ≈ 1,48 g·cm−3 (más denso que el agua).
- Solubilidad en agua: baja (≈ 8 g·L−1 a 20 °C), pero miscible con muchos disolventes orgánicos.
- Inflamabilidad: no inflamable en condiciones normales, aunque puede descomponerse y formar subproductos peligrosos.
- Reactividad: relativamente estable, pero puede oxidarse en presencia de aire, luz y ciertos catalizadores para formar compuestos tóxicos como el fosgeno (COCl2).
Usos actuales y usos históricos
- Usos históricos: en el pasado se empleó como anestésico general; su uso médico fue abandonado por efectos adversos (cardiotoxicidad, hepatotoxicidad) y por el desarrollo de anestésicos más seguros.
- Usos industriales y de laboratorio: disolvente para grasas, resinas, cloración y síntesis orgánica; intermedio en la fabricación de otros compuestos como el politetrafluoroetileno (teflón).
- Formación no intencional: aparece como subproducto (trihalometano) durante la cloración del agua cuando el cloro reacciona con materia orgánica natural; por eso se detecta en aguas tratadas.
- Limitación de usos: muchos usos se han restringido o reemplazado por razones de salud y medioambientales.
Producción y origen ambiental
Industrialmente se obtiene por cloración controlada de compuestos hidrocarbonados (por ejemplo mediante la cloración radicalaria de metano o de derivados). Además, puede formarse de manera no intencional en plantas de tratamiento de agua cuando se usa cloro como desinfectante y existe materia orgánica en el agua.
Riesgos para la salud
El cloroformo es tóxico por inhalación, ingestión y absorción cutánea. Sus efectos dependen de la dosis y de la vía de exposición.
- Efectos agudos: exposición alta puede causar mareo, náuseas, dolor de cabeza, somnolencia, pérdida de conciencia, depresión respiratoria y arritmias cardiacas. La exposición masiva puede ser mortal.
- Efectos crónicos: la exposición repetida o prolongada puede dañar hígado y riñones, y afectar al sistema nervioso central.
- Carcinogenicidad: el cloroformo está clasificado por organismos internacionales como posible carcinógeno para los humanos (clasificaciones como la IARC lo sitúan en categorías de sospecha de carcinogenicidad). Por ello, su manejo y liberación al ambiente están regulados.
- Metabolismo tóxico: en el organismo se metaboliza en el hígado a especies reactivas (entre ellas compuestos carbonílicos como el fosgeno a nivel bioquímico), responsables de daño hepático y renal.
Prevención, primeros auxilios y manejo seguro
- Prevención: evitar la inhalación de vapores (uso de campana extractora y EPI adecuados: guantes, gafas y respirador homologado si es necesario). Mantener recipientes bien cerrados, en lugares frescos y oscuros para minimizar la formación de subproductos peligrosos.
- Almacenamiento: en envases cerrados, resistentes a la corrosión, preferiblemente opacos; evitar la exposición a luz intensa y fuentes de calor. A veces se estabiliza con pequeñas cantidades de etanol u otros inhibidores para reducir la formación de fosgeno.
- Primeros auxilios:
- Inhalación: trasladar a la víctima al aire fresco; si hay dificultad respiratoria buscar asistencia médica inmediatamente.
- Contacto con la piel: retirar ropa contaminada y lavar la zona con agua y jabón abundante.
- Contacto con ojos: enjuagar con agua abundante varios minutos y buscar atención médica.
- Ingestión: no provocar el vómito; buscar atención médica urgente.
Impacto ambiental y eliminación
El cloroformo es volátil y puede escapar al aire, persistiendo en el ambiente el tiempo suficiente para dispersarse. En ecosistemas puede afectar a organismos acuáticos y su liberación está regulada. La eliminación debe realizarse como residuo peligroso mediante gestores autorizados; no debe verterse a desagües ni al medio ambiente. Los métodos de tratamiento incluyen incineración controlada en instalaciones autorizadas y procesos de eliminación especializados.
Regulación y recomendaciones
Por su toxicidad y riesgo potencial para la salud y el medio ambiente, el uso del cloroformo está regulado en muchos países: se restringen las emisiones industriales, su uso como anestésico se abandonó y su presencia en el agua potable se controla como parte de los subproductos de desinfección (trihalometanos). Si trabaja con cloroformo consulte la normativa local y las hojas de datos de seguridad (FDS/SDS) correspondientes.
Conclusión
El cloroformo (triclorometano) fue históricamente importante como anestésico, y hoy se emplea como disolvente e intermedio químico, aunque su uso es mucho más limitado por razones de salud y ambientales. Es un líquido volátil, de baja solubilidad en agua y alto potencial tóxico; su manejo exige precauciones, control de emisiones y eliminación adecuada.






-2.png)