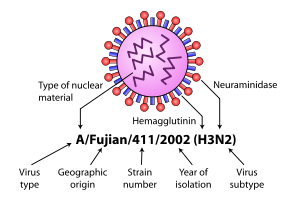
Los Orthomyxoviridae (orthos, griego para "recto"; myxa, griego para "moco") son una familia de virus de ARN. Incluyen cinco géneros: Influenzavirus A, Influenzavirus B, Influenzavirus C, Thogotovirus e Isavirus. Los tres primeros géneros contienen virus que causan la gripe en los vertebrados, incluidas las aves (véase también la gripe aviar), los seres humanos y otros mamíferos. Los isavirus infectan al salmón; los togotovirus infectan a vertebrados e invertebrados, como los mosquitos y los piojos de mar.
Los tres géneros de Influenzavirus se distinguen por la estructura de sus proteínas. Infectan a los vertebrados de la siguiente manera:
Géneros y hospedadores principales
- Influenzavirus A: infecta a aves (especialmente aves acuáticas silvestres, que son el principal reservorio), a múltiples especies de mamíferos (incluidos humanos, cerdos, caballos, focas y otros). Es el género responsable de las pandemias humanas debido a su gran diversidad antigénica.
- Influenzavirus B: circula principalmente en seres humanos y, en menor medida, en focas. Produce epidemias estacionales pero no ha causado pandemias a gran escala como A.
- Influenzavirus C: infecta a humanos y a algunos mamíferos (por ejemplo, cerdos) y suele provocar enfermedades respiratorias más leves; tiene menor impacto epidemiológico que A y B.
- Thogotovirus: incluye virus transmitidos por artrópodos (principalmente garrapatas) que pueden infectar vertebrados e invertebrados; algunos se han asociado a enfermedades neurológicas o sistémicas en animales y ocasionalmente en humanos.
- Isavirus: comprende el virus de la anemia infecciosa del salmón (infectious salmon anemia virus, ISAV), agente de importancia veterinaria y económica en la acuicultura.
Características virológicas principales
- Son virus envueltos con una membrana lipídica que presenta glicoproteínas de superficie (por ejemplo, hemaglutinina HA y neuraminidasa NA en los influenzavirus A y B; en influenza C la glicoproteína principal es la hemaglutinina esterasa fusión HEF).
- Tienen genoma de ARN monocatenario sentido negativo y segmentado. El número de segmentos varía según el género (generalmente entre 6 y 8 segmentos), lo que facilita la recombinación por reasortamiento cuando una célula es coinfectada por dos virus diferentes.
- La replicación ocurre en el núcleo celular, una característica poco común entre los virus de ARN.
Mecanismos de variación y repercusiones epidemiológicas
Los influenzavirus cambian antigénicamente por dos procesos principales:
- Deriva antigénica (antigenic drift): acumulación gradual de mutaciones puntuales en los genes que codifican las proteínas de superficie (HA y NA), lo que permite que el virus escape parcialmente a la inmunidad poblacional; es la causa de las epidemias estacionales.
- Salto antigénico o reassortment (antigenic shift): intercambio de segmentos génicos entre virus distintos que infectan la misma célula; esto puede producir virus radicalmente nuevos para los humanos y dar lugar a pandemias (fenómeno típico en Influenzavirus A).
Transmisión y clínica
- Transmisión principalmente por gotículas respiratorias, aerosoles y contacto con superficies contaminadas; en animales también por contacto directo o vector (en el caso de togotovirus).
- La enfermedad en humanos suele manifestarse con fiebre, tos, dolor de garganta, mialgias, cefalea y malestar general; puede complicarse con neumonía, infección bacteriana secundaria o exacerbar enfermedades crónicas. La gravedad varía según la cepa, la edad y condiciones del huésped.
- En aves y otros animales la presentación varía desde infecciones subclínicas hasta enfermedades sistémicas graves (p. ej., cepas altamente patógenas de gripe aviar).
Diagnóstico, tratamiento y prevención
- Diagnóstico: pruebas rápidas de antígenos (menor sensibilidad), RT‑PCR (estándar de oro por su sensibilidad y especificidad), cultivo viral y serología para estudios retrospectivos.
- Tratamiento: antivirales disponibles incluyen inhibidores de la neuraminidasa (oseltamivir, zanamivir, peramivir) y fármacos con otros mecanismos (por ejemplo, baloxavir marboxil). La eficacia depende del inicio temprano del tratamiento; además, la resistencia viral puede limitar la utilidad de algunos fármacos.
- Prevención: vacunas estacionales actualizadas anualmente (inactivadas, atenuadas o recombinantes) son la principal medida de control en humanos. En animales, medidas de bioseguridad, vigilancia, control de movimiento y, en algunos casos, vacunación específica. En brotes aviarios se aplican medidas estrictas como el sacrificio sanitario y cuarentena.
Vigilancia y control sanitario
La vigilancia global (por ejemplo, la Red Mundial de Vigilancia de la Gripe de la OMS, GISRS) monitorea las cepas circulantes para orientar la composición de las vacunas y detectar nuevas variantes con potencial pandémico. La detección temprana, el control en animales y la capacidad de respuesta sanitario-epidemiológica son claves para limitar el impacto de epidemias y pandemias.
Aspectos de laboratorio y biosafety
El manejo de muestras y cultivos de Orthomyxoviridae requiere prácticas de laboratorio y niveles de contención adecuados: generalmente BSL-2 para virus estacionales, con medidas adicionales (a veces BSL-3 o BSL-3 mejorado) para cepas altamente patógenas o para procedimientos que generan aerosoles. Los laboratorios deben seguir normativas nacionales e internacionales para manipulación, transporte y eliminación de materiales infecciosos.
Notas finales
Los Orthomyxoviridae son agentes virológicos de gran relevancia médica, veterinaria y económica. Su capacidad de cambio antigénico y la amplia diversidad de hospedadores hacen que la vigilancia continua, la investigación en vacunas y antivirales, y las medidas de salud pública sean fundamentales para su control.