Los anticuerpos (también llamados inmunoglobulinas) son grandes proteínas en forma de Y que pueden adherirse a la superficie de bacterias y virus. Se encuentran en la sangre u otros fluidos corporales de los vertebrados y son producidos por células del sistema inmune llamadas linfocitos B (y sus descendientes, las células plasmáticas). Los anticuerpos son el elemento clave del sistema inmunitario adaptativo y permiten al organismo reconocer y responder de forma específica frente a agentes extraños.
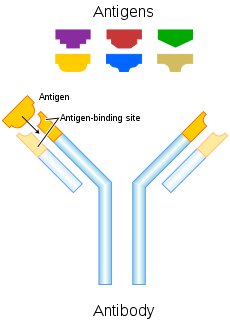
El anticuerpo reconoce una parte única de la diana extraña llamada antígeno. Cada punta de la "Y" de un anticuerpo contiene una estructura (como una cerradura) que encaja con una estructura particular similar a una llave en un antígeno. Esto une las dos estructuras y determina la especificidad del anticuerpo.
Mediante este mecanismo de unión, un anticuerpo puede marcar un microbio o una célula infectada para que sea atacada por otras partes del sistema inmunitario, o puede neutralizar su objetivo directamente. La producción de anticuerpos es la principal función de la inmunidad humoral, y contribuye tanto a la eliminación de infecciones como a la prevención de reinfecciones mediante la memoria inmunológica.
Cada anticuerpo es diferente. Todos están diseñados para atacar un solo tipo de antígeno (en la práctica, esto significa virus o bacterias). Por ejemplo, un anticuerpo diseñado para destruir la viruela es incapaz de atacar la peste bubónica o el resfriado común. Aunque la estructura general de todos los anticuerpos es muy similar, esa pequeña región en la punta de la proteína es extremadamente variable. Esto permite que existan millones de anticuerpos con estructuras de punta diferentes. Cada una de estas variantes puede unirse a un antígeno diferente, proporcionando una enorme diversidad para reconocer múltiples amenazas.
Estructura básica
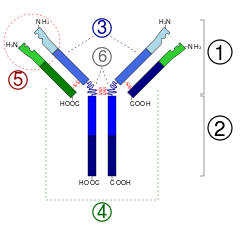
Un anticuerpo típico está formado por cuatro cadenas polipeptídicas: dos cadenas pesadas y dos cadenas ligeras unidas por enlaces disulfuro. Se distinguen dos regiones principales:
- Región variable (Fab): situada en las puntas de la "Y", contiene el sitio que reconoce el antígeno. Es la parte más diversa entre anticuerpos distintos.
- Región constante (Fc): la "base" de la Y; determina la clase de inmunoglobulina y medía interacciones con células del sistema inmune y con el sistema del complemento.
Funciones principales
Los anticuerpos participan en varias acciones defensivas:
- Neutralización: bloquean sitios clave en virus o toxinas para impedir que infecten células o ejerzan su efecto.
- Opsonización: recubren microbios para facilitar que fagocitos (macrófagos y neutrófilos) los reconozcan y eliminen.
- Activación del complemento: especialmente eficaz con IgM e IgG; el complemento ayuda a lisar bacterias y a promover la inflamación y la fagocitosis.
- Aglutinación y precipitación: unen partículas (bacterias, células o antígenos solubles) formando agregados que son más fáciles de eliminar.
- Cito/antibody-dependent cellular cytotoxicity (ADCC): anticuerpos pueden dirigir células efectoras (como células NK) para destruir células infectadas o tumorales.
Tipos de anticuerpos (isotipos)
- IgG: la más abundante en sangre; buena para neutralizar y activar el complemento. Puede atravesar la placenta y confiere protección pasiva al feto.
- IgM: suele ser la primera respuesta a una infección; forma pentámeros, excelente para activar el complemento.
- IgA: predominante en secreciones mucosas (saliva, lágrimas, leche materna) y protegiendo mucosas respiratorias y digestivas; suele ser dimérica en secreciones.
- IgE: implicada en reacciones alérgicas y defensa contra parásitos; se une a mastocitos y basófilos provocando liberación de mediadores inflamatorios.
- IgD: presente en la superficie de linfocitos B como receptor; su función completa en sangre circulante no está totalmente clara.
Cómo se generan los anticuerpos
La enorme diversidad de anticuerpos se debe a procesos en los linfocitos B:
- Recombinación somática (V(D)J): durante el desarrollo de los linfocitos B se reordenan segmentos génicos para crear regiones variables distintas, generando multitud de especificidades.
- Mutación somática y selección por afinidad: tras la exposición al antígeno, en los centros germinales de los ganglios linfáticos las células B someten sus genes variables a cambios que pueden aumentar la afinidad, y las de mayor afinidad se seleccionan.
- Cambio de clase: las células B pueden cambiar la clase de anticuerpo que producen (por ejemplo de IgM a IgG o IgA) sin cambiar la especificidad por el antígeno, adaptando la función efectora.
- Después de la activación, algunas células B se diferencian en células plasmáticas productoras de grandes cantidades de anticuerpo, y otras en células B de memoria que permiten respuestas más rápidas en futuras exposiciones.
Papel en la inmunidad y en medicina
- Vacunas: inducen la producción de anticuerpos y generación de memoria, lo que protege frente a futuras infecciones.
- Diagnóstico: pruebas como ELISA, inmunoblot o tests rápidos detectan anticuerpos para saber si ha habido exposición a un patógeno.
- Terapéutica: los anticuerpos monoclonales se emplean como fármacos contra cáncer, enfermedades autoinmunes e infecciones (p. ej. anticuerpos monoclonales contra sustancias específicas o patógenos).
- Transferencia pasiva: anticuerpos maternos (principalmente IgG) protegen al recién nacido; la leche materna aporta IgA para las mucosas del bebé.
Limitaciones y aspectos clínicos
- Evasión del sistema inmune: algunos patógenos cambian sus antígenos (variación antigénica) para escapar de anticuerpos previos.
- Reacciones adversas: anticuerpos dirigidos contra componentes propios pueden causar enfermedades autoinmunes. IgE puede mediar alergias y anafilaxia.
- Antibody-dependent enhancement (ADE): en ciertos casos raros, anticuerpos no neutralizantes pueden facilitar la entrada viral a células, empeorando la infección (fenómeno estudiado en algunos virus).
Medición y duración
Los niveles de anticuerpos se miden en títulos o unidades específicas. Tras una infección o vacunación, la respuesta primaria suele mostrar primero IgM y después IgG; en exposiciones posteriores se produce una respuesta secundaria más rápida y potente, dominada por IgG de mayor afinidad. La vida media de anticuerpos varía según la clase (por ejemplo, la IgG tiene una vida media relativamente larga en plasma).
En resumen, los anticuerpos son herramientas altamente especializadas del sistema inmunitario adaptativo: reconocen con precisión antígenos, neutralizan y facilitan la eliminación de patógenos, y constituyen la base de muchas estrategias preventivas y terapéuticas modernas.