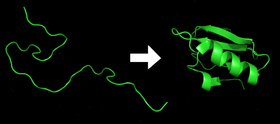
El plegado de proteínas es el proceso por el que una proteína adquiere su forma funcional o "conformación". Es, en gran medida, un proceso de autoorganización guiado por la secuencia de aminoácidos y por las interacciones físicas entre sus residuos. Partiendo de una bobina aleatoria, los polipéptidos se pliegan hasta alcanzar una estructura estable que puede realizar una función biológica. La forma final y la estabilidad se mantienen mediante varias fuerzas físicas, entre ellas enlaces de hidrógeno, interacciones hidrofóbicas, enlaces disulfuro, interacciones iónicas y fuerzas de Van der Waals.
El plegamiento ocurre principalmente de forma cotraduccional (mientras la cadena emerge del ribosoma) y/o postraduccional, y está influenciado por el entorno celular: la presencia de iones, la fuerza iónica, el pH, el potencial redox y chaperonas moleculares que facilitan el proceso. Muchas proteínas requieren asistencia para evitar agregación incorrecta y para alcanzar su estado nativo.
Las etapas generales del plegamiento incluyen:
- Al sintetizarse, cada proteína existe como un polipéptido desplegado o bobina aleatoria cuando se traduce de una secuencia de ARNm a una cadena lineal de aminoácidos. Este polipéptido carece de una estructura tridimensional desarrollada (estado inicial).
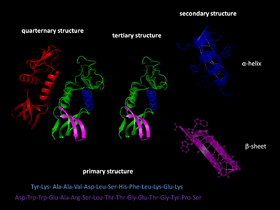
- Comienza la formación de estructuras secundarias (hélices α, láminas β) y un colapso hidrofóbico parcial que reduce la exposición de residuos hidrofóbicos al solvente. Se forman intermediarios de plegamiento y, en muchos casos, estados metaestables.
- Surge la estructura tridimensional bien definida: la proteína plegada funcional (estado nativo). La estructura tridimensional resultante viene determinada por la secuencia de aminoácidos (el llamado dogma de Anfinsen), aunque en la célula factores auxiliares modulan este proceso.
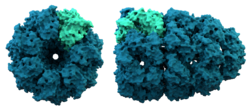
- Algunas proteínas se ensamblan con otras cadenas para formar complejos funcionales (estructura cuaternaria) y/o requieren modificaciones posraduccionales (glicosilación, formación de enlaces disulfuro, clivaje proteolítico) para ser funcionales.
- Partes de muchas proteínas pueden permanecer intrínsicamente desordenadas (sin plegarse en una estructura rígida) y esto es normal y funcional en numerosos casos (p. ej., regulación, reconocimiento molecular).
Elementos moleculares y maquinaria celular implicada: la energía libre del sistema dirige el plegamiento hacia estados de menor energía (modelo del "paisaje de energía en forma de embudo"). Las chaperonas (por ejemplo Hsp70, chaperoninas GroEL/GroES, Hsp90) y enzimas como la proteína disulfuro isomerasa (PDI) y peptidilprolil isomerasa facilitan el plegamiento correcto y la formación de enlaces disulfuro. Si una proteína está mal plegada, la célula dispone de vías de control de calidad —como el sistema ubiquitina-proteasoma y la autofagia— para eliminar o reparar estas proteínas.
Consecuencias del mal plegamiento
Si las proteínas no alcanzan su forma nativa, quedan inactivas y con frecuencia pueden agregarse formando oligómeros o fibrillas amiloides, que suelen ser tóxicos para las células. Se ha implicado el mal plegamiento y la agregación proteica en numerosas patologías:
- Enfermedades neurodegenerativas: Alzheimer (Aβ y tau), Parkinson (α-sinucleína), Huntington (huntingtina), esclerosis lateral amiotrófica (TDP‑43, SOD1), entre otras.
- Enfermedades por depósitos sistémicos o locales: amiloidosis por transtiretina, cadenas ligeras de inmunoglobulina (AL), y otras amiloidosis heredadas o adquiridas.
- Trastornos por defecto de plegamiento de proteínas específicas: fibrosis quística (misplegamiento y degradación del transportador CFTR ΔF508), déficit de alfa‑1 antitripsina (retención y daño hepático), y ciertas formas de diabetes por agregación de péptido amiloide pancreático.
- Enfermedades priónicas: donde la proteína priónica adquiere una conformación anómala que induce el cambio conformacional en otras moléculas normales, propagando la enfermedad.
El estrés del retículo endoplásmico (ER) por acumulación de proteínas mal plegadas activa la respuesta a proteínas desplegadas (UPR), que intenta restaurar la homeostasis; si falla, puede inducir apoptosis. Por eso el mantenimiento de la proteostasis (equilibrio de síntesis, plegamiento, reparación y degradación) es crítico para la salud celular.
Relevancia clínica y abordajes terapéuticos
- Diagnóstico: la presencia de depósitos proteicos (p. ej. amiloide) se detecta mediante biopsia, técnicas histológicas (tinción con rojo Congo), marcadores bioquímicos y neuroimagen. La identificación molecular de proteínas implicadas guía el diagnóstico y el pronóstico.
- Terapias dirigidas al plegamiento y a la proteostasis:
- Chaperonas farmacológicas y "correctores" que estabilizan la conformación nativa (por ejemplo, tafamidis estabiliza la transtiretina en ciertas amiloidosis hereditarias).
- Inhibidores de agregación y anticuerpos monoclonales dirigidos a especies tóxicas (en desarrollo clínico para algunas enfermedades neurodegenerativas).
- Estimulación de vías de degradación (aumentar autofagia o actividad proteasomal) y moduladores de la UPR.
- Terapias genéticas y edición para corregir mutaciones que causan misplegamiento.
- Prevención y manejo: en algunas afecciones hereditarias, el diagnóstico genético y el asesoramiento permiten intervenciones tempranas; además, el diseño de fármacos que mejoren el plegamiento o eviten la agregación es un campo activo de investigación.
Sin su correcta estructura tridimensional, una proteína no funciona. Sin embargo, algunas partes de las proteínas pueden no plegarse: esto es normal y funcional en muchos casos.
Si las proteínas no se pliegan en su forma nativa, quedan inactivas y suelen ser tóxicas. Se cree que varias enfermedades son el resultado de proteínas mal plegadas. Muchas alergias están causadas por el plegamiento de las proteínas, ya que el sistema inmunitario reconoce estructuras específicas; en la práctica, algunos alérgenos son proteínas especialmente estables (resistentes a la digestión y al calor) cuya conformación expone epítopos que inducen la sensibilización y la respuesta alérgica.
Conclusión: el plegamiento proteico es esencial para la función biológica y su estudio abarca desde la biofísica fundamental hasta aplicaciones clínicas. Comprender los mecanismos de plegamiento y misplegamiento permite desarrollar estrategias diagnósticas y terapéuticas para enfermedades relacionadas con la proteostasis.