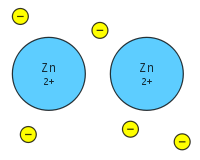
Un enlace metálico es la atracción electrostática entre múltiples iones metálicos positivos y un conjunto de electrones de valencia deslocalizados que se mueven libremente por la red cristalina. En otras palabras, los electrones actúan como un "pegamento" que mantiene unidos a los cationes metálicos y da al metal una estructura definida y cohesiva. Esto lo diferencia del enlace covalente y del enlace iónico; además, los metales suelen tener una energía de ionización baja, por lo que sus electrones de valencia pueden deslocalizarse con facilidad. Los electrones deslocalizados no están asociados a un núcleo concreto, sino que son libres de moverse por toda la estructura formando un "mar" de electrones.
Modelos y explicación a nivel atómico
Hay dos maneras complementarias y útiles de entender el enlace metálico:
- Modelo del mar de electrones: los átomos metálicos aportan sus electrones de valencia a un conjunto común, de modo que estos electrones móviles mantienen unidos a los iones positivos por atracción electrostática.
- Teoría de bandas: al acercarse muchos átomos metálicos, sus orbitales atómicos se solapan formando bandas de energía (banda de valencia y banda de conducción). Si la banda de conducción está parcialmente llena o hay solapamiento entre bandas, los electrones pueden moverse libremente bajo la acción de un campo eléctrico, lo que explica la conductividad eléctrica.
Propiedades derivadas del enlace metálico
Los enlaces metálicos son responsables de muchas características típicas de los metales:
- Maleabilidad y ductilidad: las capas de átomos pueden deslizarse unas sobre otras sin romper el enlace porque el "mar" de electrones sigue manteniendo la atracción entre iones; esto permite laminar y estirar los metales (maleabilidad, ductilidad).
- Brillo: la interacción de los electrones libres con la luz produce reflexión y absorción selectiva, de ahí el brillo metálico.
- Alta resistencia y puntos de fusión: la fuerte atracción entre electrones deslocalizados y iones da lugar a elevada resistencia mecánica y, en muchos casos, a puntos de fusión y ebullición altos (aunque existen excepciones).
- Conductividad eléctrica y térmica: los electrones móviles facilitan el transporte de carga y energía térmica a través del metal (conducción del calor y electricidad).
Conductividad eléctrica y térmica
Como los electrones se mueven libremente por la red metálica, los metales suelen ser buenos conductores eléctricos. Bajo la acción de un campo eléctrico, estos electrones se desplazan produciendo una corriente eléctrica. La misma movilidad electrónica facilita la transferencia rápida de energía cinética entre electrones y iones, lo que explica la alta conductividad térmica.
Hay excepciones y casos comparables fuera de los metales: por ejemplo, el grafito conduce electricidad porque tiene electrones deslocalizados en planos de carbono; y los compuestos iónicos fundidos o disueltos en agua conducen porque contienen iones libres en movimiento.
Factores que influyen en la fuerza del enlace metálico
- Número de electrones de valencia disponibles: cuantos más electrones deslocalizados aporte cada átomo, mayor suele ser la cohesión entre cationes y el "mar" electrónico.
- Tamaño atómico: a menor radio atómico, los iones positivos están más próximos y la atracción con los electrones es mayor, lo que refuerza el enlace.
- Tipo de empaquetamiento cristalino: estructuras compactas como FCC (cara centrada) o HCP (hexagonal compacta) favorecen una mayor cohesión; otros empaquetamientos, como BCC, presentan propiedades mecánicas diferentes.
- Enlaces metálicos específicos y compuestos: no todos los metales muestran un enlace puramente metálico en todas sus formas; la química y el estado de agregación pueden modificar el comportamiento.
Ejemplos y excepciones
Ejemplos típicos de metales con enlaces metálicos: cobre, aluminio, hierro, oro y plata. Estos muestran muchas de las propiedades comentadas (conductividad, brillo, maleabilidad).
No todos los metales forman exclusivamente enlaces metálicos. Por ejemplo, los iones de mercurio (Hg 2+
2) pueden establecer enlaces covalentes metal‑metal en determinados compuestos, y el mercurio elemental es líquido a temperatura ambiente debido a que sus fuerzas metálicas son relativamente débiles en comparación con otros metales.
Una aleación es una solución sólida de metales (o de un metal con otros elementos); las aleaciones combinan propiedades: muchas mantienen el brillo metálico y mejoran características mecánicas (por ejemplo, resistencia o dureza) en comparación con los metales puros.
Resumen
El enlace metálico es la interacción que surge cuando los electrones de valencia se deslocalizan y forman un «mar» que mantiene unidos a iones metálicos. Este tipo de enlace explica la mayoría de las propiedades distintivas de los metales: conductividad eléctrica y térmica, brillo, maleabilidad, ductilidad y, en general, buena resistencia mecánica. La teoría de bandas y el modelo del mar de electrones son herramientas útiles para entender cómo y por qué se producen estas propiedades, aunque hay excepciones y variaciones según la naturaleza del elemento y su estructura cristalina.