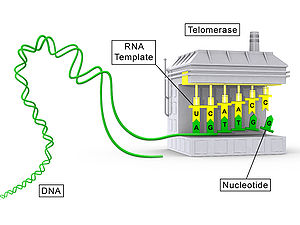
La telomerasa es una proteína de ARN que es una enzima con actividad de transcriptasa reversa. Añade repeticiones de secuencias de ADN ("TTAGGG" en todos los vertebrados) al final de las cadenas de ADN en las regiones de los telómeros. Es decir, la telomerasa es un ribonucleoproteína que utiliza su propia molécula de ARN como plantilla para sintetizar nuevas repeticiones teloméricas y así compensar el acortamiento producido por la replicación.
Estructura y componentes
La telomerasa es un complejo formado al menos por dos componentes esenciales:
- Una subunidad proteica catalítica (habitualmente denominada TERT), que posee la actividad de transcriptasa reversa.
- Una molécula de ARN (TER o TERC) que sirve de plantilla para añadir las repeticiones teloméricas.
Además, la actividad y función de los telómeros se regulan mediante proteínas asociadas (por ejemplo el complejo shelterin en eucariotas superiores, que incluye factores como TRF1, TRF2 y POT1), que protegen los extremos cromosómicos y controlan el acceso de la telomerasa.
Mecanismo de acción
Durante la replicación del ADN, la maquinaria replicativa no puede copiar completamente el extremo 3' de las hebras lineales, lo que provoca una pérdida progresiva de secuencia en cada ciclo de división celular. La telomerasa extiende el extremo 3' agregando repeticiones de TTAGGG (en vertebrados) usando su ARN interno como guía. Posteriormente, la vía convencional de replicación rellena la hebra complementaria. De este modo, la telomerasa evita la pérdida de secuencias codificantes y la fusión de cromosomas.
Función biológica
La principal función de los telómeros y de la telomerasa es proteger los extremos de los cromosomas y mantener la integridad genómica. Entre sus roles destacan:
- Evitar la pérdida de ADN importante durante la división celular.
- Prevenir la fusión de extremos cromosómicos y la activación inadecuada de respuestas a roturas en el ADN.
- Permitir la proliferación sostenida en células con alta demanda de división, como la línea germinal, células madre y linfocitos activados.
Telomerasa, envejecimiento y senescencia
Cada vez que se copia un cromosoma se pierde un fragmento del extremo: valores típicos varían según tejido y especie, y suelen estar en el orden de decenas a cientos de nucleótidos por división (en humanos se ha estimado entre ~50 y 200 nucleótidos). Como resultado, los telómeros se acortan progresivamente tras cada ciclo de replicación en células somáticas que carecen de actividad telomerasa suficiente. Cuando los telómeros alcanzan una longitud crítica, la célula entra en senescencia replicativa o activa programas de muerte celular, mecanismos implicados en el envejecimiento tisular y en la limitación de la proliferación celular.
El biólogo soviético Alexey Olovnikov predijo en 1973 la existencia de un mecanismo compensatorio del acortamiento telomérico y formuló la hipótesis de que el acortamiento de los telómeros podría estar relacionado con el envejecimiento y con el riesgo de cáncer. Estudios posteriores han confirmado que la longitud telomérica y la actividad de la telomerasa influyen en la capacidad regenerativa de tejidos y en algunos procesos relacionados con el envejecimiento.
Telomerasa y cáncer
Una de las características de la mayoría de los tumores humanos es la reactivación o activación de la telomerasa, lo que permite a las células cancerosas mantener o alargar sus telómeros y así proliferar de forma indefinida. Existen dos mecanismos principales por los que las células tumorales mantienen la longitud telomérica:
- Reactivación de la telomerasa: puede ocurrir por sobreexpresión de TERT, mutaciones en el promotor de TERT que aumentan su transcripción, o por mecanismos epigenéticos.
- ALT (Alternative Lengthening of Telomeres): un mecanismo recombinacional independiente de telomerasa que algunas células tumorales usan para alargar telómeros.
Debido a su papel en la inmortalización celular, la telomerasa es un objetivo terapéutico importante en oncología: inhibir su actividad podría limitar la proliferación tumoral. Sin embargo, la inhibición debe ser selectiva para evitar efectos adversos en células normales con actividad telomerasa (por ejemplo, células madre y células germinales).
Regulación y enfermedades asociadas
La expresión y la actividad de la telomerasa están fuertemente reguladas a varios niveles (transcripción, ensamblaje del complejo, modificaciones posraduccionales y control por proteínas asociadas). Defectos en los genes que codifican subunidades de la telomerasa o proteínas relacionadas provocan síndromes de insuficiencia telomérica, como la disqueratosis congénita, la fibrosis pulmonar y otros trastornos de fallo en tejidos con alta renovación.
Implicaciones clínicas y aplicaciones
- Diagnóstico y pronóstico: la longitud telomérica y la actividad telomerasa pueden servir como biomarcadores en ciertas enfermedades y cánceres.
- Terapias antitumorales: se están desarrollando inhibidores de la telomerasa (por ejemplo oligonucleótidos y fármacos como imetelstat) y estrategias inmunoterapéuticas dirigidas contra células que expresan TERT.
- Terapias regenerativas: existe interés en modular la telomerasa para mejorar la función de células madre y la reparación tisular, aunque elevar la actividad telomerasa conlleva riesgos oncogénicos si no se controla adecuadamente.
- Ensayos y técnicas: la actividad de la telomerasa se mide en laboratorio mediante ensayos como TRAP (Telomeric Repeat Amplification Protocol) y la longitud telomérica por PCR o hibridación in situ.
Descubrimiento e hitos históricos
La telomerasa fue descubierta por Carol Greider y Elizabeth Blackburn en 1984 en el ciliado Tetrahymena. Por este hallazgo, junto con Jack Szostak, Greider y Blackburn recibieron el Premio Nobel de Fisiología o Medicina en 2009. Sus trabajos establecieron las bases para comprender cómo se mantienen los extremos cromosómicos y cómo este proceso influye en la biología del envejecimiento y del cáncer.
En resumen, la telomerasa es un componente clave en la preservación de los telómeros y, por tanto, en la estabilidad genómica. Su actividad está finamente regulada: su carencia contribuye a la degeneración y al envejecimiento tisular, mientras que su reactivación promueve la inmortalidad celular en el cáncer, lo que la convierte en un objetivo central tanto para el estudio básico como para el desarrollo de nuevas terapias.