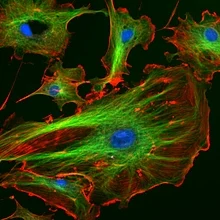
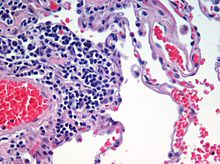
La tinción se utiliza en microscopía para que las células y los tejidos sean más fáciles de ver y comprender.
Es una forma de mejorar el contraste en la imagen microscópica. Las tinciones y los colorantes se utilizan a menudo en biología y medicina para resaltar las estructuras de los tejidos biológicos, a menudo con la ayuda de diferentes microscopios.
La tinción puede realizarse en tejidos vivos (in vivo) o en tejidos muertos (in vitro).
¿Qué es la tinción y cuál es su principio?
La tinción consiste en aplicar uno o varios colorantes que se unen con distinta afinidad a componentes celulares (núcleo, citoplasma, fibras, mucopolisacáridos, etc.) para generar contraste. Los colorantes pueden ser básicos (cationes) que tiñen componentes ácidos como el ADN y los ribosomas (p. ej. hematoxilina), o ácidos (aniones) que prefieren componentes básicos como proteínas citoplasmáticas (p. ej. eosina). Otros principios importantes incluyen la metacromasia (cambio de color según concentración o unión; ej. toluidina azul), el uso de mordientes para fijar colorantes y la especificidad por afinidad química o inmunológica.
Tipos de colorantes y ejemplos comunes
- Tinción general o de rutina: Hematoxilina y eosina (H&E) — resalta núcleos (azulado) y citoplasma/matriz (rosado).
- Tinciones especiales: PAS (ácido Schiff periódico) para carbohidratos y mucinas; Tricrómico de Masson para distinguir músculo, colágeno y fibrillas; Azul de Alcian para mucopolisacáridos ácidos.
- Tinciones para microbios: Gram (bacterias Gram +/−), Ziehl–Neelsen (bacilos ácido-alcohol resistentes como Mycobacterium), Giemsa/Wright (parasitos y frotis sanguíneos).
- Tinciones de impregnación: Plata/silver stains para fibras reticulares, neuronas y hongos.
- Técnicas inmunohistoquímicas (IHC): uso de anticuerpos dirigidos a antígenos específicos; detectores cromogénicos (DAB) o fluorescentes.
- Fluorocromos y microscopía de fluorescencia: DAPI (ADN), FITC, Alexa Fluor, TRITC — permiten marcaje múltiple y co-localización.
- Tinciones vitales: colorantes usados en tejidos o células vivas, p. ej. trypan blue (excluido por células viables), fluoresceína para estudios vasculares.
Técnicas habituales en histología y citología
- Hematoxilina y eosina (H&E): la más usada en anatomía patológica para evaluación general.
- Tinciones especiales: se emplean según la sospecha clínica (mucinas, lípidos, mielina, fibras elásticas, etc.).
- Inmunohistoquímica (IHC): para detectar proteínas específicas mediante anticuerpos; requiera a menudo recuperación antigénica y controles positivos/negativos.
- Inmunofluorescencia: indicada para localización subcelular y co-marcaje; puede realizarse en tejidos o células fijadas.
- Hibridación in situ (ISH): para localizar secuencias de ADN/ARN en cortes tisulares.
- Frotis y extendidos: coloración tipo Romanowsky (Giemsa/Wright) en hematología y parasitología.
Protocolo general en tinción histológica (pasos clave)
- Fijación: conserva la morfología (p. ej. formol 10%).
- Procesado y embebido: deshidratación, aclaramiento y embutición en parafina o congelación para criocortes.
- Corte: se obtienen secciones finas (microtomía) o cortes congelados.
- Desparafinización y rehidratación: antes de aplicar colorantes sobre cortes de parafina.
- Tinción: aplicación de colorantes y, si procede, pasos de diferenciación y lavado.
- Deshidratación, aclaramiento y montaje: preparar el portaobjetos para su observación y conservación.
- Controles: incluir controles técnicos y biológicos para asegurar especificidad y calidad.
Aplicaciones prácticas
- Diagnóstico en anatomía patológica (tumores, inflamación, necrosis).
- Identificación de microorganismos y su clasificación.
- Investigación celular y molecular (localización de proteínas o ácidos nucleicos).
- Evaluación de la viabilidad celular y estudios funcionales en vivo con tinciones vitales.
Controles, artefactos y limitaciones
La calidad del resultado depende de la fijación, del control del tiempo de tinción, de la calidad de los reactivos y de la técnica. Entre los artefactos comunes se encuentran: tinción desigual, desprendimiento de secciones, precipitados del colorante y pérdida antigénica. Es esencial incluir controles positivos y negativos, además de validar protocolos nuevos.
Seguridad y gestión de residuos
Muchos colorantes y disolventes son tóxicos o irritantes; algunos son potencialmente carcinogénicos. Se debe usar equipo de protección personal (guantes, gafas, campana), seguir las hojas de datos de seguridad (MSDS) y las normas del laboratorio para la eliminación de residuos líquidos y sólidos.
Consejos y resolución básica de problemas
- Si los núcleos no se tiñen bien, verifique la fijación y el pH de la hematoxilina.
- Si hay fondo excesivo, aumente los lavados o reduzca el tiempo de tinción.
- Para tinciones inmunohistoquímicas débiles, optimice la recuperación antigénica, la concentración del anticuerpo y los tiempos de incubación.
- Mantenga lotes de reactivos y controles documentados para reproducibilidad.
En resumen, la tinción en microscopía es una herramienta esencial para visualizar y distinguir componentes celulares y tisulares. La elección del colorante y la técnica dependerá del objetivo (diagnóstico, investigación, microbiología) y requiere protocolos controlados, controles adecuados y buenas prácticas de seguridad.